盐类水解的原理 知识点题库
 减小
D . 加入NaOH固体,溶液pH减小
减小
D . 加入NaOH固体,溶液pH减小
-
(1) 已知部分弱酸的电离常数如下表:
弱酸
HCOOH
HCN
H2CO3
电离常数
(25 ℃)
Ka=1.77×10-4
Ka=5.0×10-10
Ka1=4.3×10-7
Ka2=5.6×10-11
①HCOONa、NaCN、NaHCO3、Na2CO3这4种溶液中阴离子结合质子能力最强的是。
②体积相同、c(H+)相同的三种酸溶液a.HCOOH;
B.HCN;
C.H2SO4分别与同浓度的NaOH溶液完全中和,消耗NaOH溶液的体积由大到小的排列顺序是(填字母)。
③向NaCN溶液通入少量CO2反应的化学方程式是。
-
(2) ①一定浓度的NaCN溶液pH=9,用离子方程式表示呈碱性的原因是;此时c(HCN)/c(CN-)=。
②HCN溶液有挥发性,HCN是有剧毒的物质,实验室在做有关NaCN的实验时尽量不采用的实验条件是。
A、冰水浴 B、加热 C、浓溶液 D、稀溶液 E、酸性条件 F、碱性条件
③常温下,NaCN与过氧化氢溶液反应,生成NaHCO3和能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性。该反应的化学方程式是。
| 序号 | ① | ② | ③ | ④ |
| pH | 11 | 11 | 3 | 3 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
-
(1) 用K2FeO4给水消毒、杀菌时得到的Fe3+可以净水,Fe3+净水原因是(用离子方程式表示);但Fe3+净水要腐蚀设备,在腐蚀钢铁设备时,除H+作用外,另一主要原因是。
-
(2) 钢铁腐蚀造成很大损失,用如图装置防止钢铁腐蚀(烧杯中均为食盐水),X极的电极材料应是________________(填字母)。
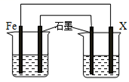 A . 锌 B . 铜 C . 银 D . 石墨
A . 锌 B . 铜 C . 银 D . 石墨 -
(3) 高铁电池是一种新型的二次电池,电解液为碱性溶液,其反应式如下:
3Zn + 2K2FeO4 + 8H2O
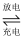 3Zn(OH)2 + 2Fe(OH)3 + 4KOH
3Zn(OH)2 + 2Fe(OH)3 + 4KOH①写出该电池放电时的正极反应式。
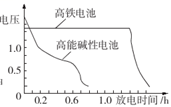
②如图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有。
-
(4) 从保护环境的角度考虑,制备K2FeO4较好的方法为电解法,其装置如图所示。
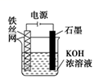
①石墨做电解池的极(填“阴”或“阳”),溶液中OH-向移动(填“铁丝网”或“石墨”)
②电解过程中阳极的电极反应式为。
③若维持电流强度为6A,电解5小时,理论上可制得K2FeO4的质量为g(已知F=96500 C/mol,结果保留1位小数)
-
(5) 已知25℃时Ksp[Fe(OH)3]=4.0×10-38 , 此温度下若在实验室中配制5 mol/L 500 mL FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入mL 2 mol/L的盐酸(滴加盐酸前后,溶液总体积不变)。
①0. 1 mol/L NH4Cl ②0. 1 mol/L CH3COONH4 ③0. 1 mol/L NH4HSO4 ④0. 1mol/L NH3·H2O
请根据要求填写下列空白:
-
(1) 溶液①呈性(填“酸”、“碱”或“中”),其原因是(用离子方程式表示)。
-
(2) 在上述四种溶液中,pH最小的是;c(NH4+)最小的是(填序号)。
-
(3) 室温下,测得溶液②的pH=7,则CH3COO-与
 浓度的大小关系是: c (CH3COO-) c(
浓度的大小关系是: c (CH3COO-) c(  ) (填“>”、“<”或“=”)。
) (填“>”、“<”或“=”)。
 + D2O ⇌ NH3·HDO + D+
B . NaH2PO4溶液:H2PO
+ D2O ⇌ NH3·HDO + D+
B . NaH2PO4溶液:H2PO  + H2O ⇌ HPO
+ H2O ⇌ HPO 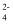 + H3O+
C . Na2CO3溶液:CO
+ H3O+
C . Na2CO3溶液:CO 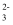 + 2H2O ⇌ H2CO3 + 2OH-
D . 明矾净水:Al3+ + 3H2O ⇌ Al(OH)3↓ + 3H+
+ 2H2O ⇌ H2CO3 + 2OH-
D . 明矾净水:Al3+ + 3H2O ⇌ Al(OH)3↓ + 3H+
 可以大量共存
B . 该溶液中,K+、CH3COO-、
可以大量共存
B . 该溶液中,K+、CH3COO-、  、F-可以大量共存
C . NH4Al(SO4)2可作净水剂,其净水原理;Al3++ 3H2O=Al(OH)3↓+3H+
D . 和足量Ba(OH)2稀溶液反应:2Ba2+ 5OH-+NH
、F-可以大量共存
C . NH4Al(SO4)2可作净水剂,其净水原理;Al3++ 3H2O=Al(OH)3↓+3H+
D . 和足量Ba(OH)2稀溶液反应:2Ba2+ 5OH-+NH  +Al3++2SO
+Al3++2SO  =2BaSO4↓ +NH3·H2O+AlO
=2BaSO4↓ +NH3·H2O+AlO  +2H2O
+2H2O
 B .
B .  C .
C . 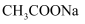 D .
D . 
①放热反应在常温下均能自发进行;
②电解过程中,化学能转化为电能而“储存”起来;
③原电池工作时所发生的反应一定有氧化还原反应;
④加热时,化学反应只向吸热反应方向进行;
⑤盐类均能发生水解反应;
⑥化学平衡常数的表达式与化学反应方程式的书写无关。
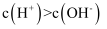 , 水溶液一定呈酸性
B . pH相等的盐酸和醋酸溶液:
, 水溶液一定呈酸性
B . pH相等的盐酸和醋酸溶液: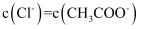 C . 0.010mol/L、0.10mol/L的醋酸溶液,电离度分别为
C . 0.010mol/L、0.10mol/L的醋酸溶液,电离度分别为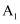 、
、 , 则
, 则 D . 浓度均为0.1mol/L的碳酸钠溶液和碳酸氢钠溶液均满足:
D . 浓度均为0.1mol/L的碳酸钠溶液和碳酸氢钠溶液均满足:
-
(1) I.联氨(N2H4)及其衍生物是一类重要的火箭燃料。N2H4与N2O4反应能放出大量的热。
在25℃时,1.00gN2H4(l)与足量N2O4(1)完全反应生成N2(g)和H2O(1),放出19.14kJ的热量。写出该反应的热化学方程式。
-
(2) II.NO2是氮的常见氧化物,能自发发生如下反应:2NO2(g)⇌N2O4(g)
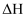 =-57.20kJ/mol
=-57.20kJ/mol写出该反应的平衡常数表达式K=。已知:在一定温度下的密闭容器中,该反应已达到平衡。保持其他条件不变,下列措施能提高NO2转化率的是。
a.减小NO2的浓度 b.降低温度 c.增大压强 d.升高温度
-
(3) III.Na2CO3俗称纯碱,是生活中的常用物质。某化学兴趣小组的同学对Na2CO3溶液显碱性的原因进行了探究,设计了如下实验方案进行操作并记录实验现象。
实验操作
实验现象
取少量Na2CO3固体,加入无水酒精,充分振荡、静置
溶液为无色
取上层清液于试管中,滴加酚酞试剂
溶液为无色
在试管中继续加入少量水
溶液变为红色
向该红色溶液中滴加足量BaCl2溶液(中性)
红色褪去
①该实验表明,Na2CO3溶液显碱性的原因是(请结合化学用语,简要说明)。
②从形成盐的酸和碱的强弱角度看,Na2CO3属于盐。
③为了使Na2CO3溶液中
 的比值变小,可适量加入(或通入)的物质是。
的比值变小,可适量加入(或通入)的物质是。a.CO2气体 b.KOH固体 c.HCl气体 d.Na2CO3固体
- 现有①干冰;②金刚石;③一氧化碳 三种物质,请你从这三种物质中,选择适当的物质按下列要求填空(填序号)。 (1)与血红蛋
- 2.如图表示生物体内的某种物质,请分析回答:(1)A包括____________元素。 (2)B的名称叫_______
- 《国家中长期教育改革和发展规划纲要(2010—2020年)》启动第二轮征求民意工作以来,社会各界反响热烈、参与踊跃,积极
- 一带电粒子沿图所示的曲线越过匀强电场,重力不计,则粒子带何种电荷以及该粒子在a 、b两点的动能大小,下列结论正确的是:(
- However,US speakers often use “may” ________British English
- 如图所示,物体A靠在竖直墙面上,在力F作用下,A、B保持静止。物体B的受力个数为: ( ) A
- 下列关于高倍镜使用的描述,错误的是()A .先在低倍镜下找到目标,并将目标移至视野中央,再转至高倍镜B .先用粗准焦螺旋
- 台湾是中国领土不可分割后部分。我国早在三国时期就与台湾有着密切的关系。当时在台湾与内地之间的经济文化交流做出重大贡献的人
- 从语法和逻辑的角度看,下列句子搭配合理的一句是( ) A.我国五亿农民自古以来就在这块土地上辛勤地劳动着,生活着。
- 下列各句中,括号中的成语使用恰当的一项是( ) A.雷锋一生很短暂,但所做的好事却极多,简直(罄竹难书)。
- (本题6分) 已知AB//EF,求∠A+∠ACE+∠E的度数。
- 如图,∠ABC=90°,D、E分别在BC、AC上,AD⊥DE,且AD=DE,点F是AE的中点,FD与AB相交于点M. (
- 请填写有关细胞工程的内容: (1)生物体的每一个细胞都包含有该物种的
- (1)如图a所示,如图所示的电压表的示数为 V; (2)如图b所示,温度计的示数是 ℃。
- Last July, my 12-year-old car died on California’s Santa Fre
- 下列关于能量转化的认识中错误的是() A.电解水生成氢气和氧气时,电能转化为化学能 B.绿色植物进行光合作用时,太阳能转
- 为了除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种试剂,过滤后,再加入适量的HCl,这种试剂(
- 7.某线性DNA分子含有5000个碱基对(bp),先用限制酶a切割,再把得到的产物用限制酶b切割,得到的DNA片段大小如
- 下列有关实验现象的描述,正确的是() A.白磷在空气中燃烧产生大量白雾 B.硫在氧气中燃烧,产生蓝紫色火焰 C.细铁丝在
- 2009年5月,航天飞机在完成对哈勃空间望远镜的维修任务后,在A点从圆形轨道I进入椭圆轨道II,B为轨道II上的一点,如



