盐类水解的原理 知识点题库
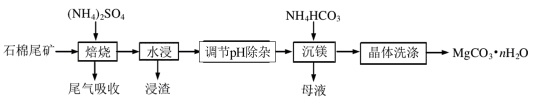
已知“焙烧”过程中的主反应为:
![]()
-
(1) 写出焙烧产物NH3的电子式。
-
(2) 为提高水浸速率,可采取的措施为(任写一条),“浸渣”的主要成分为。
-
(3) “调节pH除杂”时,需将pH调至5.0,则除去的杂质离子是,此时溶液中的c(Fe3+)=(已知Ksp[Fe(OH)3]=4.0×10-38)。
-
(4) “沉镁”过程中反应的离子方程式为。“沉镁”时若温度超过60℃,将产生较多的碱式碳酸镁杂质,原因是
 )+2c(H+)
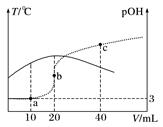
D . a、b、c 三点对应 NH
)+2c(H+)
D . a、b、c 三点对应 NH  的水解平衡常数:Kh(b)>Kh(a)>Kh(c)
的水解平衡常数:Kh(b)>Kh(a)>Kh(c)
| 选项 | 实验目的 | 实验操作 |
| A | 探究浓度对反应速率影响 | 向两支各盛有5mL0.1mol•L-1KMnO4溶液的试管中分别滴加2滴0.1mol•L-1H2C2O4和0.01mol•L-1H2C2O4 , 观察KMnO4溶液褪色所需时间 |
| B | 比较NaHSO3溶液中c( | 在pH试纸上滴2~3滴NaHSO3 溶液,测pH |
| C | 验证I-与Fe3+的反应有一定限度 | 向5mL0.1mol•L-1KI溶液中加入10mL0.1mol•L-1FeCl3溶液,充分反应后滴加KSCN 溶液 |
| D | 验证H2O2的氧化性比Fe3+强 | 将硫酸酸化的H2O2滴入Fe(NO3)2溶液,溶液变黄色 |
 )≈l.7×10-5 mol·L-1
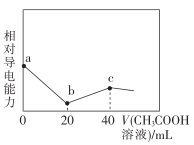
B . b点时混合溶液中:c(CH3COOH)<c(
)≈l.7×10-5 mol·L-1
B . b点时混合溶液中:c(CH3COOH)<c(  )
C . c点时混合溶液中:c(CH3COO- )+c(CH3COOH)=c(
)
C . c点时混合溶液中:c(CH3COO- )+c(CH3COOH)=c(  )+c(NH3·H2O)+c(Na+)
D . c点时混合溶液中:pH=7
)+c(NH3·H2O)+c(Na+)
D . c点时混合溶液中:pH=7
| 实验 | 实验操作和现象 |
| 1 | 测得0.1mol·L−1Na2C2O4溶液的pH≈8.4 |
| 2 | 向0.2mol·L−1Na2C2O4溶液中加入等体积0.2mol·L−1盐酸,测得混合后溶液的pH≈5.5 |
| 3 | 向0.1mol·L−1Na2C2O4溶液中滴加几滴酸性KMnO4溶液,振荡,溶液仍为无色 |
| 4 | 向0.1mol·L−1Na2C2O4溶液中加入等体积0.1mol·L−1CaCl2溶液,产生白色沉淀 |
下列有关说法错误的是( )
 )
B . 实验2得到的溶液中有c(H2C2O4)>c(Cl-)>c(C2O
)
B . 实验2得到的溶液中有c(H2C2O4)>c(Cl-)>c(C2O  )
C . 实验3中MnO
)
C . 实验3中MnO  被还原成Mn2+ , 则反应的离子方程式为2MnO
被还原成Mn2+ , 则反应的离子方程式为2MnO  +5C2O
+5C2O  +16H+=2Mn2++10CO2↑+8H2O
D . 依据实验4可推测Ksp(CaC2O4)<2.5×10−3
+16H+=2Mn2++10CO2↑+8H2O
D . 依据实验4可推测Ksp(CaC2O4)<2.5×10−3
-
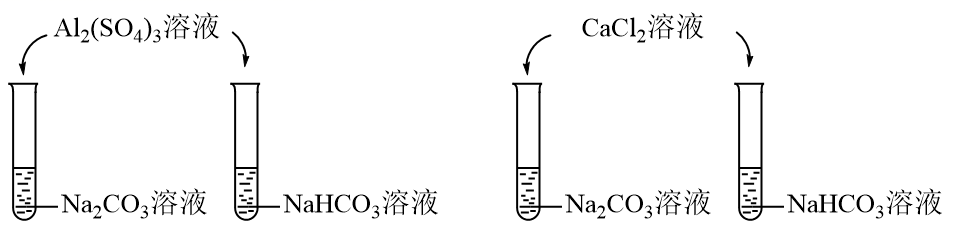
(1) 泡沫灭火器内装有NaHCO3饱和溶液,该溶液呈现碱性的原因是(用离子方程式表示);灭火器内另一容器中装有Al2(SO4)3溶液,该溶液呈酸性的原因是(用离子方程式表示):,当意外失火时,使泡沫灭火器倒过来摇动即可使药液混合,喷出大量的白色泡沫,阻止火势蔓延,其相关的离子方程式为:
-
(2) 在25 ℃时,将a mol·L-1的KCN溶液与0.01 mol·L-1的盐酸等体积混合,反应达到平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度a0.01 mol·L-1(填“>”、“<”或“=”);用含a的代数式表示HCN的电离常数Ka=。
 )>c(C2O
)>c(C2O  )
B . 0.1mol/L NaHC2O4溶液:c(C2O
)
B . 0.1mol/L NaHC2O4溶液:c(C2O  )>c(HC2O
)>c(HC2O  )>c(H2C2O4)
C . 0.1mol/L Na2C2O4溶液:c(OH-)-c(H+)=2c(H2C2O4)+ c(HC2O
)>c(H2C2O4)
C . 0.1mol/L Na2C2O4溶液:c(OH-)-c(H+)=2c(H2C2O4)+ c(HC2O  )
D . 0.1mol/L NaHC2O4溶液和0.1mol/L Na2C2O4溶液等体积混合:c(HC2O
)
D . 0.1mol/L NaHC2O4溶液和0.1mol/L Na2C2O4溶液等体积混合:c(HC2O  )+2 c(C2O
)+2 c(C2O  )<0.15mol/L
)<0.15mol/L
-
(1) 已知部分弱酸的电离常数如下表:
弱酸
HF
CH3COOH
H2CO3
H2S
电离平衡常数(25℃)
Ka=7.2×10-4
Ka=1.75×10-5
Ka1=4.30×10-7
Ka2=5.61×10-11
Ka1=9.1×10-8
Ka2=1.1×10-12
①写出H2S的Ka1的表达式:。
②常温下,浓度相同的三种溶液NaF、Na2CO3、CH3COONa,pH由大到小的顺序是。
③将过量H2S通入Na2CO3溶液,反应的离子方程式是。
-
(2) 室温下,用0.100 mol·L-1盐酸溶液滴定20.00 mL 0.100 mol·L-1的氨水溶液,滴定曲线如图所示。
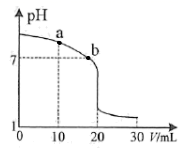
(忽略溶液体积的变化,①②填“>”“<”或“=”)
①a点所示的溶液中c (NH3·H2O)c (Cl-)。
②b点所示的溶液中c (Cl-)c (NH
 )。
)。③室温下pH=11的氨水与pH=5的NH4Cl溶液中,由水电离出的c (H+)之比为。
-
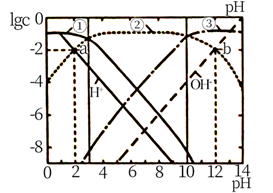
(3) 雌黄(As2S3)可转化为用于治疗白血病的亚砷酸(H3AsO3)可以用于治疗白血病,其在溶液中存在多种微粒形态,各种微粒物质的量分数与溶液的pH 关系如下图所示:
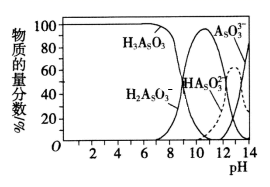
①人体血液的pH在7.35 -7.45之间,用药后人体中含砷元素的主要微粒是 。
②将KOH 溶液滴入亚砷酸溶液,当pH 调至11 时发生反应的离子方程式是。
③下列说法正确的是(填字母序号)
a.n(H3AsO3)∶n(H2AsO
 )=1∶1时,溶液显碱性
)=1∶1时,溶液显碱性b.pH=12时,溶液中c(H2AsO
 )+2c(HAsO
)+2c(HAsO  )+3c(AsO
)+3c(AsO 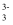 )+c(OH-)=c(H+)
)+c(OH-)=c(H+)c.在K3AsO3溶液中,c(AsO
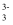 )>c(HAsO
)>c(HAsO  )>c(H2AsO
)>c(H2AsO  )
)
 的平衡常数
的平衡常数 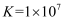 D . 25℃时,0.1mol/L的NaHA溶液中:
D . 25℃时,0.1mol/L的NaHA溶液中: 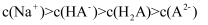
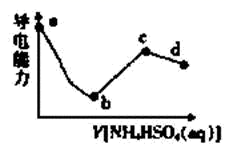
 D . bc段之间存在某点,其溶液中:c(NH4+)=2c(SO42-)
D . bc段之间存在某点,其溶液中:c(NH4+)=2c(SO42-)
 )/c(HC2O4)]随溶液pH的变化关系如图所示。下列说法正确的是( )
)/c(HC2O4)]随溶液pH的变化关系如图所示。下列说法正确的是( ) 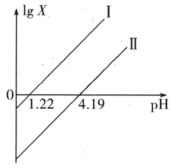
 )>c(H2C2O4)>c(C2O
)>c(H2C2O4)>c(C2O  )
D . 当pH=4.22时,溶液中c(HC2O
)
D . 当pH=4.22时,溶液中c(HC2O  ):c(H2C2O4)=1000:1
):c(H2C2O4)=1000:1
-
(1) 用离子方程式表示 NH4Cl 溶液显示酸性的原因:。
-
(2) 有机物 M 经过太阳光光照可转化成 N,转化过程如下:
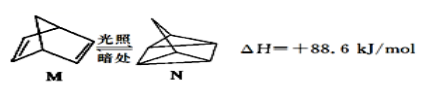
则 M、N 相比,较稳定的是。
-
(3) 已知在常温常压下:
①2CH3 OH(l)+3O 2 (g) =2CO2(g)+4H2O(g) ΔH=-1275.6 kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
写出表示甲醇燃烧热的热化学方程式。
 含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(
含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(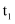 ,
,  )海水中
)海水中 浓度与模拟空气中
浓度与模拟空气中 浓度的关系曲线。下列说法错误的是( )
浓度的关系曲线。下列说法错误的是( )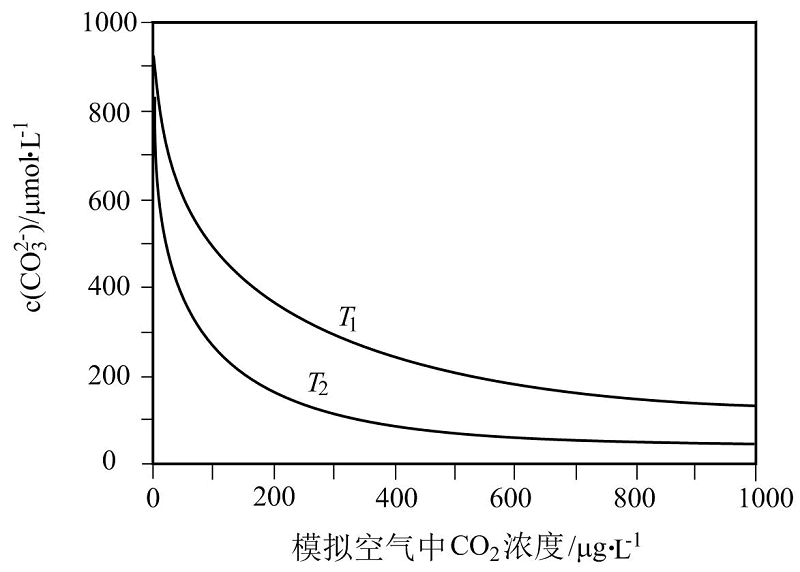
 浓度增加,海水中溶解的
浓度增加,海水中溶解的 随之增大,导致
随之增大,导致 浓度降低
B . 大气中
浓度降低
B . 大气中 含量增加时,海水中的珊瑚礁溶解的反应为:
含量增加时,海水中的珊瑚礁溶解的反应为:
 C . 当大气中
C . 当大气中 浓度确定时,海水温度越高,则
浓度确定时,海水温度越高,则 浓度越低
D . 海水呈弱碱性,是铝、铁元素在海水中含量少,而在陆地含量高的原因
浓度越低
D . 海水呈弱碱性,是铝、铁元素在海水中含量少,而在陆地含量高的原因
- 阅读下面的一段文字,完成5―7题。有人说2006年是草根文化全面崛起的一年。从“超女”的热天下到
- I’m in a situation quite _____ yours, also lack of experienc
- 民族团结是社会稳定的前提,是经济发展和社会发展的前提。作为公民,维护民族团结必须 ( ) A.实行民族区域自治政策
- 柳宗元的《小石潭记》的主旨句是:“ , 。”
- 下列对哺乳动物运动系统的描述中,你不认可的是( ) A.运动系统使身体能够产生各种动作 B.运
- 关于高压系统的叙述,正确的是( )A.高压系统只指高气压 B.高压系统气流下沉辐
- 设函数y=f(x)的定义域为D,若对于任意x1,x2∈D且x1+x2=2a,恒有f(x1)+f(x2)=2b,则称点(a
- 化合物III可由以下合成路线获得。 (1)I的分子式为________;II中含有的官能团名称为_______;II
- 解方程(本小题共6分)(1); (2)
- (10分)(1) 已知某粒子的结构示意图为: 试回答: ① 当x-y=10时,该粒子为 (填“原子
- M的名称是乙烯雌酚,它是一种激素类药物,结构简式如下.下列叙述不正确的是() A.M的分子式为C18H20O2 B.M可
- 第二节 书面表达(满分25分) 2012龙年央视春晚亮点之一,节目中无一广告植入。最近,某网站举行了一次题为“对今年春
- 康有为在诗中写道:“海东龙泣舰沉波,上相锚轩(古代使臣乘坐的一种轻车)出议和……台 人号泣秦桧歌,九城谣谍遍网罗
- 下列有关蛋白质合成的叙述中,正确的是 A.一个氨基酸只对应一个密码子 B.每一种氨基酸对应一种tRNA C.都在内质网上
- 使9 g乙二酸和某一定量二元醇完全酯化,生成W g酯和3.6 g水,则该醇的相对分子质量为
- He has changed a lot. He is not what he was used to be.
- 在抗洪救灾中,一架直升机通过绳索用恒力F竖直向上拉起一个漂在水面上的木箱,使其由水面开始加速上升到某一高度.若考虑空气阻
- (07年湖北卷文)(12分)已知函数(Ⅰ)求的最大值和最小值;(Ⅱ)若不等式上恒成立,求实数m的取值范围.
- He came home aftermidnight,and _____ , he was drunk. A.in
- 用单色光源照射一个不透光的圆板,在距圆板一定距离的屏上将观察到圆盘模糊不清的影,在阴影中心有一个____________
 )和c(H2SO3)大小
)和c(H2SO3)大小


