等效平衡 知识点题库
 2C(g) ΔH=-a kJ·mol-1(a > 0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2 , 在500℃时充分反应达到平衡后C的浓度为w mol·L-1 , 放出热量b kJ。
2C(g) ΔH=-a kJ·mol-1(a > 0),在一个有催化剂的固定容积的容器中加入2 mol A2和1 mol B2 , 在500℃时充分反应达到平衡后C的浓度为w mol·L-1 , 放出热量b kJ。
-
(1) a(填“>”“=”或“<”)b。
-
(2) 若将反应温度升高到700℃,该反应的平衡常数将(填“增大”“减小”或“不变”)。
-
(3) 若在原来的容器中,只加入2 mol C,500℃时充分反应达到平衡后,吸收热量c kJ,
C的浓度(填“>”“=”或“<”)w mol·L-1。
-
(4) 能说明该反应已经达到平衡状态的是。(填序号,下同)
a.v(C)=2v(B2) b.容器内压强保持不变
c.v逆(A2)=2v正(B2) d.容器内气体的密度保持不变
-
(5) 使该反应的反应速率增大,且平衡向正反应方向移动的操作是;能使B的 转化率增大的操作是;使平衡向逆反应方向移动的操作是。
a.及时分离出C气体 b.适当升高温度
c.增大B2的浓度 d..选择高效的催化剂
①2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH1=-70.8 kJ·mol-1
②CO(g)+2H2(g)  CH3OH(g) ΔH2
CH3OH(g) ΔH2
③2CH4(g)+O2(g)  2CH3OH(g) ΔH3=-251.0 kJ·mol-1
2CH3OH(g) ΔH3=-251.0 kJ·mol-1
-
(1) ΔH2=kJ·mol-1。
-
(2) 在恒容密闭容器里,按物质的量比1:1加入一定量的碳和水蒸气反应生成水煤气。一定条件下达到平衡,当改变反应的某一条件时,下列变化能说明平衡一定向正反应方向移动的是_________。(填序号)A . 正反应速率先增大后减少 B . 化学平衡常数K减少 C . 再加入一定量碳 D . 反应物气体体积分数增大
-
(3) 在体积可变的密闭容器中投入1mol CO和2mol H2 , 在不同条件下发生反应:CO(g)+2H2(g)
 CH3OH(g)。实验测得CH3OH的物质的量随温度、压强的变化如图所示。
CH3OH(g)。实验测得CH3OH的物质的量随温度、压强的变化如图所示。 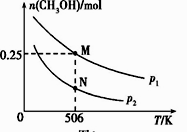
①该反应自发进行的条件是(填“低温”、“高温”或“任意温度”)
②506 K时,反应平衡时H2的转化率为;压强:p1(填“>”“<”或“=”)p2。
③反应速率:N点v正(CO)(填“>”“<”或“=”)M点v逆(CO)。
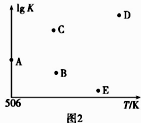
④若压强为p1、在1L恒容密闭容器中进行上述反应(起始投料不变),在不同温度下上述反应的平衡常数的对数(lg K)如图所示。则温度为506 K时,平衡常数K=(保留三位小数),B、C、D、E四点中能正确表示该反应的lg K与T的关系的点为。
-
(4) 在2L恒容密闭容器中充入a(a>0)mol H2、2mol CO和7.4mol CH3OH(g),在506 K下进行上述反应。为了使该反应逆向进行,a的范围为。
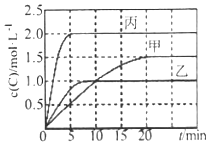
 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示:
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示: |
| 甲 | 乙 | 丙 | |
| 起始物质的量 | n(SO2)/mol | 0.4 | 0.8 | 0.8 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | |
| SO2的平衡转化率/% | 80 | α1 | α2 | |
下列判断中,正确的是( )
 N2O4(g) ΔH<0,下列说法正确的是( )
N2O4(g) ΔH<0,下列说法正确的是( )
 B(g)+3C(g) 达到平衡时,A、B和C的物质的量分别为6 mol、2 mol、6 mol。在保持温度和压强不变的情况下,下列说法正确的是( )
B(g)+3C(g) 达到平衡时,A、B和C的物质的量分别为6 mol、2 mol、6 mol。在保持温度和压强不变的情况下,下列说法正确的是( )
 2NH3(g) △H=-92.4kJ/mol];下列说法正确的是( )
2NH3(g) △H=-92.4kJ/mol];下列说法正确的是( ) 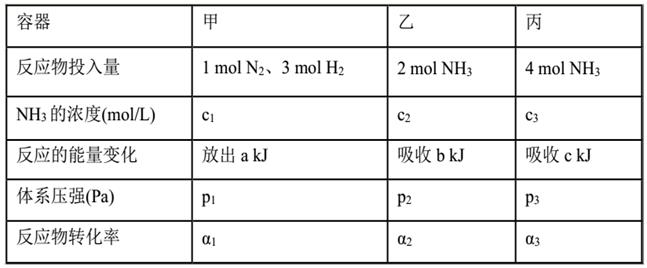
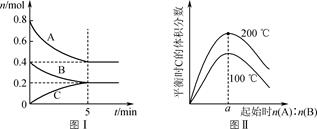
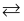 2Z(g) DH<0。当改变某个条件并达到新平衡后,下列叙述错误的是( )
2Z(g) DH<0。当改变某个条件并达到新平衡后,下列叙述错误的是( )
 xC(g),按不同方式投入反应物,测得反应达到平衡时的有关数据如下:
xC(g),按不同方式投入反应物,测得反应达到平衡时的有关数据如下: | 容器 | 甲 | 乙 | 丙 |
| 反应物的投入量 | 3molA、2molB | 9molA、6molB | 2molC |
| 达到平衡的时间/min | 5 | 8 | |
| A的浓度/mol·L-1 | c1 | c2 | |
| C的体积分数% | w1 | w3 | |
| 混合气体的密度/g·L-1 | ρ1 | ρ2 |
下列说法正确的是( )
 C(g)+3D(g)。现分别从两条途径建立平衡:Ⅰ.A和B的起始浓度均为2mol/L;Ⅱ.C和D的起始浓度分别为2 mol/L和6 mol/L。下列叙述正确的是 ( )
C(g)+3D(g)。现分别从两条途径建立平衡:Ⅰ.A和B的起始浓度均为2mol/L;Ⅱ.C和D的起始浓度分别为2 mol/L和6 mol/L。下列叙述正确的是 ( )
 ,测得有关数据如表:
,测得有关数据如表: | 时间/min | 0 | 10 | 20 | 40 | 50 | |
| T1 | | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | | 0.50 | 0.30 | 0.18 | - | 0.15 |
下列说法正确的是( )
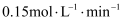 C . T2时CH4的平衡转化率为60.0%
D . T1时,保持其他变化不变,再充入0.5mol CH4和1.2mol NO2 , 达新平衡时N2的浓度增大
C . T2时CH4的平衡转化率为60.0%
D . T1时,保持其他变化不变,再充入0.5mol CH4和1.2mol NO2 , 达新平衡时N2的浓度增大
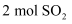 和
和 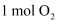 ,乙中充入
,乙中充入 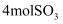 和
和 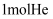 ,在恒定温度和相同的催化剂条件下,发生如下反应:
,在恒定温度和相同的催化剂条件下,发生如下反应:  .下列有关说法正确的是( )
.下列有关说法正确的是( ) 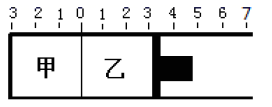
 B . 若活塞固定在3处不动,平衡时两容器中
B . 若活塞固定在3处不动,平衡时两容器中  的浓度:
的浓度: 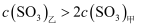 C . 若活塞固定在3处不动,平衡时两容器中
C . 若活塞固定在3处不动,平衡时两容器中  的体积分数:
的体积分数: 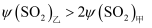 D . 若活塞固定在7处不动,达平衡时两容器中
D . 若活塞固定在7处不动,达平衡时两容器中 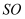 的物质的量分数相等
的物质的量分数相等
-
(1) CO还原NO的反应为
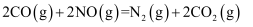 , 请回答下列问题:
, 请回答下列问题:①已知该反应为自发反应,则该反应的反应热△H0(填“>”或“<”或“=”)
②已知:

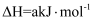
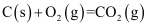
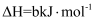
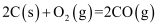
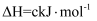
则
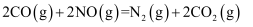 △H =
△H =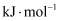 (用含a、b、c的表达式表示)。
(用含a、b、c的表达式表示)。③一定温度下,将2 mol CO、4 mol NO充入2 L密闭容器。5 min到达平衡,测得N2的物质的量为0.5 mol,则:
i.5min内v(NO)=。
ii.该条件下,可判断此反应到达平衡的标志是。
A.单位时间内,消耗2 mol CO同时形成1 mol N2
B.混合气体的平均相对分子质量不再改变。
C.混合气体的密度不再改变。
D.CO与NO的转化率比值不再改变。
④某研究小组探究催化剂对CO、NO转化的影响。将CO和NO以一定的流速通过两种不同的催化剂进行反应,相同时间内测量逸出气体中N2的含量,从而确定尾气脱氮率(即NO的转化率),结果如图所示:
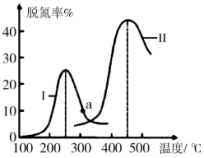
i.由图可知:要达到最大脱氮率,该反应应采取的最佳实验条件为。
ii.若低于200℃,图中曲线Ⅰ脱氮率随温度升高变化不大的主要原因为。
-
(2) 用焦炭还原NO的反应为:
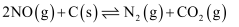 。恒容恒温条件下,向体积均为1 L的甲、乙、两三个容器中分别加入足量的焦炭和一定量的NO,测得各容器中NO的物质的量n(NO)随反应时间(t)的变化情况如下表所示:
。恒容恒温条件下,向体积均为1 L的甲、乙、两三个容器中分别加入足量的焦炭和一定量的NO,测得各容器中NO的物质的量n(NO)随反应时间(t)的变化情况如下表所示: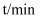
容器
0
40
80
120
160
甲/400℃
2.00
1.5
1.10
0.80
0.80
乙/400℃
1.00
0.80
0.65
0.53
0.45
丙/T℃
2.00
1.45
1.00
1.00
1.00
①T400℃(填“>”或“<”)。
②乙容器达平衡时n(N2)=mol。
容器 | 甲 | 乙 | 丙 |
容积 | 0.5L | 0.5L | 1.0L |
温度 | T1 | T2 | T2 |
反应物起始量 | 1.5molA0.5molB | 1.5molA0.5molB | 6molA2molB |
- 如图,轮A和轮B之间无相对滑动,轮B和轮C共轴转动。已知轮B的半径为r,轮A半径为2r,轮C半径为4r,当轮A匀速转动时
- 右图为小鼠(2n= 40)细胞正常分裂时有关物成或结构的数量变化曲线,下列分析错误的是A.若曲线表示有丝分裂染色体数目变
- 下列加点成语使用不正确的一项是( ) A.这一种仪式既经举行,即倘有后患,各部门都该负责,不能超然物外,说风凉
- 在“绿叶在光下制造淀粉”的实验里,把叶片放在酒精里隔水加热,酒精的作用是 ( ) A.溶解叶绿体
- China had decided to take action to stop the use of plastic
- 已知各项为正数的等差数列的前20项和为100,那么的最大值为 ( ) A.25
- 家庭的投资理财应根据不同的经济态势,采取不同的选择。当银行储蓄利率下降,企业经济效益大幅下滑时,下列最适宜的家庭投资理财
- 下列能体现公有制的主体地位的是( ) ①国有资产在社会总资产中占优势 ②国有经济对
- “湖广熟,天下足”表明长江中游地区是中国重要的产粮区,其主要原因是 A.雨热条件好,土壤肥沃 B.地形平坦,自
- 漫画《售“后”》反映的现象告诉我们( )①市场经济具有盲目性的弱点和缺陷 ②房地产公司制定了成功的经营战略 ③消费者
- It rained hard yesterday, __________ stopped me from going t
- 在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表。下列判断不正确的是() 0.
- 下列各组气体或溶液用括号内试剂加以鉴别,其中不合理的是() A.二氧化碳、氮气(澄清石灰水) B.氯化
- 如图,在中,点分别在边,,上,且,.下列四个判断中,不正确的是
- 南半球海洋上的月平均最高气温出现在 A.1月 B.2月
- 下列对下图所示生物学实验的叙述,正确的是A.若用显微镜观察图①中正在发生质壁分离的紫色洋葱表皮细胞,可见其液泡体积逐渐变
- Our school is no longer _________ is was 10 years ago, _____
- Luckily, I_______________ buy the ticket yesterday. A.
- (一)文言文阅读(19分) 阅读下面的文言文,完成小题。 王鼎字鼎臣,以进士第,累迁太常博士。时天子患吏治多弛,监司
- 读“不同类型国家人口年龄系数曲线图”,完成下列问题。发达国家和发民菜中国家老年人口系数超过少年儿童人口系数的时间依次是(




