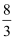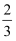等效平衡 知识点题库
如右下图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器。当其它条件相同时,在Ⅰ、Ⅱ中分别加入2 mol X和2 mol Y,开始时容器的体积均为V L,发生如下反应并达到平衡状态: 2X(?)+Y(?)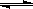 aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断正确的是( )
aZ(g)。此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断正确的是( )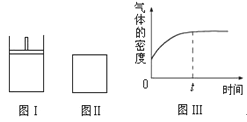
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
试回答下列问题
-
(1) 上述正向反应是反应 (填“放热”或“吸热”)
-
(2) 要使上述反应的逆反应速率增大且平衡正反应方向移动,下列措施不可行的有( )A . 加入催化剂 B . 增大CO的物质的量以提高体系的压强 C . 降低温度 D . 减小H2的浓度
-
(3) 向某密闭容器中充入2molCO和4molH2O(g),发生反应:CO(g)+H2O(g)⇌H2(g)+CO2(g),当反应达平衡时,CO的体积分数为X,若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数不等于X的有( )A . 1molCO(g)+4molH2O+2molCO2(g)+2molH2(g) B . 2molCO(g)+2molH2O+2molCO2(g)+2molH2(g) C . 1molCO(g)+3molH2O+0.8molCO2(g)+0.8molH2(g) D . 1molCO(g)+3molH2O+1molCO2(g)+1molH2(g)
-
(4) 若反应在800℃时进行,设起始CO和H2O(g)共为5mol,水蒸气的体积分数为X;平衡时CO的转化率为y,则y随x变化的函数关系式为y=
-
(5) 在VL密闭容器中通入10mol CO和10mol水蒸气,在T℃达到平衡,然后急速通过碱石灰,将所得混合气体燃烧,测得放出的热量为2845KJ(已知CO燃烧热为283KJ/mol,H2燃烧热为286KJ/mol),则T℃平衡常数K= , T= K
(0℃时T=273K)
选项 | 起始状态/mol | ||
N2 | H2 | NH3 | |
A | 2 | 0 | 2 |
B | 2.5 | 1.5 | 1 |
C | | 2 | |
D | 0 | 0 | 2 |
 2SO3(g) ΔH= −197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2和1 mol O2;(乙)1 mol SO2和0.5 mol O2;(丙)2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是( )
2SO3(g) ΔH= −197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲)2 mol SO2和1 mol O2;(乙)1 mol SO2和0.5 mol O2;(丙)2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是( )
-
(1) CO可用于炼铁,
已知:Fe2O3(s)+ 3C(s)=2Fe(s)+ 3CO(g) ΔH 1=+489.0 kJ·mol-1
C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为。
-
(2) 分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液)。写出该电池的负极反应式:。
-
(3) CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如图。①曲线I、Ⅱ对应的平衡常数大小关系为KⅠKⅡ(填“>”或“=”或“<”)。
CH3OH(g)+H2O(g),测得CH3OH的物质的量随时间的变化如图。①曲线I、Ⅱ对应的平衡常数大小关系为KⅠKⅡ(填“>”或“=”或“<”)。 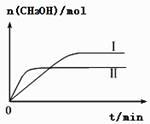
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
容 器
甲
乙
反应物投入量
1molCO2、3molH2
a molCO2、b molH2、
c molCH3OH(g)、c molH2O(g)
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为。
③一定温度下,此反应在恒压容器中进行,能判断该反应达到化学平衡状态的依据是。
a.容器中压强不变 b.H2的体积分数不变 c.c(H2)=3c(CH3OH) d.容器中密度不变 e.2个C=O断裂的同时有3个H-H断裂
-
(4) 将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g) + 6H2(g)
 CH3OCH3(g) + 3H2O(g)。已知一定条件下,该反应中CO2的平衡转化率随温度、投料比[n(H2) / n(CO2)]的变化曲线如下图。若温度升高,则反应的平衡常数K将(填“增大”、“减小”或“不变”。下同);若温度不变,提高投料比n(H2)/n(CO2),则K将;该反应△H0(填“>”、“<”或“=”)。
CH3OCH3(g) + 3H2O(g)。已知一定条件下,该反应中CO2的平衡转化率随温度、投料比[n(H2) / n(CO2)]的变化曲线如下图。若温度升高,则反应的平衡常数K将(填“增大”、“减小”或“不变”。下同);若温度不变,提高投料比n(H2)/n(CO2),则K将;该反应△H0(填“>”、“<”或“=”)。 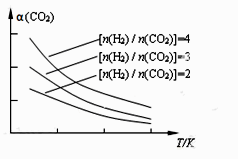
 PCl5(g) 达到平衡后,PCl5为0.8 mol,如果此时移走2.0mol PCl3和1.0mol Cl2 , 相同温度下再达到平衡时PCl5的物质的量是( )
PCl5(g) 达到平衡后,PCl5为0.8 mol,如果此时移走2.0mol PCl3和1.0mol Cl2 , 相同温度下再达到平衡时PCl5的物质的量是( )
 2C(g)+2D(g) ΔH=Q,2 min末达到平衡,生成0.8 mol D。
2C(g)+2D(g) ΔH=Q,2 min末达到平衡,生成0.8 mol D。
-
(1) 300 ℃时,该反应的平衡常数表达式为:K=。已知K300 ℃<K350 ℃ , 则ΔH0(填“>”或“<”)。
-
(2) 在2 min末时,B的平衡浓度为,D的平均反应速率为。
-
(3) 若温度不变,缩小容器容积,则A的转化率(填“增大”“减小”或“不变”),原因是。
-
(4) 如果在相同的条件下,上述反应从逆反应方向进行,开始时加入C、D各4/3mol。若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入Bmol。
 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( ) 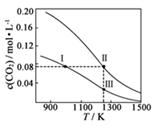
 2CO(g)的ΔS>0、ΔH<0
B . 体系的总压强p总:p总(状态Ⅱ)<2p总(状态Ⅰ)
C . 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D . 逆反应速率:v逆(状态Ⅰ)>v逆(状态Ⅲ )
2CO(g)的ΔS>0、ΔH<0
B . 体系的总压强p总:p总(状态Ⅱ)<2p总(状态Ⅰ)
C . 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D . 逆反应速率:v逆(状态Ⅰ)>v逆(状态Ⅲ )
 3C(g)+D(g),平衡时C的浓度为amol·L-1。若维持容器体积和温度不变,按下列4种方法配比作为起始物质充入该容器中,达到平衡后,C的浓度仍为amol·L-1的是( )
3C(g)+D(g),平衡时C的浓度为amol·L-1。若维持容器体积和温度不变,按下列4种方法配比作为起始物质充入该容器中,达到平衡后,C的浓度仍为amol·L-1的是( )
 2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
2SO3(g)。经过一段时间后达到平衡。反应过程中测定的部分数据见下表: | t/s | 0 | 2 | 4 | 6 | 8 |
| n(SO3)/mol | 0 | 0.8 | 1.4 | 1.8 | 1.8 |
下列说法正确的是( )
 xC(g),平衡后,C的体积分数为w%,若维持容器容积和温度不变,0.6 mol A、0.3 mol B和1.4 mol C为起始物质,达到平衡后,C的体积分数也为w%。平衡后若缩小容器体积,C的浓度c(C)、C的体积分数C%、混合气体平均相对分子质量(
xC(g),平衡后,C的体积分数为w%,若维持容器容积和温度不变,0.6 mol A、0.3 mol B和1.4 mol C为起始物质,达到平衡后,C的体积分数也为w%。平衡后若缩小容器体积,C的浓度c(C)、C的体积分数C%、混合气体平均相对分子质量(  B .
B . 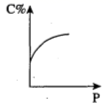 C .
C . 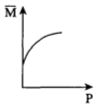 D .
D . 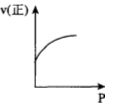
 ,其他条件不变,缩小反应容器体积,正逆反应速率不变
B .
,其他条件不变,缩小反应容器体积,正逆反应速率不变
B .  ,碳的质量不再改变说明反应已达平衡
C . 若压强不再随时间变化能说明反应
,碳的质量不再改变说明反应已达平衡
C . 若压强不再随时间变化能说明反应 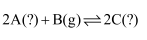 已达平衡,则A、C不能同时是气体
D .
已达平衡,则A、C不能同时是气体
D . 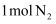 和
和 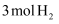 反应达到平衡时
反应达到平衡时  转化率为
转化率为 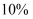 ,放出的热量为
,放出的热量为 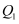 ;在相同温度和压强下,当
;在相同温度和压强下,当 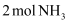 分解为
分解为  和
和  的转化率为
的转化率为 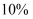 时,吸收的热量为
时,吸收的热量为  ,
,  不等于
不等于 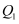
 2HI(g),温度为T时,在两个体积均为1 L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w (HI)与反应时间t的关系如下表:
2HI(g),温度为T时,在两个体积均为1 L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w (HI)与反应时间t的关系如下表: | 容器编号 | 起始物质 | t/min | 0 | 20 | 40 | 60 | 80 | 100 |
| I | 0.5 mol I2、0.5 mol H2 | w (HI)/% | 0 | 50 | 68 | 76 | 80 | 80 |
| II | x mol HI | w (HI)/% | 100 | 91 | 84 | 81 | 80 | 80 |
研究发现上述反应中:v正=ka·w(H2)·w(I2),v逆=kb·w2(HI),其中ka、kb为常数。下列说法正确的是:( )
 B . 容器I中在前20 min的平均速率v(HI)=0.0125 mol·L-1·min-1
C . 若起始时向容器I中加入物质的量均为0.1 mol的H2、I2、HI,反应逆向进行
D . 若两容器中存在kaⅠ= kaⅡ且kbⅠ= kbⅡ , 则x的值可以为任何值
B . 容器I中在前20 min的平均速率v(HI)=0.0125 mol·L-1·min-1
C . 若起始时向容器I中加入物质的量均为0.1 mol的H2、I2、HI,反应逆向进行
D . 若两容器中存在kaⅠ= kaⅡ且kbⅠ= kbⅡ , 则x的值可以为任何值
-
(1) Ⅰ.恒温、恒压下,在一个可变容积的容器中发生如下反应:A(g)+B(g)
 C(g)
C(g) 若开始时放入1molA和1molB,到达平衡后,生成amolC,这时A的物质的量为mol。
-
(2) 若开始时放入3molA和3 molB,到达平衡后,生成C的物质的量为mol。
-
(3) 若开始时放入xmolA、2 molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3amol,则x =mol,y =mol。平衡时,B的物质的量可能大于,等于或小于2mol,作出判断的理由是。
-
(4) 若在(3)的平衡混合物中再加入3molC,待再次达到平衡后,C的物质的量分数是
-
(5) Ⅱ.若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应。
开始时放入1molA和1molB到达平衡后生成bmolC.将b与(1)小题中的a进行比较(选填一个编号)。
(甲)a<b (乙)a>b (丙)a=b (丁)不能比较a和b的大小
作出此判断的理由是。
- ________,hisbookishness,curiously little is known about the
- —Can you speed it up a little? I’ll be late for myflight.—
- 中国古代文献记载了丰富的化学知识。 (1)黑火药是我国的“四大发明”之一,爆炸时发生的主要反应如下,请完成配平(在方框内
- 我们不能随地吐痰是因为痰中含有大量的病菌。痰生成的部位是( ) A.鼻腔黏膜 B
- Not only the students but alsothe teacher ___ enjoying the
- 函数 的大致图象是( )。A. B. C.
- 如图,直线a∥b,直线c与直线a、b分别相交于A、B两点,若∠1=60°则∠2= .
- 下列说法中能表明国家的根本属性的是①国家是阶级矛盾不可调和的产物和表现 ②国家是一个阶级对另一个阶级专政的机器 ③国家
- ---So what do you usually do in your free time?----At _____
- 某校相邻的两个班级,在对待开窗通风、清理垃圾问题上的态度截然相反。甲班全班同学同心协力,积极开窗通风,清理垃圾;乙班的部
- 对我们青年学生的指导意义有( ) (1)矛盾是普遍存在的,因而要正视而不能躲避矛盾 (2)我们要懂得福与祸是对立
- Shenzhou VI , ______ on Oct, 12, 2005, has greatly inspired
- 如图所示的四种现象中,由于光的折射形成的是:
- It’s too noisy here. Please ask him to ____the radio a littl
- 2008年南方雪灾给我国造成了巨大的损失,引起了社会各界的关注。雪灾中电线结起冰柱现象的成因是 A.由水蒸气液化而成
- 下列句子中没有错别字的一项是 A.雨气空而迷幻,细细嗅嗅,有一点点薄荷的香味,浓的时候,竟发出草和树林之后特有的淡淡土腥
- 图中图一表示的是八月份某一晴天,一昼夜中棉花植株CO2的吸收和释放曲线;图二表示棉花叶肉细胞两种细胞器的四种生理活动状
- 第三节.完形填空(共20小题;每小题1.5分,满分30分) 阅读下面的短文,掌握其大意,然后从21--40各题所给的
- “低碳生活”倡导我们在生活中所耗用的能量、材料要尽量减少,从而减低二氧化碳的排放量,下列做法不符合“低碳生活”理念的是
- 镁是海水中含量较多的金属,镁、镁合金及其镁的化合物在科学研究和工业生产中用途非常广泛。 (1)Mg2Ni是一种储氢合金,