等效平衡 知识点题库
一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)⇌3C(g),若反应开始时充入2mol A和2mol B,达平衡后A的体积分数为a%.其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是( )
A . 2mol C
B . 2mol A、1mol B和1mol He(不参加反应)
C . 1mol B和1mol C
D . 2mol A、3mol B和3mol C
如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:
N2(g)+3H2(g)⇌2NH3(g)△H=﹣192kJ•mol﹣1 . 向 M、N 中,都通入 xmol N2 和ymol H2的混合气体,初始M、N容积相同,保持温度不变.下列说法正确的是( )
![]()
A . 若x:y=1;2,则平衡时,M中的转化率:N2>H2
B . 若x:y=1:3,当M中放出热量172.8kJ时,N2的转化率为90%
C . 若x=1,y=3,则达到平衡时反应物的转化率N>M
D . 平衡时N2气体在两容器中体积分数可能相等
某温度下在密闭容器中发生如下反应:2M(g)+N(g)⇌2E(g)若开始时只充入2molE(g),达平衡时,混合气体的压强比起始时增大了20%;若开始时只充入2molM和1molN的混合气体,达平衡时M的转化率为( )
A . 20%
B . 40%
C . 60%
D . 80%
某体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:A+3B  2C若维持温度和压强不变,当达到平衡时,容器的体积为V升,其中C气体的体积占10%,下列推断正确的是( )
2C若维持温度和压强不变,当达到平衡时,容器的体积为V升,其中C气体的体积占10%,下列推断正确的是( )
①原混和气体的体积为1.2V升;
②原混和气体的体积为1.1V升;
③反应达平衡时气体A消耗掉0.05V升;
④反应达平衡时气体B消耗掉0.05V升.
A . ②③
B . ②④
C . ①③
D . ①④
已知:H2(g)+I2(g)  2HI(g)△H<0。相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。下列说法错误的是( )
2HI(g)△H<0。相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。下列说法错误的是( )
 2HI(g)△H<0。相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。下列说法错误的是( )
2HI(g)△H<0。相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。下列说法错误的是( )
A . 反应放出的热量一定相同
B . 此时体系的压强一定相同
C . 反应物的转化率可能相同
D . 此时HI的浓度一定相同
在一定温度下,将气体X和气体Y各0.16 mol充入10 L恒容密闭容器中,发生反应:X (g) +Y (g)  2Z (g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
2Z (g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
 2Z (g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:
2Z (g) △H<0。一段时间后达到平衡,反应过程中测定的数据如下表:t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
A . 反应前2 min的平均速率v(Z) =2.0×10=3mol.L-1·min-1
B . 其他条件不变,降低温度,反应达到新平衡前:v(逆)>v(正)
C . 保持其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 moI气体Y,到达平衡时,C (Z) =0.24 mol·L-1
D . 该温度下此反应的平衡常数:K=1. 44
向一体积为2 L 的恒温恒容密闭容器中充入一定量的H2 和N2 , 发生反应:N2(g)+ 3H2(g)  2NH3(g) △H=a kJ•mol-1。体系中气体的物质的量随时间的变化如图所示。
2NH3(g) △H=a kJ•mol-1。体系中气体的物质的量随时间的变化如图所示。
 2NH3(g) △H=a kJ•mol-1。体系中气体的物质的量随时间的变化如图所示。
2NH3(g) △H=a kJ•mol-1。体系中气体的物质的量随时间的变化如图所示。 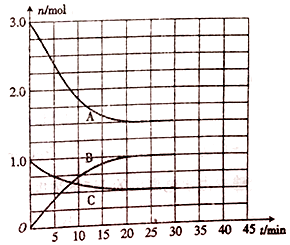
-
(1) 表示N2浓度变化的曲线是 (填“A”“ B”或“C”),25 min 时,c(NH3)= 。
-
(2) 0~20 min 内,v(H2)= 。若该过程中反应放出的热量为47.2 kJ,则a=。
-
(3) 30 min 时,向容器中再充入一定量的NH3 , 一段时间后,与原化学平衡状态时的反应速率相比,正反应速率(填“增大”“ 减小”或“不变”,下同),逆反应速率。
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下。[已知N2(g)+3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol-1]
2NH3(g) ΔH=-92.4 kJ·mol-1]
 2NH3(g) ΔH=-92.4 kJ·mol-1]
2NH3(g) ΔH=-92.4 kJ·mol-1]容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1 mol N2、3 mol H2 | 2 mol NH3 | 4 mol NH3 |
NH3的浓度(mol·L-1) | c1 | c2 | c3 |
反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
体系压强(Pa) | p1 | p2 | p3 |
反应物转化率 | α1 | α2 | α3 |
下列说法正确的是( )
A . 2c1>c3
B . α1+α3=1
C . 2 p2 <p3
D . a+b=92.4
在盛有足量A的体积可变的密闭容器中,加入B,发生反应:A(s)+2B(g)  4C(g)+D(g) ΔH<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是( )
4C(g)+D(g) ΔH<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是( )
 4C(g)+D(g) ΔH<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是( )
4C(g)+D(g) ΔH<0。在一定温度、压强下达到平衡。平衡时C的物质的量与加入B的物质的量的变化关系如图所示。下列说法正确的是( ) 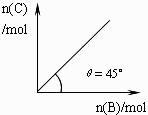
A . 若保持压强一定,当温度升高后,则图中θ>45
B . 若再加入B,则再次达到平衡时正、逆反应速率均逐渐增大
C . 若保持压强一定,再加入B,则反应体系气体密度减小
D . 平衡时B的转化率为50%
一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g)  3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是( )
3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是( )
 3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是( )
3C(g),若反应开始时充入2 mol A和2 mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数大于a%的是( )
A . 2.5mol C
B . 2 mol A、 2 mol B和10 mol He(不参加反应)
C . 1.5 mol B和1.5 mol C
D . 2molA、3 mol B和3 mol C
已知2A(g)+B(g)  2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
 2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
-
(1) 比较ab(填“>”“=”或“<”)。
-
(2) 下表为不同温度下该反应的平衡常数。由此可推知,表中T1T2(填“>” “=”或“<”)。
T/K
T1
T2
T3
K
1.00×107
2.45×105
1.88×103
若在原来的容器中,只加入2molC,500℃时充分反应达平衡后,吸收热量为c kJ,C的浓度(填“>”、“=”或“<”)ωmol/L,a、b、c之间满足何种关系(用代数式表示)。
-
(3) 在相同条件下要想得到2a kJ热量,加入各物质的物质的量可能是_____。A . 4molA和2molB B . 4molA、2molB和2molC C . 4molA和4molB D . 6molA和4molB
-
(4) 为使该反应的反应速率增大,且平衡向正反应方向移动的是____。A . 及时分离出C气体 B . 适当升高温度 C . 增大B的浓度 D . 选择高效催化剂
-
(5) 若将上述容器改为恒压容器(反应前体积相同),起始时加入2molA和1molB,500℃时充分反应达平衡后,放出热量为d kJ,则db(填“>”“=”或“<”),理由是。
-
(6) 在一定温度下,向一个容积可变的容器中,加入3molA和2molB及固体催化剂,使之反应:2A(g)+B(g)
 2C(g),平衡时容器内气体物质的量为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4molA、3molB和2molC,则平衡时A的百分含量(填“不变”“变大”“变小”或“无法确定”)。
2C(g),平衡时容器内气体物质的量为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4molA、3molB和2molC,则平衡时A的百分含量(填“不变”“变大”“变小”或“无法确定”)。
一定温度下,将 2mol NO2 装入 5 L 带活塞的密闭容器中,当反应 2NO2(g)⇋ N2O4(g)ΔH=-60 kJ/mol 达到平衡时,恢复到原来的温度,测得此过程中体系向外界共释放了 40 kJ 的热量。 下列说法正确的是( )
A . 温度升高,平衡常数 K 增大
B . 慢慢压缩气体体积,平衡向右移动,混合气体颜色变浅
C . 上述反应达到平衡时,NO2的转化率是 40%
D . 若起始时向容器中充入 1.0 mol N2O4 , 保持温度不变,达到平衡时共吸收 20 kJ的热量
在某温度时,密闭容器中进行反应:X(g)+4Y(g)  2Z(g)+3R(g),其中X、Y、Z、R的起始浓度依次为0.1、0.4、0.2、0.3(单位均为mol·L-1 , 下同),则达平衡时,各物质的浓度不可能的是( )
2Z(g)+3R(g),其中X、Y、Z、R的起始浓度依次为0.1、0.4、0.2、0.3(单位均为mol·L-1 , 下同),则达平衡时,各物质的浓度不可能的是( )
 2Z(g)+3R(g),其中X、Y、Z、R的起始浓度依次为0.1、0.4、0.2、0.3(单位均为mol·L-1 , 下同),则达平衡时,各物质的浓度不可能的是( )
2Z(g)+3R(g),其中X、Y、Z、R的起始浓度依次为0.1、0.4、0.2、0.3(单位均为mol·L-1 , 下同),则达平衡时,各物质的浓度不可能的是( )
A . c(X)=0.15
B . c(Z)=0.3
C . c(Y)=0.9
D . c(R)=0.6
在一个1L的密闭容器中加2molA和1molB发生反应: 2A(g)+B(g)  3C(g)+D(s),达到平衡时C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L,C的体积分数仍为a% 的是( )
3C(g)+D(s),达到平衡时C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L,C的体积分数仍为a% 的是( )
 3C(g)+D(s),达到平衡时C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L,C的体积分数仍为a% 的是( )
3C(g)+D(s),达到平衡时C的浓度为1.2mol/L , C的体积分数为a% 。维持容器的体积和温度不变,按下列配比作为起始物质,达到平衡后,C的浓度仍是1.2mol/L,C的体积分数仍为a% 的是( )
A . 6mol C+2mol D
B . 4mol A+2mol B
C . 1mol A+0.5mol B+1.5mol C
D . 3mol C+5mol D
在恒压、SO2和O2的起始浓度一定的条件下,测得不同温度下SO2的平衡转化率如图所示。下列说法正确的是( )
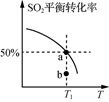
A . 若图中a点使用了催化剂,则b点没有使用催化剂
B . 反应2SO2(g)+O2(g)  2SO3(g)的ΔH<0
C . 若将起始n(SO2)和n(O2)变为原来的一半,图象发生改变
D . T1℃下,c起始(O2)=2.0×10-2 mol·L-1 , 则平衡常数K>50
2SO3(g)的ΔH<0
C . 若将起始n(SO2)和n(O2)变为原来的一半,图象发生改变
D . T1℃下,c起始(O2)=2.0×10-2 mol·L-1 , 则平衡常数K>50
 2SO3(g)的ΔH<0
C . 若将起始n(SO2)和n(O2)变为原来的一半,图象发生改变
D . T1℃下,c起始(O2)=2.0×10-2 mol·L-1 , 则平衡常数K>50
2SO3(g)的ΔH<0
C . 若将起始n(SO2)和n(O2)变为原来的一半,图象发生改变
D . T1℃下,c起始(O2)=2.0×10-2 mol·L-1 , 则平衡常数K>50
一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:2CH3OH(g)  CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g) | 容器 编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| I | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
下列说法正确的是( )
A . 该反应的正方应为吸热反应
B . 达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小
C . 容器I中反应达到平衡所需时间比容器Ⅲ中的长
D . 若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行
一定压强下,向10 L密闭容器中充入1molS2Cl2(g)和1 molCl2 , 发生反应:S2Cl2(g)+Cl2(g)⇌2SCl2(g)。Cl2与SCl2的消耗速率(v)与温度(T)的关系如图所示,以下说法中错误的是( )
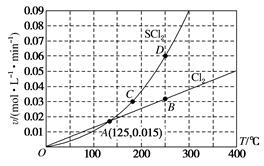
A . A,B,C,D四点对应状态下,达到平衡状态的是B,D
B . 正反应的活化能大于逆反应的活化能
C . 达到平衡后再加热,平衡向逆反应方向移动
D . 在300℃下,达到平衡后缩小容器容积,重新达到平衡后,Cl2的平衡转化率不变
在一固定容积的密闭容器中,一定量的NO和足量碳发生反应:C(s)+2NO(g)  CO2(g)+N2(g),平衡时c(NO)与温度T的关系如图所示。下列说法正确的是( )
CO2(g)+N2(g),平衡时c(NO)与温度T的关系如图所示。下列说法正确的是( )
 CO2(g)+N2(g),平衡时c(NO)与温度T的关系如图所示。下列说法正确的是( )
CO2(g)+N2(g),平衡时c(NO)与温度T的关系如图所示。下列说法正确的是( ) 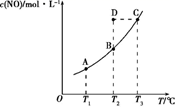
A . 在T2时,N2的浓度c(D)>c(B)
B . 增大NO的物质的量,可以提高NO的平衡转化率
C . 若状态A,B,C时反应速率分别为vA、vB、vC , 则vA>vB>vC
D . 当容器内混合气体密度不变时,反应处于平衡状态
工业上以CO和H2为原料合成甲醇的反应:  ,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇,如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是( )
,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇,如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是( )
 ,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇,如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是( )
,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇,如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是( ) 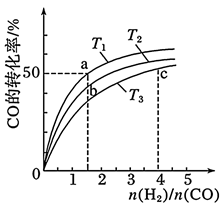
A . H2转化率:c>a>b
B . 上述三种温度之间关系为T1>T2>T3
C . a点状态下再通入 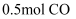 和
和 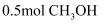 平衡向正方向移动
D . c点状态下再通入
平衡向正方向移动
D . c点状态下再通入 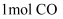 和
和 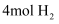 ,新平衡中
,新平衡中  的体积分数增大
的体积分数增大
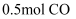 和
和 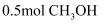 平衡向正方向移动
D . c点状态下再通入
平衡向正方向移动
D . c点状态下再通入 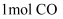 和
和 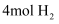 ,新平衡中
,新平衡中  的体积分数增大
的体积分数增大
在相同温度下,体积均为1L的四个密闭容器中,保持温度和容积不变,以四种不同的投料方式进行反应。平衡时有关数据如下(已知2SO2(g)+O2(g)  2SO3(g) ΔH=-196.6kJ·mol-1)。
2SO3(g) ΔH=-196.6kJ·mol-1)。
| 容器 | 甲 | 乙 | 丙 | 丁 |
| 起始投料量 | 2molSO2+1molO2 | 1molSO2+0.5molO2 | 2molSO3 | 2molSO2+2molO2 |
| 反应放出或吸收的热量(kJ) | a | b | c | d |
| 平衡时c(SO3)(mol·L-1) | e | f | g | h |
下列关系正确的是( )
A . a=c;e=g
B . a>2b;e>2f
C . a>d;e>h
D . c+98.3e>196.6
最近更新
- 阅读下列材料,回答以下问题。(11分) 材料一 目前农业部在北方13个省份重点推广保护性耕作法。即对耕地实行免耕或浅耕措
- 下列各组物质互为同分异构体的是 A.O2和O3 B.CH3CH2CH2CH3和CH(CH3)3 C.
- —Jane, have you finished your’paper? —No,I my sister
- 点P( —a2—1,)关于原点的对称点在第_____象限。( )A.一B.二C.三D.四
- 根据右图溶解度曲线,判断下列说法正确的是 A.t1℃时,甲的溶解度大于乙 B.t2℃时,甲、乙两溶液的溶质质量分数一定相
- 下列命题中,是真命题的是 A.同位角相等. B.邻补角一定互补. C.相等的角是对顶角. D.有且只有一条直线与已知直线
- 阅读下列材料:(15分)材料一 材料二:世祖皇帝建元中统以来,始末取故老诸儒之言,考求前代之前典,立朝廷而建官府,辅相者
- 在气温为0℃的室内,把盛有冰和水的金属盒漂浮在盛有酒精溶液的开口容器里,过一段时间后,金属盒内冰和水的变化情况是(
- 一次函数y=﹣2x+1的图象不经过下列哪个象限() A. 第一象限 B.第二象限 C.第三象限
- 一工厂生产了某种产品16 800件,它们来自甲、乙、丙3条生产线,为检查这批产品的质量,决定采用分层抽样的方法进行抽样.
- 1912年,世界第一艘超级豪华游轮――“泰坦尼克”号在大西洋沉没。由于该船运用了当时最先进的通讯方式,一千多名乘客中有6
- During both World War I and II, pigeons were e by
- 阅读《例外的惭愧》,完成第17-20题。(共12分) 例外的惭愧 张晓风 ①有一件事,我十分惭愧,那就是:我经常
- 26.如图12甲所示电路,电源电压为12V,电阻R1的阻值为20Ω,滑动变阻器R2的最大阻值为100Ω,当开关S闭合时,
- ----Jack hasn’t got a job yet, has he? ---- Oh yes, in fa
- 各种细胞器在细胞代谢中起重要的作用,下列有关说法不合理的是 () A.内质网与蛋白质、脂质和核糖核酸
- 如图,线段,所在直线是异面直线,,,,分别是线段,,,的中点. 求证:共面且面,面; 设,分别是和上任意一点,求证:被平
- 下列四种有机化合物的结构简式如下所示,均含有多个官能团,下列有关说法中正确的是()A.①属于酚类,可与NaHCO3溶液反
- 音像店的老板养了一只狗,天天听着腾格尔的《天堂》这首歌,渐渐地狗也会“唱”这首歌了,只要音乐响起就会仰起头,跟着节律高声
- 夏天从冰箱中取出的鸡蛋,常看到鸡蛋先湿后干的现象,此现象反映的物态变化过程正确的是()A. 先液化后蒸发 B. 先升华后



