等效平衡 知识点
等效平衡 知识点题库
时间/min | CO(g) | H2O(g) | CO2(g) | H2(g) |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c4 |
4 | c1 | c2 | c3 | c4 |
-
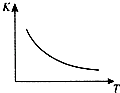
(1) Q0(填“>”、“=”或“<”).
-
(2) 若在850℃时向反应容器中充人H2O(g),K值(填“增大”、“减小”或“不变”).
-
(3) 上表中 c2为 mol/L,CO(g)的转化率为.
-
(1) I若开始时放入1molA和1molB,到达平衡后,生成amolC,这时A的物质的量为mol.
-
(2) 若开始时放入xmolA、2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3amol,则x=mol,y=mol.
-
(3) 若在(2)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是.
-
(4) II 若维持温度不变,在一个与(1)反应前起始体积相同、且容积固定的容器中发生上述反应.
开始时放入1molA和1molB到达平衡后生成bmolC.将b与(1)小题中的a进行比较(选填一个编号)
(甲)a<b (乙)a>b
(丙)a=b (丁)不能比较a和b的大小.
 2HI(g) ΔH<0。实验测得:v正=v(H2)消耗=v(I2)消耗=k正c(H2)·c(I2),v逆=v(HI)消耗=k逆c2 (HI),k正、k逆为速率常数,受温度影响。下列说法正确的是( )
2HI(g) ΔH<0。实验测得:v正=v(H2)消耗=v(I2)消耗=k正c(H2)·c(I2),v逆=v(HI)消耗=k逆c2 (HI),k正、k逆为速率常数,受温度影响。下列说法正确的是( )容器 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度 | ||
c(H2) | c(I2) | c(HI) | ||
Ⅰ(恒容) | 0.1 | 0.1 | 0 | c(I2)=0.07 mol·L-1 |
Ⅱ(恒压) | 0 | 0 | 0.6 | |
 成立
D . 达平衡时,向容器Ⅰ中同时再通入0.1 mol I2和0.1 mol HI,则此时ν正>ν逆
成立
D . 达平衡时,向容器Ⅰ中同时再通入0.1 mol I2和0.1 mol HI,则此时ν正>ν逆
-
(1) Ⅰ.在一固定容积的密闭容器中,保持一定温度,在一定条件下进行如下反应: A(g)+2B(g)
 3C(g),已知起始时加入 3 mol A(g)和 2 mol B(g),达平衡后,生成 a mol C(g)。
3C(g),已知起始时加入 3 mol A(g)和 2 mol B(g),达平衡后,生成 a mol C(g)。 相同实验条件下,若在同一容器中改为开始加入 1.5 mol A 和 1 mol B,达平衡时 C 的 物质的量为mol(用含字母 a 的代数式表示),此时 C 在反应混合物中的体积分数 (填“增大”、“减小”或“不变”)。
-
(2) 相同实验条件下,若在同一容器中改为开始时加入 2 mol A 和 1 mol B,达平衡时,要 求 C 在混合物中体积分数与(1)相同,则开始时还需加入mol C。
-
(3) Ⅱ.向 BaSO4 中加入饱和 Na2CO3溶液,当溶液中 c(CO32-)=6 mol/L 时,有部分BaSO4转化成了 BaCO3 , 则此时 c(SO42-)=。(已知 Ksp(BaCO3)=2.6×10-9 , Ksp=(BaSO4)1.1×10-10)
-
(4) Ⅲ.25℃时,V1 L pH=2 的 HCl 和 V2 L pH=11 的 NaOH 溶液反应后 pH=9,则 V1∶V2= 。
 SO3(g)+NO(g)。投入NO2和SO2 , 起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列说法正确的是( )
SO3(g)+NO(g)。投入NO2和SO2 , 起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列说法正确的是( ) | 起始浓度 | 甲 | 乙 | 丙 |
| c(NO2)/(mol·L-1) | 0.10 | 0.20 | 0.20 |
| c(SO2)/(mol·L-1) | 0.10 | 0.10 | 0.20 |
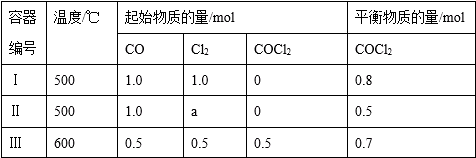
下列说法中正确的是( )
 2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。
2C(g),△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2molA和1molB,在500℃时充分反应达平衡后C的浓度为ωmol/L,放出热量为b kJ。-
(1) 比较ab(填“>”“=”或“<”)。
-
(2) 下表为不同温度下该反应的平衡常数。由此可推知,表中T1T2(填“>” “=”或“<”)。
T/K
T1
T2
T3
K
1.00×107
2.45×105
1.88×103
若在原来的容器中,只加入2molC,500℃时充分反应达平衡后,吸收热量为c kJ,C的浓度(填“>”、“=”或“<”)ωmol/L,a、b、c之间满足何种关系(用代数式表示)。
-
(3) 在相同条件下要想得到2a kJ热量,加入各物质的物质的量可能是 。A . 4molA和2molB B . 4molA,2molB和2molC C . 4molA和4molB D . 6molA和4molB
-
(4) 为使该反应的反应速率增大,且平衡向正反应方向移动的是 。A . 及时分离出C气体 B . 适当升高温度 C . 增大B的浓度 D . 选择高效催化剂
-
(5) 若将上述容器改为恒压容器(反应前体积相同),起始时加入2molA和1molB,500℃时充分反应达平衡后,放出热量为d kJ,则db(填“>”“=”或“<”),理由是。
-
(6) 在一定温度下,向一个容积可变的容器中,通入3molA和2molB及固体催化剂,使之反应:2A(g)+B(g)
 2C(g) 平衡时容器内气体物质的量为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4molA、3molB和2molC,则平衡时A的百分含量(填“不变”“变大”“变小”或“无法确定”)。
2C(g) 平衡时容器内气体物质的量为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4molA、3molB和2molC,则平衡时A的百分含量(填“不变”“变大”“变小”或“无法确定”)。
 2NH3(g)
2NH3(g)  H=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表:
H=-92.6 kJ/mol,实验测得起始、平衡时的有关数据如下表: | 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体 系能量的变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量:23.15 kJ |
| ② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述不正确的是( )
 2E(g)。若开始时只充入2 mol E(g),达到化学平衡时,混合气体的压强比开始时增大了20%;若开始时只充入2 mol M(g)和1 mol N(g) 的混合气体,则达到化学平衡时M的转化率是( )
2E(g)。若开始时只充入2 mol E(g),达到化学平衡时,混合气体的压强比开始时增大了20%;若开始时只充入2 mol M(g)和1 mol N(g) 的混合气体,则达到化学平衡时M的转化率是( )
 N2+3H2 , 达到平衡时,容器内N2的百分含量为a%,若维持容器的体积和温度都不变,分别通入下列几组物质,达到平衡时,容器内N2的含量仍为a%的是( )
N2+3H2 , 达到平衡时,容器内N2的百分含量为a%,若维持容器的体积和温度都不变,分别通入下列几组物质,达到平衡时,容器内N2的含量仍为a%的是( )
-
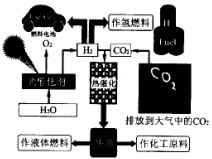
(1) 联系自然界的光合作用原理,并结合上述图示, 写出“人工”光合作用的化学方程式;;在图示转化过程中,太阳能除了储存在甲醇中,还储存在中(填化学式)。
-
(2) 图中热催化过程的反应原理为CO2(g) + 3H2(g) = CH3OH(g) + H2O(g)△H。
已知:2H2(g)+O2(g)=2H2O (g)△H1= -483.6 kJ•mo1-1;
2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g)△H2=-1352.86 kJ•mol-1
△H =。
-
(3) 实验室对热催化反应进行模拟探究:一定温度下,向容积均为2 L 的恒容密闭容器中分别通入1.0 mol CO2(g)和3.0 mol H2(g), 在不同催化剂X、Y 的催化下发生反应。测得5 min时,CO2转化率与温度的变化关系如图所示。
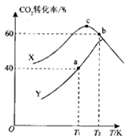
①该反应适宜选用的催化剂为(填“X'”或 “Y”)。
②T1K时,a点对应容器在0~5 min内的平均反应速率v(H2)=;b、c点对应状态下反应物的有效碰撞几率bc(填“>”“<”或“=”),原因为。
③T2K时,若反应前容器内的压强为p, 则该温度下反应的平衡常数KP=。 (KP为用分压表示的平衡常数)。
-
(4) 我国化学家结合实验和计算机模拟结果,研究得出热催化反应的一种可能历程如图所示,其中自由基用“•”标出,过渡态用TS表示。
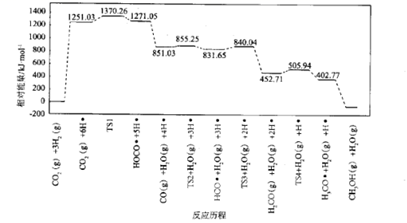
四个过渡态中对反应速率影响最大的是,理由为;该步骤的化学方程式为。
 cC(g)+dD(g) ΔH<0。当反应进行一段时间后,测得A减少了n mol,B减少了0.5n mol,C增加了1.5n mol,D增加了n mol,此时达到化学平衡状态则下列说法正确的是( )
cC(g)+dD(g) ΔH<0。当反应进行一段时间后,测得A减少了n mol,B减少了0.5n mol,C增加了1.5n mol,D增加了n mol,此时达到化学平衡状态则下列说法正确的是( ) 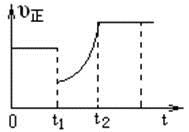
 ,在相同温度和催化剂的条件下,两容器中各自发生下列反应:
,在相同温度和催化剂的条件下,两容器中各自发生下列反应: 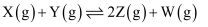
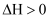 ;达到平衡时,
;达到平衡时, 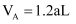 ,则下列说法错误的是( )
,则下列说法错误的是( ) 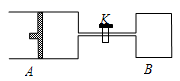
-
(1) 已知25℃、101kPa时,以下反应的热化学方程式为:
4Fe(s)+3O2(g)=2Fe2O3(s) △H1=-1644kJ•mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-564kJ•mol-1
C(s)+O2(g)=CO2(g) △H3=-393kJ•mol-1
则Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)的△H=kJ•mol-1。
-
(2) 已知反应NO(g)+O3(g)
 NO2(g)+O2(g) △H=-200.9kJ•mol-1在低温下自发进行,则该反应的熵变△S0(填“大于”或“小于”)。
NO2(g)+O2(g) △H=-200.9kJ•mol-1在低温下自发进行,则该反应的熵变△S0(填“大于”或“小于”)。
-
(3) Ⅱ.资料显示,在催化剂存在条件下,可分别用CO和CO2作碳源,均能与H2S反应产生羰基硫(COS),COS是一种粮食熏蒸剂,能防治某些害虫和真菌的危害。具体反应如下:
反应1:CO(g)+H2S(g)
 COS(g)+H2(g) △H=-11.3kJ•mol-1
COS(g)+H2(g) △H=-11.3kJ•mol-1反应2:CO2(g)+H2S(g)
 COS(g)+H2O(g)
COS(g)+H2O(g)研究表明,反应1分两步完成,具体过程如下:
①2H2S(g)
 S2(g)+2H2(g) △H1=+168.9kJ•mol-1
S2(g)+2H2(g) △H1=+168.9kJ•mol-1②2CO(g)+S2(g)
 2COS(g) △H2
2COS(g) △H2已知,决定COS生成速率的步骤为第一步,请在图1中画出反应1两步过程的能量变化图(标清每步反应的产物和状态)。

-
(4) 在恒压密闭容器中,投入等物质的量的反应物,分别发生反应1和反应2。图2中,曲线a(实线)表示反应1在不同温度下反应相同时间t时,COS的物质的量分数;曲线b(虛线)表示反应2在不同温度下达到平衡时COS的物质的量分数。根据图中信息回答下列问题:
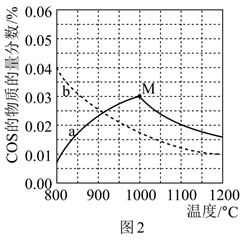
①由图2可知,反应2:CO2(g)+H2S(g)
 COS(g)+H2O(g)的△H0(填“>”或“<”),当温度升高时,反应2的化学平衡常数K(填“增大”、“减小”或“不变”),在a(绝热恒容)、b(恒温恒容)、c(恒温恒压)三个容器中,起始状态和投料等完全相同,如图3所示,反应达到平衡后,H2S的转化率由大到小的顺序为(用a、b、c表达)。
COS(g)+H2O(g)的△H0(填“>”或“<”),当温度升高时,反应2的化学平衡常数K(填“增大”、“减小”或“不变”),在a(绝热恒容)、b(恒温恒容)、c(恒温恒压)三个容器中,起始状态和投料等完全相同,如图3所示,反应达到平衡后,H2S的转化率由大到小的顺序为(用a、b、c表达)。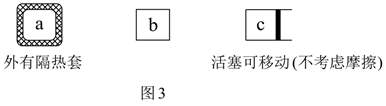
②图2中曲线a上,若M点反应1尚未达到平衡,则后面曲线变化的可能原因是;若M点反应1达到平衡,则请在图2中画出900℃~1100℃之间反应1平衡时COS的物质的量分数随温度的变化曲线。
 和
和
 , 发生反应:
, 发生反应:
 。
。
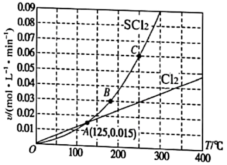
 的消耗速率(v)、
的消耗速率(v)、
 的消耗速率(v)、温度(T)三者的关系如图所示,以下说法中不正确的是( )
的消耗速率(v)、温度(T)三者的关系如图所示,以下说法中不正确的是( )
 和
和
 ,
,
 的平衡转化率不变
D . 125℃,平衡时
的平衡转化率不变
D . 125℃,平衡时
 的消耗速率为0.015
的消耗速率为0.015
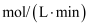
-
(1) I:2SO2(g)+O2(g)
 2SO3(g) ΔH1=-197.7kJ/mol K1(浓度平衡常数)
2SO3(g) ΔH1=-197.7kJ/mol K1(浓度平衡常数)为研究该反应,某同学设计了以下三种已装固体V2O5催化剂的密闭容器装置:

在初始体积与温度相同的条件下,甲、乙、丙中均按2 mol SO2、1molO2进行投料,达平衡时,三个容器中SO2的转化率从大到小的顺序为(用“甲、乙、丙”表示)。
-
(2) 在容器丙中,0.1 MPa条件下,在不同温度或不同投料方式下研究上述反应,得到数据如下表:
实验序号
A组
B组
C组
反应温度
451℃
451℃
551℃
投料方式(按照SO2、O2、SO3的顺序)
2 mol 、1mol、0 mol
0mol 、0mol 、2mol
2mol 、1mol 、0mol
含硫化合物的转化
60%
b
c
反应的热量变化
放热a
吸热79.08kJ
放热
压强平衡常数(Kp)
Kp1
Kp1
Kp2
①表中:a= 。
②已知用平衡分压(分压=总压×物质的量分数)代替平衡浓度计算,得到的平衡常数即为压强平衡常数,则Kp1=MPa-1。
③451℃时,若按0.4 mol SO2、0.4mol O2、0.4 mol SO3进行投料,则反应开始时v正(SO2)v逆(SO2)(填“>”、“<”或“=”)。
-
(3) 将上述固体催化剂V2O5换成NO2气体同样可以对该反应起到催化作用,此催化过程如下:
Ⅱ:SO2(g)+NO2(g)
 SO3(g)+NO(g) △H2 K2(浓度平衡常数)
SO3(g)+NO(g) △H2 K2(浓度平衡常数)Ⅲ:2NO(g)+O2(g)
 2NO2(g) △H3=-114.1 kJ/mol K3(浓度平衡常数),△H2=;K3=(用含有K1、K2的表达式表示)。
2NO2(g) △H3=-114.1 kJ/mol K3(浓度平衡常数),△H2=;K3=(用含有K1、K2的表达式表示)。
- 下列属于文化传播途径的是 ①通过商品交换将商品中蕴涵的丰富文化加以交流 ②通过大规模的人口迁徙来传播文化③通过国家之间的
- X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质 的基础元素,M是地壳中含量最高的金属元素
- 夏天,打开冰箱门,常可看到白雾。这是 ( ) A.空气中的水蒸气降温形成的小水滴 B.冰箱内食物中的水分遇到高温
- 一辆汽车运动的位移时间关系式为,则 A.这个汽车做匀减速运动 B
- “If you want a necklace, I’ll buy one for you at once.” “Oh,
- 材料一:近来中东局势不断恶化,以色列不新暗杀巴勒斯坦激进派领导人, 中东和平路线图计划难以实施,;美国在伊拉克的军队不断
- 某小组以CoCl2·6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X。为确定其组成,进
- 阅读下列材料,回答下列问题: 材料一 在中国近代化探索的历程中,国人相继走过了自救之路、维新之路、共和之路。但都没有完
- (8分)(1)(4分)同温同压下,同体积的甲烷(CH4)和CO2气体的分子数之比为 ;质量比为
- 将氢气、甲烷、乙醇等物质在氧气中燃烧时的化学能直接转化为电能的装置叫燃料电池。燃料电池的基本组成为电极、电解质、燃料和氧
- 若直线(1+a)x+y+1=0与圆x2+y2-2x=0相切,则a的值为() A.1,-1
- 将一张浸湿了溴水的滤纸挂在SO2气体中,滤纸会由黄色变成白色,这主要是因为 A.SO2漂白了滤纸
- 关于国庆60周年大阅兵场景如图所示,下列说法正确的是 A.旗手帽子上的军徽熠熠发光,因为军徽是光源 B.整个队列整齐划一
- 如果分式方程无解,则x的值是( ▲ )A.2B.0C.-1D.-2
- 从发展经济的角度来看,珠江三角洲较特殊的人文优势在于______________,西双版纳发展经济的人文优势在于____
- 用分子的相关知识解释下列生活中的现象,其中错误的是( ) A.非吸烟者受到被动吸烟的危害,是因为分子在不断地运动
- — does your brother go to school?—At 7:00.A. What ti
- 如图为叶绿体亚显微结构图,关于其结构与功能的不正确叙述是()A.①和②均为选择透过性膜 B.光反应的产物有O2、[H]、
- 在快节奏的生活中,市民们无意于追求典雅的意境、浓郁迷离的诗情,而是醉心于能直接地并情调热烈地满足感官享受的艺术样式,在这
- 如图,F1、F2分别是椭圆C:+=1(a>b>0)的左、右焦点,A是椭圆C的顶点,B是直线AF2与椭圆C的另一个交点,∠



