化学反应速率的影响因素 知识点题库
对于反应2SO2(g)+O2(g) 2SO3(g),能增大正反应速率的措施是( )
2SO3(g),能增大正反应速率的措施是( )
A . 通入大量O2
B . 增大容器容积
C . 移去部分SO2
D . 降低体系温度
下列有关研究化学反应原理的叙述中,正确的是( )
A . 研究化学反应中的能量变化,有利于通过改变反应条件,使同一反应消耗相同量的物质而放出更多的热,提高化学能的利用率
B . 任何放热的化学反应,均可以利用原电池直接把化学能转化为电能
C . 研究化学反应速率与化学平衡,有利于指导实际生产中达到“多,快,好,省”的生产效率
D . 使用催化剂常常可以加快化学反应速率,但不能提高反应物的转化率,因此在实际生产中较少使用催化剂
下列有关化学反应速率的描述中正确的是( )
A . 在任何化学反应中,只要提高反应温度,就可提高反应速率
B . 在任何化学反应中,只要增大某一反应物的用量,就会增大反应速率
C . 在任何化学反应中,增大压强时,都会使反应速率增大
D . 在任何化学反应中,只要缩小容器的体积,都会使反应速率增大
用100mL2mol/L稀硫酸与过量铁片反应制取氢气时,下列措施能使氢气的生成的速率增大而产生氢气的量不变的是( )
A . 给反应体系适当加热
B . 向反应体系中加水稀释
C . 加入少量氧化铜固体
D . 加压
下列关于有机化合物的认识不正确的是( )
A . 制取乙炔,为了降低反应速率可用饱和食盐水代替水
B . 除去乙烷中混有的少量乙烯,可用高锰酸钾溶液
C . 甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同
D . 乙烷和甲苯中都含有甲基,甲苯可以被酸性KMnO4溶液氧化成苯甲酸,而乙烷不能被其氧化,说明苯环对侧链产生了影响
下列说法中正确的是( )
A . 增大反应物浓度,能增大活化分子百分数,所以反应速率增大
B . 使用正催化剂,能增大活化分子百分数,所以反应速率增大
C . 对于任何反应,增大压强都可加快反应速率
D . 升高温度,只能增大吸热反应的反应速率
合成氨反应为:N2(g)+3H2(g)  2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。 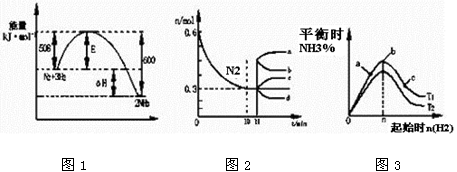
 2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。 
下列说法正确的是( )
A . 该反应为自发反应,由图1可得加入适当的催化剂,E和△H都减小
B . 图2中0~10min内该反应的平均速率v(H2)=0.045mol·L-1·min-1 , 从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为d
C . 图3中a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点
D . 图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2 , 则:T1>T2 , K1>K2
钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图所示。下列说法不正确的是( )
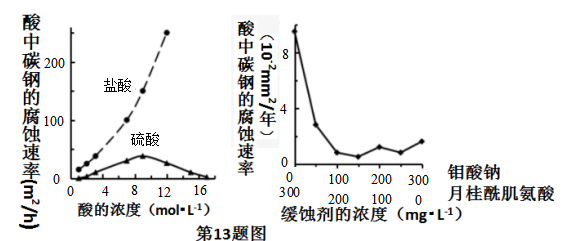
A . 盐酸的浓度越大,腐蚀速率越快
B . 碳素钢的腐蚀速率不随硫酸的浓度增大而增大,说明反应速率不与c(H+)成正比
C . 钼酸钠和月桂酰肌氨酸的浓度相等时,腐蚀速率最小
D . 对比盐酸和硫酸两条曲线,可知Cl-也可能会影响碳素钢的腐蚀速率
设C+CO2  2CO △H>0,反应速率为V1 , N2+3H2
2CO △H>0,反应速率为V1 , N2+3H2  2NH3 △H<0,反应速率为V2 , 当温度升高时,速率变化情况为:( )
2NH3 △H<0,反应速率为V2 , 当温度升高时,速率变化情况为:( )
 2CO △H>0,反应速率为V1 , N2+3H2
2CO △H>0,反应速率为V1 , N2+3H2  2NH3 △H<0,反应速率为V2 , 当温度升高时,速率变化情况为:( )
2NH3 △H<0,反应速率为V2 , 当温度升高时,速率变化情况为:( )
A . V1增大,V2减小
B . V1、V2都增大
C . V1减小,V2增大
D . V1、V2都减小
在容积一定的密闭容器中,进行可逆反应A(g)+2B(g) 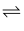 C(g) +D(g),有图Ⅰ、Ⅱ所示的反应曲线,下列说法中错误的是( )
C(g) +D(g),有图Ⅰ、Ⅱ所示的反应曲线,下列说法中错误的是( )
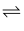 C(g) +D(g),有图Ⅰ、Ⅱ所示的反应曲线,下列说法中错误的是( )
C(g) +D(g),有图Ⅰ、Ⅱ所示的反应曲线,下列说法中错误的是( ) 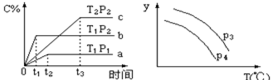
图I 图II
A . 正反应是放热反应
B . P1 <P2
C . 若P3<P4 , y轴表示A的转化率
D . 若P3>P4 , y轴表示C的体积分数
温度为T时,向VL的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g)  C(s)+xD(g) △H>0,容器中A、B、D的物质的量浓度随时间的变化如下图所示。下列说法中不正确的是( )
C(s)+xD(g) △H>0,容器中A、B、D的物质的量浓度随时间的变化如下图所示。下列说法中不正确的是( )
 C(s)+xD(g) △H>0,容器中A、B、D的物质的量浓度随时间的变化如下图所示。下列说法中不正确的是( )
C(s)+xD(g) △H>0,容器中A、B、D的物质的量浓度随时间的变化如下图所示。下列说法中不正确的是( ) 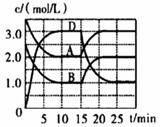
A . 反应在前10min以B物质表示的平均反应速率v(B)=0.15 mol·L-1·min-1
B . 该反应方程式中的x=2
C . 若平衡时保持温度不变,压缩容器容积,平衡向逆反应方向移动
D . 反应至15min时,改变的条件是降低温度
投入一定量的物质A和B发生可逆反应:2A(g)+nB(g)  mC(g) ,在温度分别为T1、T2 , 压强分别为P1、P2的条件下,测得C的物质的量与时间的关系如右图所示, 有关该反应的说法正确是( )
mC(g) ,在温度分别为T1、T2 , 压强分别为P1、P2的条件下,测得C的物质的量与时间的关系如右图所示, 有关该反应的说法正确是( )
 mC(g) ,在温度分别为T1、T2 , 压强分别为P1、P2的条件下,测得C的物质的量与时间的关系如右图所示, 有关该反应的说法正确是( )
mC(g) ,在温度分别为T1、T2 , 压强分别为P1、P2的条件下,测得C的物质的量与时间的关系如右图所示, 有关该反应的说法正确是( ) 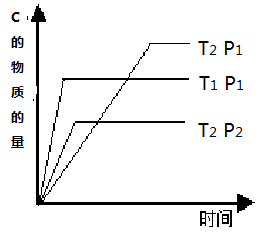
A . n+2<m该反应正反应为放热反应
B . n+2<m该反应正反应为吸热反应
C . n+2>m该反应正反应为放热反应
D . n+2>m该反应正反应为吸热反应
已知:X(s)+2Y(g)⇌3Z(g),正反应放热。下列说法错误的是( )
A . 增加 X 的用量,对反应速率没有影响
B . 升高反应温度,逆反应速率增大,正反应速率减小
C . 达到化学平衡状态时,Z 的浓度不再发生变化
D . 0.1 mol X 和 0.2 mol Y 充分反应生成 Z 的物质的量一定小于 0.3 mol
某化学研究小组探究外界条件对化学反应mA (g)+nB (g)  pC (g)的速率和平衡的影响图象如下,下列判断正确的是( )
pC (g)的速率和平衡的影响图象如下,下列判断正确的是( )
 pC (g)的速率和平衡的影响图象如下,下列判断正确的是( )
pC (g)的速率和平衡的影响图象如下,下列判断正确的是( ) 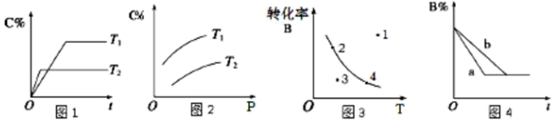
A . 由图1可知,T1<T2 , 该反应正反应为吸热反应
B . 由图2可知,该反应m+n<p
C . 图3中,点3的反应速率v正>v逆
D . 图4中,若m+n=p, 则a曲线一定使用了催化剂
氮气是制备含氮化合物的一种重要物质,而含氮化合物的用途广泛,如图表示两个常见固氮反应的平衡常数对数值(lg K)与温度的关系:①N2+3H2  2NH3 , ②N2+O2
2NH3 , ②N2+O2  2NO。
2NO。
 2NH3 , ②N2+O2
2NH3 , ②N2+O2  2NO。
2NO。 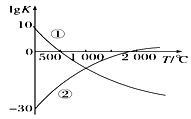
根据图中的数据判断下列说法正确的是( )
A . 反应①和②均为放热反应
B . 升高温度,反应①的反应速率减小
C . 在常温下,利用反应①固氮和利用反应②固氮反应程度相差很大
D . 在1 000 ℃时,反应①和反应②体系中N2的浓度一定相等
为研究碳酸钙与稀盐酸的反应速率,标准状况下测得生成CO2体积随时间变化情况如图所示,下列分析正确的是( )
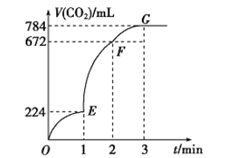
A . FG段的反应速率最快
B . F点收集到CO2的量最多
C . 影响EF段反应速率的主要因素是c(HCl)
D . OE、EF、FG三段中,CO2的生成速率之比为2:4:1
在密闭容器中进行反应CH4(g)+H2O(g)  CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是( )
CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是( )
 CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是( )
CO(g)+3H2(g) ΔH>0,测得c(CH4)随反应时间(t)的变化如图所示。下列判断正确的是( ) 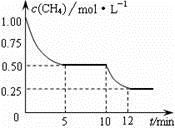
A . 0~5 min内,v(H2)=0.1 mol·(L·min)-1
B . 反应进行到12min时,CH4的转化率为25%
C . 恒温下,缩小容器体积,平衡后H2浓度减小
D . 10 min时,改变的外界条件可能是升高温度
已知:X(g)+2Y(g) 3Z(g) △H=-akJ·mol-1(a>0),下列说法不正确的是( )
3Z(g) △H=-akJ·mol-1(a>0),下列说法不正确的是( )
 3Z(g) △H=-akJ·mol-1(a>0),下列说法不正确的是( )
3Z(g) △H=-akJ·mol-1(a>0),下列说法不正确的是( )
A . 0.1molX和0.2molY充分反应生成Z的物质的量一定小于0.3mol
B . 达到化学平衡状态时,X、Y、Z的浓度不再发生变化
C . 达到化学平衡状态时,反应放出的总热量可达a kJ
D . 升高反应温度,逆反应速率增大,正反应速率减小
常见的氮氧化物有NO、NO2、N2O5等。
-
(1) 在一定条件下,N2与O2反应生成1molNO气体,吸收90kJ的热量。该反应的热化学方程式为。
-
(2) 在800℃,2L密闭容器中,发生反应2NO(g)+O2(g)
 2NO2(g),体系中NO物质的量随时间变化如表:
2NO2(g),体系中NO物质的量随时间变化如表:时间/s
0
1
2
3
4
5
n(NO)/mol
0.020
0.010
0.008
0.007
0.007
0.007
①0~2s,以O2的浓度变化表示该反应的平均速率
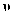 (O2)=mol·L-1·s-1。
(O2)=mol·L-1·s-1。②若要进一步提高该反应的化学反应速率,除了使用催化剂和升高温度外,还可以采取的措施有(填一种)。
③若上述反应在恒容的密闭容器中进行,判断该反应达到平衡状态的标志是。
a.c(NO):c(O2)=2:1
b.每消耗1molO2的同时生成2molNO2
c.混合气体的颜色保持不变
硝酸盐污染已成为一个日益严重的环境问题,甲酸(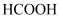 )在纳米级磁性
)在纳米级磁性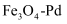 (钯)表面分解为活性
(钯)表面分解为活性 和
和 , 再经下列历程实现
, 再经下列历程实现 的催化还原,进而减少污染。已知
的催化还原,进而减少污染。已知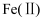 、
、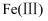 表示
表示 中二价铁和三价铁。下列说法错误的是( )
中二价铁和三价铁。下列说法错误的是( )
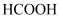 )在纳米级磁性
)在纳米级磁性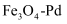 (钯)表面分解为活性
(钯)表面分解为活性 和
和 , 再经下列历程实现
, 再经下列历程实现 的催化还原,进而减少污染。已知
的催化还原,进而减少污染。已知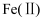 、
、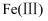 表示
表示 中二价铁和三价铁。下列说法错误的是( )
中二价铁和三价铁。下列说法错误的是( )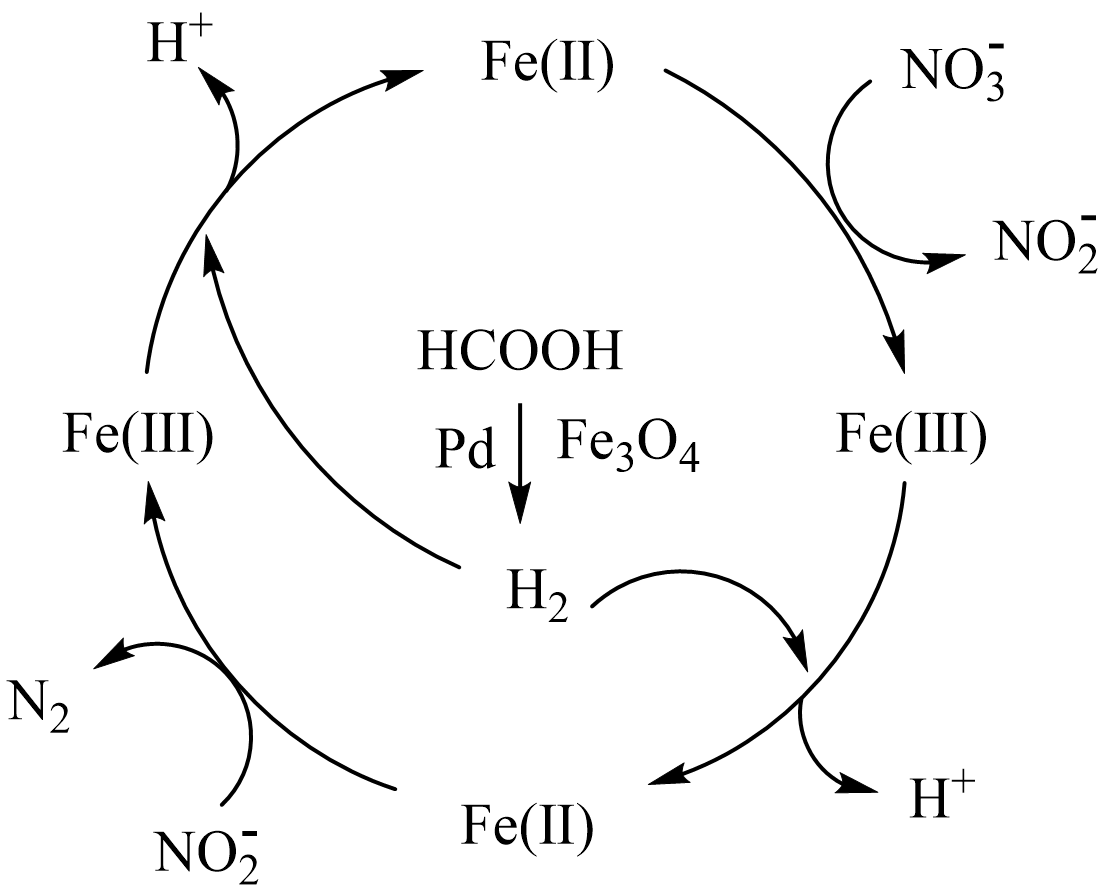
A . 生产中将催化剂处理成纳米级颗粒可增大甲酸分解的速率
B . 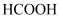 分解时,只有极性共价键发生了断裂
C . 在整个历程中,
分解时,只有极性共价键发生了断裂
C . 在整个历程中,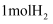 可完全还原
可完全还原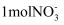 D . 反应历程中生成的
D . 反应历程中生成的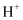 可调节体系
可调节体系 , 有增强
, 有增强 氧化性的作用
氧化性的作用
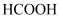 分解时,只有极性共价键发生了断裂
C . 在整个历程中,
分解时,只有极性共价键发生了断裂
C . 在整个历程中,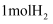 可完全还原
可完全还原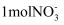 D . 反应历程中生成的
D . 反应历程中生成的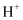 可调节体系
可调节体系 , 有增强
, 有增强 氧化性的作用
氧化性的作用
最近更新
- 如图14-2-8所示LC回路中C是一平行板电容器,两板水平放置,开关断开时,电容器内带电灰尘恰好静止,当开关S闭合后,灰
- —Dothey like salad? —Yes, they like ________ very much. A.it
- 若关于x的不等式的解集为x<2,则k的取值范围是 .
- 青春期身体各个器官都已经发育成熟,可以生育........ ...... .......( )
- A、B、C、D、E是前四周期原子序数依次增大的五种元素。A、D同主族且能形成两种常见化合物DA2和DA3;基态C原子最外
- 工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g)CH3OH(g)。图1表示反应中能量的变化;图2表
- 下列解释实验事实的方程式不正确的是 ( ) A.0.1mol/LCH3COOH溶液的pH>1
- The students in this college are all taking courses _______a
- 下列各对器官中,哪一可让演化上是同源的? A 长臂猿的上肢与下肢 B 苍蝇的翅和蝙蝠的翅 C 蛇的尾和苍蝇的
- ----- Is she a teacher? ------ Yes, _____. A. all right B. t
- 有一包白色粉末可能由Na2SO4、Na2CO3、BaCl2、CuSO4中的一种或几种组成。小刚为了测定该白色粉末的组成,
- 一位西方思想家曾说:“中国的儒教是令人钦佩的。毫无迷信,毫无荒诞不经的传说,更没有那种蔑视理性和自然的教条。”他可能属于
- 朱熹提出“存天理,灭人欲”,其中的“天理”主要是指
- 《新唐书》记载:“(卢商)早孤,家窭(jù,贫寒)困,能以学自奋。举进士、拔萃,皆中。由校书郎佐宣歙、西川幕府。入朝,累
- 皇权是对社会权力资源的独家垄断。它不仅有一套垄断和管理体系,而且有一套完备的调节系统,如防止皇帝决策失误的“封驳”制度、
- 做验证力的平行四边形定则实验,在圆形透明桌面上平铺一张白纸,在桌子边缘安装三个光滑的滑轮,如图所示,其中滑轮 固定在桌子
- 有两种有机物Q()与P(),下列有关它们的说法中正确的是( ) A.二者的核磁共振氢谱中均只出现两种峰且峰面积之比为
- 若=2,则= .
- 等离子电视4年来价格大幅度下降的根本原因是 A.生产的厂家增加,供求关系发生了根本变化 B.社会劳动生产率的提高,社会必
- “中国梦”,深刻道出了中国近代以来历史发展的主题主线,深情描绘了近代以来中华民族生生不息、不断求索、不懈奋斗的历史。她



