化学反应速率的影响因素 知识点题库
-
(1) 氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和NH3 , 在一定条件下发生反应:6NO(g) + 4NH3(g)
 5N2(g) +6H2O(g)。
5N2(g) +6H2O(g)。 ①能说明该反应已达到平衡状态的标志是
a.反应速率
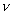 ( NH3) =
( NH3) = 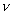 ( N2)
( N2) b.容器内压强不再随时间而发生变化
c.容器内N2的物质的量分数不再随时间而发生变化
d.容器内n(NO)∶n(NH3)∶n(N2)∶n(H2O) = 6∶4∶5∶6
②某次实验中测得容器内NO及N2的物质的量随时间变化如图所示,图中b点对应的速率关系是
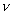 (正)
(正) 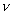 (逆)(填“﹥”、“﹤”或“﹦”),d点对应的速率关系是
(逆)(填“﹥”、“﹤”或“﹦”),d点对应的速率关系是 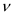 (正)
(正) 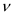 (逆)(填﹥、﹤或﹦)。
(逆)(填﹥、﹤或﹦)。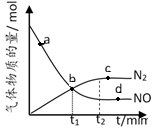
-
(2) 298 K时,若已知生成标准状况下2.24 L NH3时放出热量为4.62 kJ。写出合成氨反应的热化学方程式。在该温度下,取1 mol N2和3 mol H2放在一密闭容器中,在催化剂存在时进行反应。测得反应放出的热量总小于92.4 kJ,其原因是。
-
(3) 一定条件下,在2 L密闭容器内,反应2NO2(g)
 N2O4(g) ΔH=-180 kJ·mol-1 , n(NO2)随时间变化如下表:
N2O4(g) ΔH=-180 kJ·mol-1 , n(NO2)随时间变化如下表: 时间/s
0
1
2
3
4
5
n(NO2)/mol
0.040
0.020
0.010
0.005
0.005
0.005
用NO2表示0~2 s内该反应的平均速度。在第5 s时,NO2的转化率为。根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是。
 2CO
2CO  H>0。升高温度,关于该反应v正和v逆的说法正确的是( )
H>0。升高温度,关于该反应v正和v逆的说法正确的是( )
-
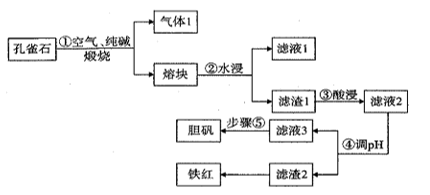
(1) 气体1的成分除H2O(g)外,还有,步骤①中发生氧化还原反应的化学方程式为 ,滤液1的主要成分的用途之一为。
-
(2) 目前工业生产中步骤③酸浸的百分率为70%,为进一步提高酸浸的百分率可采取的措施有(答出两点)。
-
(3) 步骤④调pH所用试剂为 。
-
(4) 室温下滤液3的pH=4,Ksp[Fe(OH) 3]=4×10-38 , 则滤液3中c(Fe3+)=。
-
(5) 步骤⑤操作为.。
-
(6) 假设使用孔雀石质量为m kg,步骤③酸浸的百分率为70%,经滤渣2所得铁红的质量为n kg,则孔雀石矿石中铁元素的含量为。
 N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol,在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=a kJ/mol,在温度T1和T2时,分别将0.50 mol CH4和1.2 mol NO2充入体积为1 L的密闭容器中,测得n(CH4)随时间变化数据如下表: | 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4) | 0.50 | 0.30 | 0.18 | …… | 0.15 |
下列说法不正确的是( )
-
(1) Fe、Co、Ni在周期表中的位置为,基态Fe原子的电子排布式为。
-
(2) CoO的面心立方晶胞如图所示。设阿伏加德罗常数的值为NA , 则CoO晶体的密度为g﹒cm-3:三种元素二价氧化物的晶胞类型相同,其熔点由高到低的顺序为。
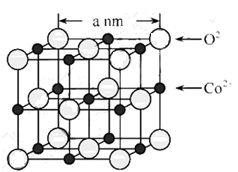
-
(3) Fe、Co、Ni能与Cl2反应,其中Co和为Ni均生产二氯化物,由此推断FeCl3、CoCl3和Cl2的氧化性由强到弱的顺序为,Co(OH)3与盐酸反应有黄绿色气体生成,写出反应的离子方程式:。
-
(4) 95℃时,将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示,当
 大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为。由于Ni与H2SO4反应很慢,而与稀硝酸反应很快,工业上选用H2SO4和HNO3的混酸与Ni反应制备NiSO4。为了提高产物的纯度,在硫酸中添加HNO3的方式为(填“一次过量”或“少量多次”),此法制备NiSO4的化学方程式为。
大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为。由于Ni与H2SO4反应很慢,而与稀硝酸反应很快,工业上选用H2SO4和HNO3的混酸与Ni反应制备NiSO4。为了提高产物的纯度,在硫酸中添加HNO3的方式为(填“一次过量”或“少量多次”),此法制备NiSO4的化学方程式为。 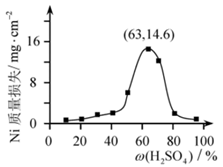
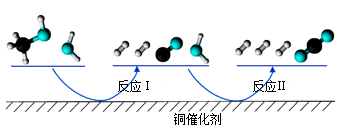

下列说法正确的是( )
 CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( )
CH3OH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是( ) 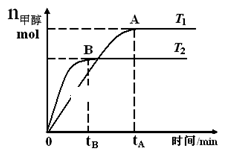
 B . 该反应在T1时的平衡常数比T2时的小
C . 任意时刻,T2温度下的反应速率均大于T1温度下的速率
D . 处于A点的反应体系从T1变到T2 , 达到平衡时
B . 该反应在T1时的平衡常数比T2时的小
C . 任意时刻,T2温度下的反应速率均大于T1温度下的速率
D . 处于A点的反应体系从T1变到T2 , 达到平衡时  增大
增大
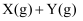
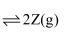 分别在①、②、③三种不同实验条件下进行,它们的起始浓度为
分别在①、②、③三种不同实验条件下进行,它们的起始浓度为 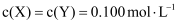 及
及 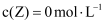 ,反应物X的浓度随时间变化如图所示。②、③与①比较只有一个实验条件不同,下列说法错误的是( )
,反应物X的浓度随时间变化如图所示。②、③与①比较只有一个实验条件不同,下列说法错误的是( ) 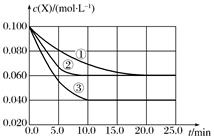
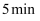 时实验③的反应速率最快
B . 条件②的反应最先达到平衡
C . ②与①比较可能是压强更大
D . 该反应的正反应是吸热反应
时实验③的反应速率最快
B . 条件②的反应最先达到平衡
C . ②与①比较可能是压强更大
D . 该反应的正反应是吸热反应
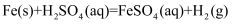 ,下列叙述错误的是( )
,下列叙述错误的是( )
 体积的变化情况表示该反应的速率
D . 若依据该反应设计原电池,正极材料应为铁
体积的变化情况表示该反应的速率
D . 若依据该反应设计原电池,正极材料应为铁
 浓度,降低
浓度,降低 浓度)
浓度)
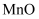 、
、  、
、 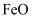 、
、  和一些有机物等杂质,其制备工艺流程如下:
和一些有机物等杂质,其制备工艺流程如下: 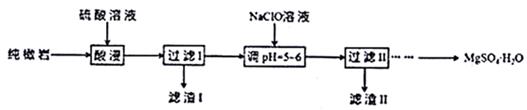
已知:① 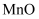 不溶于水,可溶于硫酸溶液②
不溶于水,可溶于硫酸溶液②  不溶于稀硫酸
不溶于稀硫酸
③ 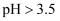 时,
时,  以
以 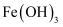 形式完全沉淀
形式完全沉淀
-
(1) 酸浸时,将纯橄岩粉碎的目的是。
-
(2) 酸浸时温度控制在
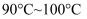 ,可采用的合适加热方式是。
,可采用的合适加热方式是。
-
(3) 滤渣Ⅰ中的主要成分是,实验室中过滤操作所需玻璃仪器有烧杯、漏斗、。
-
(4) 加入
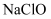 溶液,可将滤液I中的
溶液,可将滤液I中的  氧化成
氧化成  ,同时也将
,同时也将  氧化成
氧化成  。生成
。生成  反应的离子方程式是。检验滤液Ⅱ是否还含有
反应的离子方程式是。检验滤液Ⅱ是否还含有  :取适量溶液于试管中,加入试剂
:取适量溶液于试管中,加入试剂  ,观察现象。X最好选择(填符合题意选项的字母编号)。
,观察现象。X最好选择(填符合题意选项的字母编号)。 A.
 溶液 B.酸性
溶液 B.酸性  溶液 C.
溶液 C.  溶液
溶液 -
(5) 取10g洗净并已干燥的滤渣II,加入足量稀硫酸,充分反应后得4.65g固体,则滤渣II中铁元素的质量分数为。
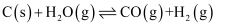 在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
在一密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
-
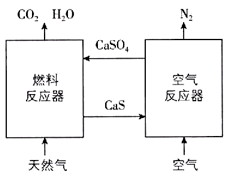
(1) 已知在燃料反应器中发生如下反应:
i.4CaSO4(s)+CH4(g)=4CaO(s)+CO2(g)+4SO2(g)+2H2O(g) ΔH1=a kJ·mol-1
ii.CaSO4(s)+CH4(g)=CaS(s)+2H2O(g)+CO2(g) ΔH2=b kJ·mol-1
iii.CaS(s)+3CaSO4(s)=4CaO(s)+4SO2(g) ΔH3=c kJ·mol-1
①燃料反应器中主反应为(填"i""ii"或"iii")。
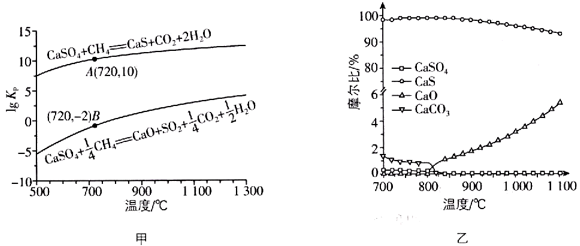
②反应i和ii的平衡常数Kp与温度的关系如图甲,则a(填">""="或"<")0;720 ℃时反应iii的平衡常数Kp=。
③下列措施可提高反应ii中甲烷平衡转化率的是。
A.增加CaSO4固体的投入量
B.将水蒸气冷凝
C.降温
D.增大甲烷流量
-
(2) 如图乙所示,该燃料反应器最佳温度范围为850~900℃之间,从化学反应原理的角度说明原因:。
-
(3) 空气反应器中发生的反应为CaS(s)+2O2(g)=CaSO4(s) ΔH4=d kJ·mol-1
①根据热化学原理推测该反应为反应。
②在天然气燃烧过程中,可循环利用的物质为。
-
(4) 该原理总反应的热化学方程式为。
 CO(g)+H2(g)在一容积可变的密闭容器中进行,下列条件的改变能使反应速率加快的是( )
CO(g)+H2(g)在一容积可变的密闭容器中进行,下列条件的改变能使反应速率加快的是( )①将容器的容积缩小一半 ②加入过量炭 ③保持容器压强不变,充入N2 ④升高温度
- 【小题1】It’s ________ (polite) to ask a woman’s name in western
- 道教植根中华文化沃土,坚持“行道立德、济世利人”。近代以来,其尊道贵德、道法自然、 返璞归真、崇俭抑奢、上善若水、正己化
- 若向量满足:,,,则( ) A.2 B. C.1 D.
- 物体A和B用轻绳相连挂于轻弹簧下静止不动,如图所示,A质量为m,B质量为M,当A、B间的轻绳突然断开后,物体A第一次上升
- 除去下列各物质中的少量杂质,所选用的试剂、方法均正确的是()编号 物质 杂质 试剂 除杂操作方法 A CO2 CO ﹣﹣
- 图1是某微粒的结构示意图,其中X=,该微粒在化学反应中易(填“得”或“失”)电子变成的微粒;写出一条从图2中获得的信息.
- 下列细胞分裂时观察不到纺锤体的是 () ①细菌细胞 ②根尖的分生区细胞 ③蛙的红细胞 ④蛙的次级精
- 公说公有理,婆说婆有理是( ) (1)不正确的,因为客观事物的本来面目是唯一的 (2)正确的,因为在认识上有仁者见仁
- 计算:= ,= .
- 离子推断题(6分)某待测液中可能含有Mg2+、NH4+、Ba2+、CO32-、SO42-、AlO2-等离子,各取少量进行
- 某班某同学要测量学校升旗的旗杆高度,在同一时刻,量得某一同学的身高是1.5m,影长是1m,旗杆的影长是8m,则旗杆的高度
- 现有下列物质,其中符合Cn(H2O)m的组成,但不属于糖类的是() ①纤维素 ②甲酸甲酯 ③淀粉 ④甲醛 ⑤丙酸 ⑥
- 下列物理量属于标量的是( ) A.速度 B.位移 C.功
- 在⊙O中,AB是⊙O的直径,AB=8cm,==,M是AB上一动点,CM+DM的最小值是() A.6cm B
- 在水中波长为400 nm的光子的能量为______________J,已知水的折射率为1.33,普朗克常量h=6.63×
- 下列实验现象的描述错误的是A. 氢气在氯气中燃烧生成绿色烟雾 B. 红热的铁丝在氧气中燃烧,火星四射,生成黑色固体颗粒
- 10g细铁丝在充足的氧气中完全燃烧,燃烧后生成物的质量 ( ) A. 约等于10g B.
- 实验证明,维生素B1在140℃时还不至于被分解破坏。有人做馒头时爱加过量的碱,长此以往,容易患脚气病。这是因为( )A.
- 下列没有安全问题的是( ) A 食用氢氧化钠治胃酸过多病 B 蚊虫叮咬(分泌蚁酸)涂抹牙膏或肥皂水 C 食
- 1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决.它不能解释下列哪些



