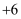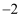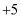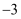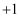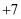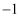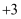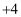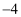元素周期表中原子结构与元素性质的递变规律 知识点题库
如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是 ( )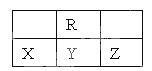
①酸性:HClO4>HBrO4>HIO4②碱性:Ba(OH)2>Mg(OH)2>Be(OH)2③氧化性:F>C>O ④还原性:Cl<S<Si⑤气态氢化物稳定性:HF>HCl>H2S.
-
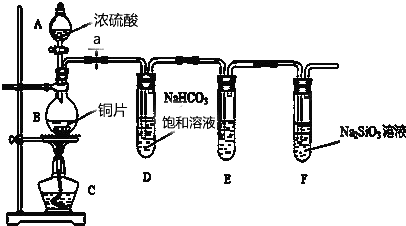
(1) 填写所示仪器名称A
-
(2) 实验步骤:连接仪器、、加药品后,打开a、然后滴入浓硫酸,加热
-
(3) 问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是.装置E中盛足量酸性KMnO4溶液的作用是
②该实验证明碳元素的非金属性比硅元素非金属性强的实验依据是.请写出F 中发生反应的离子方程式
③依据试管D中的发生的反应,能否证明硫元素的非金属性强于碳元素的非金属性(填“能”或“否”),原因是.
性质 元素 | 8O | 16S | 34Se | 52Te |
单质熔点(℃) | ﹣218.4 | 113 | 450 | |
单质沸点(℃) | ﹣183 | 444.6 | 685 | 989 |
主要化合价 | ﹣2 | ﹣2,+4,+6 | ﹣2,+4,+6 | |
原子半径 | 逐渐增大 | |||
单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
请根据表回答下列问题:
-
(1) 硒的熔点范围可能是.
-
(2) 碲的化合价可能有.
-
(3) 氢硒酸有较强的(填“氧化性”或“还原性”),因此放在空气中长期保存易变质,其可能发生反应的化学方程式为.
-
(4) 工业上Al2Te3可用来制备H2Te,完成下列化学方程式: Al2Te3+═ Al(OH)3↓+H2Te↑
① 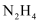 分子中既含极性键又含非极性键
分子中既含极性键又含非极性键
②若  和
和 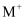 的电子层结构相同,则原子序数:
的电子层结构相同,则原子序数: 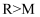
③  、
、 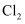 、
、 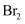 、
、  熔点随相对分子质量的增大而升高
熔点随相对分子质量的增大而升高
④  、
、  、
、  、
、  分子中各原子均达到
分子中各原子均达到 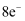 稳定结构
稳定结构
⑤固体熔化成液体的过程是物理变化,所以不会破坏化学键
⑥ 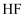 分子很稳定是由于
分子很稳定是由于 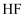 分子之间能形成氢键
分子之间能形成氢键
⑦由于非金属性: 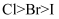 ,所以酸性:
,所以酸性: 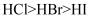
-
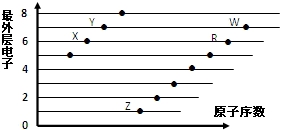
(1) Z在元素周期表中的位置是。
-
(2) 该玉石的成分是W2Y10Z12X30 , 若CaSO4的化学式可以写成CaO·SO3二元化合物组合的形式,则该玉石的成分用二元化合物组合的形式可以写成。
-
(3) 已知Z的单质可以溶于Y的氧化物对应的水化物溶液中,该过程发生反应的离子方程式是。
-
(4) 四种元素的单质及其化合物广泛应用于电池、通信等领域。
①Z的单质常用作材料(填一种,下同);X和Z组成的化合物常用作材料。
②W离子电池比Y离子电池有更好的储能优势,其原因是。在W离子电池
中,W离子嵌入石墨形成复合材料WC6 , 该材料是电池的负极材料,当电池部分放电释
放出x个W离子时,该电极反应式是。
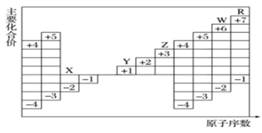
性质元素 | 原子半径 | 最高价态 | 最低价态 | 性质元素 | 原子半径 | 最高价态 | 最低价态 |
① | 1.02 |
|
| ⑥ | 1.10 |
|
|
② | 2.27 |
| - | ⑦ | 0.99 |
|
|
③ | 0.74 | - |
| ⑧ | 1.86 |
| - |
④ | 1.43 |
| - | ⑨ | 0.75 |
|
|
⑤ | 0.77 |
|
| ⑩ | 1.17 |
|
|
试回答下列问题:
-
(1) 以上10种元素中,第一电离能最小的是(填编号)。
-
(2) 上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每一个原子都满足
 稳定结构的物质是(写分子式)。元素⑤和⑩形成的化合物的化学式为物质类型为(填离子化合物、共价化合物):元素①的原子价电子排布式是。
稳定结构的物质是(写分子式)。元素⑤和⑩形成的化合物的化学式为物质类型为(填离子化合物、共价化合物):元素①的原子价电子排布式是。
-
(3) ①、⑥、⑦三种元素的气态氢化物的稳定性,由强到弱的顺序是(填化学式)。
-
(4) ③和⑨两元素比较,非金属性较弱的是(填名称),可以验证你的结论的是下列中的(填序号)。
A.气态氢化物的挥发性
B.单质分子中的键能
C.两元素的电负性
D.含氧酸的酸性
E.氢化物中
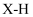 键的键长(X代表③和⑨两元素)
键的键长(X代表③和⑨两元素)
- 从甲地(70°N,80°E)到乙地(70°N,60°E),若不考虑地形因素,最近的走法是 A.一直朝正东方走 B.先向东
- SOUTHPORT, ENGLAND—A British teaching union famous for stran
- 十六大报告强调:要“形成全民学习、终身学习的学习型社会,促进人的全面发展。”结合文化的有关知识,谈谈你对建立学习型社会的
- 《论语》是大思想家孔子的语录,宋代宰相赵普有“半部论语治天下”之说。孔子思想的核心主张是A.“仁”和“礼” B.“因材
- (·黑龙江省哈三中高三上月月考) 35. --- Do you know the reason _______
- (8分)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。(1)
- His first baby was born soon after he got married,which see
- 下列文学常识错误的一项是 ( )(3分)A.《我的叔叔于勒》作者是莫泊桑,法国人,他与契诃夫、欧·亨利被并称为“世
- 取10g金属锌样品(假设其中杂质和硫酸不反应,也不溶于水),加入到试管中,和足量的稀硫酸充分反应后,得到0.2g氢气。请
- 中国古代早期的政治制度对后世产生了深远影响。当今社会提倡尊老爱幼、家庭和睦等文明行为,追溯历史渊源应与下列哪一制度有关
- 联合国将2011年定为“国际化学年”,以彰显化学对知识进步、环境保护和经济发展做出的重要贡献. (1)化肥的使用大幅度提
- 洛克认为,人出生时心灵像白纸或白板一样,人的一切观念和知识都是外界事物在白纸或白板上留下的痕迹,最终都源于经验。他的观点
- 阅读下面的文字,根据要求写一篇不少于800字的文章。 4月12日晚,湖南卫视大型魔幻情景互动秀开播。节目开始不久
- ......
- 有关人类生殖和发育的叙述,不正确的是( ) A.受精作用发生在女性输卵管里 B.卵巢产生卵细胞和分泌雌性激素,睾丸产生
- 函数的定义域是 ________ _
- 水展示万千气象。因势而变,舒缓为溪,低吁浅唱;陡峭为瀑,虎啸龙吟。水因势利导,焕发勃勃生机。因器而变,遇圆则圆,逢方则方
- 已知等比数列{an}满足a1+a2=3,a2+a3=6,则a7= A、64 B、81 C、128
- 现提供以下器材: 电流表: ( 满偏电流100μA,内阻100Ω); 电流表:(量程10mA,内阻40Ω); 滑动变阻器
- He bought a book that could glee him much knowledge and ____