浓硫酸的性质 知识点题库
下列各组气体中,在通常情况下能共存且都能用浓硫酸干燥的是( )
A . SO2、H2S
B . NO2、O2
C . HCl、HBr
D . H2S、CO2
下列不能与浓H2SO4反应的物质是( )
A . Cu
B . C
C . Na2CO3
D . SiO2
下列对硫酸的叙述正确的是( )
A . 因浓硫酸具有强氧化性,故不可用它来干燥氢气
B . 浓硫酸与浓氨水靠近时产生大量白烟
C . 浓硫酸有强氧化性,稀硫酸不具有氧化性
D . 浓硫酸具有腐蚀性,取用时要小心
向50mL 18mol/L的硫酸中加入足量的铜片并加热,被还原的硫酸的物质的量( )D
A . 等于0.9mol
B . 大于0.45mol,小于0.9mol
C . 等于0.45mol
D . 小于0.45mol
浓硫酸和2mol•L﹣1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如图,分析a、b曲线变化的原因是( )
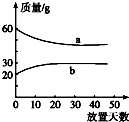
A . a升华、b冷凝
B . a冷凝、b吸水
C . a挥发、b潮解
D . a挥发、b吸水
某同学为了检验浓硫酸与木炭发生反应产生的所有气体产物,设计了如下反应流程:
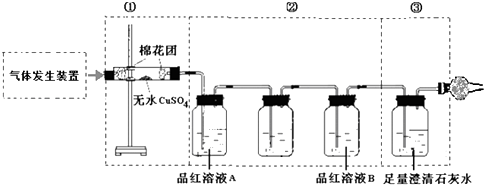
-
(1) 气体发生装置应该选择下图给出的;
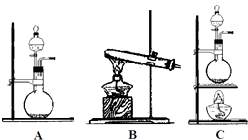
写出浓硫酸和木炭在该装置中发生反应的化学方程式;
-
(2) ①中无水硫酸铜的作用是;
-
(3) ②中间洗气瓶中试剂为;作用是;
-
(4) ②中两次用到品红溶液,B的作用是;
-
(5) ③中出现的现象是.
某化学兴趣小组用下图所示装置探究浓硫酸与铜是否发生反应及反应所产生气体性质.请回答下列问题:
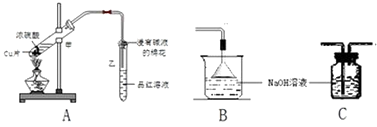
-
(1) 写出试管甲中所发生反应的化学反应方式.
试管乙口部浸有碱液的棉花其作用是.
-
(2) 试管甲中溶液变为色,乙中品红溶液等现象,说明了铜和浓硫酸发生了化学反应,并且该现象还能说明产生的气体具有性.
-
(3) SO2的排放是造成酸雨的主要因素,为了减少SO2的排放,常用石灰(CaO)法对煤燃烧后的烟气脱硫,其原理是(用化学方程式表示).
-
(4) SO2在适当的温度并有一定催化剂存在的条件下可以转化为SO3 , 其化学方程式为.
-
(5) 为防止二氧化硫造成空气污染,如果需要在装置末端增加尾气吸收装置,应选择的装置是(填“B”或“C”).
50mL18mol/L的硫酸与足量铜片共热,被还原的硫酸的物质的量是( )
A . 大于0.9 mol
B . 等于0.45 mol
C . 小于0.45mol
D . 大于0.45 mol小于0.9 mol
-
(1) 把对应物质的字母代码填入括号内.
A.水玻璃
B.明矾
C.次氯酸钙
D.过氧化钠 E.新制氯水 F.小苏打
①能使石蕊试液先变红后褪色。
②能做木材防火剂。
③能做处理胃酸过多的一种药剂。
-
(2) 把下列现象中硫酸所表现出来的性质填写在空白处。
①用玻璃棒蘸浓硫酸滴在纸上时,纸变黑。浓硫酸表现性。
②在常温下可以用铁、铝制容器盛装冷的浓硫酸。浓硫酸表现性。
③盛有浓硫酸的烧杯敞口放置一段时间后,质量增加。浓硫酸表现性。
下列相关实验的说法中错误的是( )
A . 镀锌铁皮锌层厚度测定时,当反应速率突然变慢时,表明铁皮表面的的锌层已反应完全
B . 可用纸层析法分离微量的Fe3+离子与Cu2+离子形成的混合物
C . 分液时,先将上层液体从上口倒出,然后再将下层液体从下口放出
D . 可用白纸鉴别浓硫酸和稀硫酸
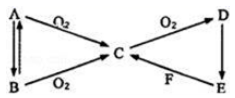
A、B、C、D、E、F为中学化学常见的单质或化合物,其中A、F为单质,常温下,E的浓溶液能使铁、铝钝化,相互转化关系如图所示(条件已略去)。完成下列问题:
-
(1) 若A为淡黄色固体,B为气体,F为非金属单质。
①写出E转变为C的化学方程式。
②B在空气中能使银器表面失去金属光泽、逐渐变黑,反应的化学方程式为。
-
(2) 若B为能使湿润的红色石蕊试纸变蓝的气体。
①A的电子式为。
②做过银镜反应后的试管可用E的稀溶液清洗,反应的离子方程式为。
③在干燥状态下,向②反应得到的溶质中通入干燥的氯气,得到N2O5和一种气体单质,写出反应的化学方程式。
下列实验的现象与对应结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显变化 | Al与浓硝酸不反应 |
| C | 过量的Fe粉中加入稀HNO3 , 充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |
A . A
B . B
C . C
D . D
某实验过程如图所示,则下列叙述中正确的是( )
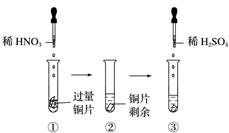
A . 试管①中的离方程式为:Cu+4H++2NO  = Cu2++2NO2↑+2H2O
B . 试管③中铜片溶解,放出红棕色有刺激性气味的气体
C . 试管③中无明显现象,因稀H2SO4不与铜反应
D . 试管③中的离方程式为:3Cu+8H++2NO
= Cu2++2NO2↑+2H2O
B . 试管③中铜片溶解,放出红棕色有刺激性气味的气体
C . 试管③中无明显现象,因稀H2SO4不与铜反应
D . 试管③中的离方程式为:3Cu+8H++2NO  =3Cu2++2NO↑+4H2O
=3Cu2++2NO↑+4H2O
 = Cu2++2NO2↑+2H2O
B . 试管③中铜片溶解,放出红棕色有刺激性气味的气体
C . 试管③中无明显现象,因稀H2SO4不与铜反应
D . 试管③中的离方程式为:3Cu+8H++2NO
= Cu2++2NO2↑+2H2O
B . 试管③中铜片溶解,放出红棕色有刺激性气味的气体
C . 试管③中无明显现象,因稀H2SO4不与铜反应
D . 试管③中的离方程式为:3Cu+8H++2NO  =3Cu2++2NO↑+4H2O
=3Cu2++2NO↑+4H2O
浓硫酸是实验室必备的重要试剂。下列有关浓硫酸的说法中,错误的是( )
A . 具有强腐蚀性,不可用手直接接触
B . 具有吸水性,实验室中可用于干燥氨气
C . 具有脱水性,能使蔗糖因脱水而变黑
D . 具有强氧化性,加热时能与铜发生反应
某实验小组的同学在实验室利用下列装置进行实验。
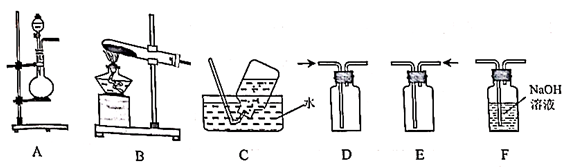
请回答下列问题:
-
(1) 甲同学用
 装置制备
装置制备  气体,上述装置中可用于收集
气体,上述装置中可用于收集  气体的是(填字母),
气体的是(填字母),  中发生反应的离子方程式为。
中发生反应的离子方程式为。
-
(2) 乙同学用上图中的装置
 进行铜与浓硫酸反应制取
进行铜与浓硫酸反应制取  气体,装置
气体,装置  中还缺少的仪器名称是,该反应的化学方程式为;实验所产生的
中还缺少的仪器名称是,该反应的化学方程式为;实验所产生的  尾气选用装置(填字母)来吸收。
尾气选用装置(填字母)来吸收。
-
(3) 丙同学用装置
 制取氨气,发生反应的化学方程式是;为了检验集气瓶中氨气是否集满,可将湿润的红色石蕊试纸置于导管口,若,则证明已收集满;若将一端蘸有浓盐酸的玻璃棒接近导管口,观察到的现象是,该反应的化学方程式为。
制取氨气,发生反应的化学方程式是;为了检验集气瓶中氨气是否集满,可将湿润的红色石蕊试纸置于导管口,若,则证明已收集满;若将一端蘸有浓盐酸的玻璃棒接近导管口,观察到的现象是,该反应的化学方程式为。
-
(4) 丙同学在实验室中模拟氨的催化氧化反应,该反应中,当生成标准状况下
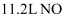 时,被氧化的氨的质量是
时,被氧化的氨的质量是 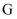 。
。
实验室盛装浓硫酸的试剂瓶上贴有的标识是( )
| A | B | C | D |
| | | | |
| 有毒气体 | 腐蚀品 | 易燃液体 | 爆炸品 |
A . A
B . B
C . C
D . D
实验目的:为研究铁质材料与热浓硫酸的反应
-
(1) 称取铁钉(碳素钢)
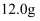 放入
放入 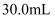 浓硫酸中,加热,充分反应后得到溶液
浓硫酸中,加热,充分反应后得到溶液  并收集到气体
并收集到气体  。
。 ①甲同学认为
 中除
中除  外还可能含有
外还可能含有  。若要确认其中是否含有
。若要确认其中是否含有  ,应选择加入的试剂为(选填序号)
,应选择加入的试剂为(选填序号)A.
 溶液和氯水 B.铁粉和
溶液和氯水 B.铁粉和  溶液 C.浓氨水 D.酸性
溶液 C.浓氨水 D.酸性  溶液
溶液②乙同学取
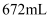 (标准状况)气体
(标准状况)气体  通入足量溴水中,然后加入足量
通入足量溴水中,然后加入足量  溶液,经适当操作后得到干燥固体
溶液,经适当操作后得到干燥固体 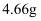 。据此推知气体
。据此推知气体  中
中  的体积分数为。(保留三位有效数字)。
的体积分数为。(保留三位有效数字)。 -
(2) 分析上述实验中
 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有  和
和  气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有  的原因是。
的原因是。 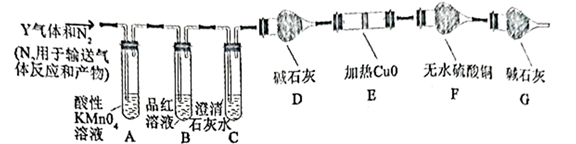
-
(3) 装置A中试剂的作用是,反应的离子方程式。
-
(4) 简述确认气体Y中含有
 的实验现象。
的实验现象。
-
(5) 如果气体Y中含有
 ,预计实验现象应是。
,预计实验现象应是。
按要求回答下列问题:
-
(1) 写出
 的电子式;
的电子式;
-
(2) 用电子式表示
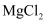 的形成过程;
的形成过程;
-
(3) 写出
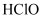 的结构式,它的空间构型为;
的结构式,它的空间构型为;
-
(4) 写出铜和浓硫酸反应的化学方程式;
-
(5) 写出实验室用
 代替
代替  制氯气的离子方程式。
制氯气的离子方程式。
某兴趣小组设计以下装置进行铜与浓硫酸的反应,并检验生成产物。试管a中加入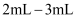 浓硫酸,在烧杯中加入饱和的氢氧化钠溶液,将螺旋状的铜丝连接在2号注射器活塞的橡胶上,1号注射器配有较长的耐腐蚀的针头。
浓硫酸,在烧杯中加入饱和的氢氧化钠溶液,将螺旋状的铜丝连接在2号注射器活塞的橡胶上,1号注射器配有较长的耐腐蚀的针头。
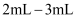 浓硫酸,在烧杯中加入饱和的氢氧化钠溶液,将螺旋状的铜丝连接在2号注射器活塞的橡胶上,1号注射器配有较长的耐腐蚀的针头。
浓硫酸,在烧杯中加入饱和的氢氧化钠溶液,将螺旋状的铜丝连接在2号注射器活塞的橡胶上,1号注射器配有较长的耐腐蚀的针头。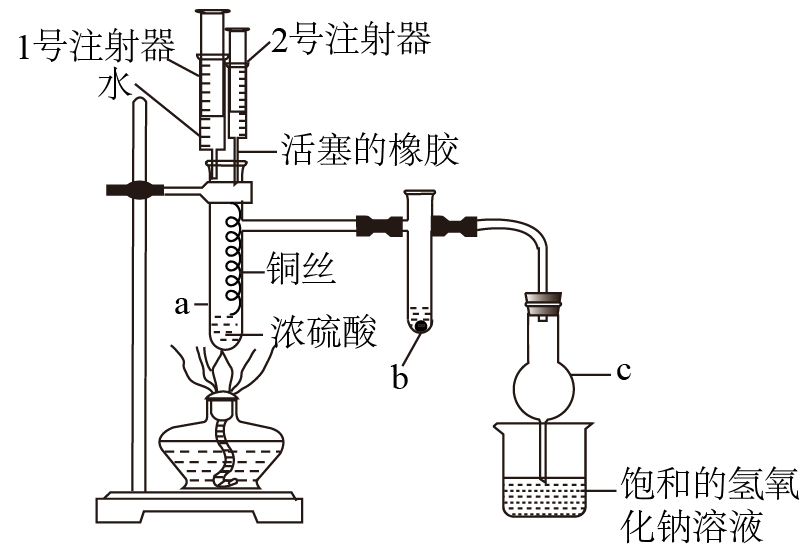
请回答:
-
(1) 试剂b为
-
(2) 推动2号注射器活塞,将铜丝浸没在浓硫酸中,加热试管a,使反应开始进行,实验任务完成后,使反应停止的操作:
-
(3) 利用1号注射器证明该实验中有
 生成的具体操作和现象:
生成的具体操作和现象:
-
(4) 实验结束后,如何检验烧杯中是否有硫酸根离子?
下列有关硫酸的叙述正确的是( )
A . 常温下铜与浓硫酸剧烈反应
B . 盛有浓硫酸的试剂瓶敞口放置,瓶口会出现大量白雾
C . 将浓硫酸和稀硫酸分别滴入蔗糖中会产生不同现象
D . 浓硫酸有强氧化性,常温下不能用铁制或铝制容器盛装
最近更新
- 、英国议会中的内阁是对哪个机构负责( ) A.国王 B.首相
- 德国当地时间2010年10月25日夜间,章鱼保罗在奥博豪森水族馆去世。2010年南非世界杯期间,章鱼哥保罗成功预测了8场
- 在1833~1915年“共和”、“民主”这两个关键词在部分著作和报刊中出现频率的统计中,1905~1913年“共和”出现
- 已知是两个集合,定义集合,若、,则 A. B. C. D.
- 氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如右图。 4NH3(g)+
- 010年8月7日,甘肃甘南藏族自治州舟曲县发生特大泥石流,一汽车停在小山坡底,突然司机发现在距坡底240 m的山坡处泥石
- 宁宁在学习“化学元素与人体健康”后,查阅到如下资料,请你给下表的“*”处选择恰当的选项 () *_______种类
- (10分)短周期主族元素A、B、C、D的原子序数依次增大,A与D同主族,B与C在同一周期,B原子最外层电子数比C原子少2
- 某同学做了一个用以测定光照强度与生态缸生物气体交换的试验,将若干小球藻、水草及小鱼各一份(完全相同)放入甲、乙两个等同的
- 根据右图所示的实验现象,下列判断不正确的是 A.现象①②说明物质燃烧需要氧气 B.现象①说明白磷的着火点不高于80℃ C
- 若点M(x,y)满足(x+y)2 =x2 +y2 -2,则点M所在象限是 A.第一象限或第三象限 B.第二象限
- 依次填入下列各句横线处的词语,恰当的一组是( ) (1)这些药品质量低劣,__群众,严重危害人民群众的健康与生命安
- It’s me why Alice, aged 28, gave up her job and got
- ---IsJenny an outgoing girl? ---No, she is
- 已知:如图,正方形纸片ABCD的边长是4,点M、N分别在两边AB和CD上(其中点N不与点C重合),沿直线MN折叠该纸片,
- 中国首个空间实验室——“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),它是一种将水电解技术与氢氧燃料电池技术相结合
- 下列有关生态系统功能的描述,错误的是 A.物质循环的关键环节是分解者的分解作用 B.物质流是循环的,能量流是单向的,信息
- 在△ABC中,AB=CB,∠ABC=90°,F为AB延长线上一点,点E在BC上,且AE=CF. (1)求证:Rt△ABE
- 1921年10月,列宁在党代会上指出:“新经济政策的全部意义……就在于而且仅仅在于:要找到我们用很大力量才能建立起来的那
- 某交流发电机产生的按正弦规律变化的电动势最大值为311V,其线圈共100匝,在匀强磁场中,匀速转动的角速度为。 (1)







