工业合成氨 知识点题库
①水 ②空气 ③焦炭 ④铁触媒
①原料气制备 ②氨的合成 ③原料气净化和压缩 ④氨的分离.
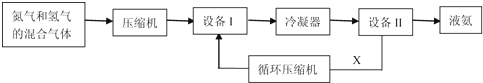
(1)设备 I的名称是 ,沿X路线循环的物质是 (填字母).
A.N2和H2 B.催化剂 C.NH3D.N2、H2和NH3
(2)合成氨中H2可以由焦炭和水蒸汽反应获得.请写出该反应的化学方程式: .
(3)原料气中往往含有H2S、CO、CO2等杂质,必须除去这些杂质的目的是 ,常用K2CO3溶液除去CO2 , 其反应的离子方程式为 .
(4)近年有人将电磁场直接加在氮气和氢气反应的容器内,在较低的温度和压强条件下合成氨,获得了较高的产率.电磁场对合成氨反应本质的影响是 ,该方法的优点是 .
(4)合成氨工业往往含有大量含氨废水,为了防止对环境造成污染,可以利用电解法将NH3•H2O转化为对环境无污染的加以处理.电解时以石墨做电极,以硝酸作为电解质,则理论上处理1mol NH3•H2O,电路中转移电子 mol,阳极的电极反应式为 .
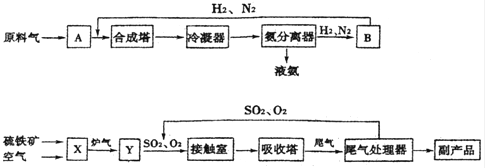
合成塔和接触室中的反应分别为:
N2(g)+3H2(g)⇌2NH3(g)△H=0;2SO2(g)+O2(g)⇌2SO2(g)△H=0.
(1)写出流程中设备的名称:B ,X .
(2)进入合成塔和接触室中的气体都要进行热处理,最理想的热处理方法是 充分利用反应中放出的热量加热反应气 .
(3)采用循环操作可提高原料的利用率,下列生产中,采用循环操作的是 (填序号).
①硫酸工业 ②合成氨工业 ③硝酸工业
(4)工业上常用98.3%的浓硫酸吸收SO3而不用稀硫酸或水的原因是 .
(5)工业生产中常用氨﹣﹣酸法进行尾气脱硫,以达到消除污染、废物利用的目的.硫酸工业尾气中的SO2经处理可以得到一种化肥,该肥料的化学式是 .
(6)根据化学平衡移动原理,下列条件或措施合理的是 (填序号).
①合成氨工业在高压下进行 ②合成氨工业和硫酸工业都使用催化剂 ③及时将氨液化而分离 ④硫酸工业中,净化后的炉气中要有过量空气 ⑤合成氨工业和硫酸工业都采用适宜的温度.
-
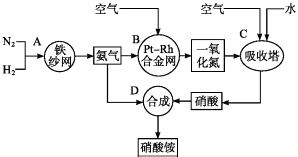
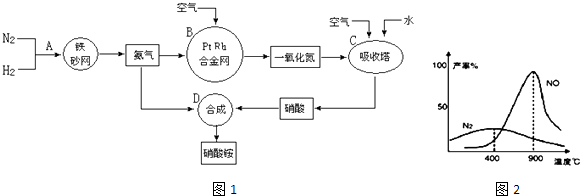
(1) 写出N2和H2通过红热的铁纱网生成氨气的反应方程式:.
-
(2) B装置中Pt﹣Rh合金网的作用是
-
(3) 写出B中的反应方程式:.
-
(4) 写出D中的反应方程式:.
-
(5) 吸收塔C中通入空气的目的是.
-
(1) Ⅰ污水经过一级、二级处理后,还含有少量Cu2+、Hg2+、Pb2+等重金属离子,可加入沉淀剂使其沉淀.下列物质不能作为沉淀剂的是
A.氨水 B.硫化氢气体
C.硫酸钠溶液 D.纯碱溶液
Ⅱ合成氨的流程示意图如下:
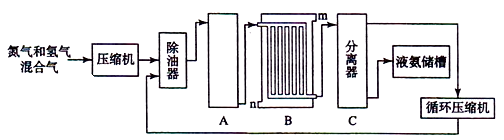
回答下列问题:
工业合成氨的原料是氮气和氢气.氮气是从空气中分离出来的,通常使用的两种分离方法是,;氢气的来源是水和碳氢化合物,写出分别采用煤和天然气为原料制取氢气的化学反应方程式,;
-
(2) 设备A中含有电加热器、触煤和热交换器,设备A的名称,其中发生的化学反应方程式为;
-
(3) 设备B的名称,其中m和n是两个通水口,入水口是(填“m”或“n”).不宜从相反方向通水的原因;
-
(4) 设备C的作用;
-
(5) 在原料气制备过程中混有CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:
CO(g)+H2O(g)⇌CO2 (g)+H2 (g)
已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于.
回答下列问题:
-
(1) 氨合成塔适宜的压强是20~50MPa,如果压强过大,除对设备要求高外,还会导致的结果是.
-
(2) 合成硝酸的吸收塔内填充瓷环,其作用是,吸收塔中还需补充空气的目的是.
-
(3) 若输送NH3的管道某处发生泄漏,检测的简单方法为.
-
(4) 在一定温度和压强的密闭容器中,将物质的量之比为3:2的H2和N2混合,当该反应达到平衡时,测出平衡混合气中氨的体积分数为25%,此时H2的转化率为.
-
(5) 制硝酸氧化炉中氨气和氧气在145℃就开始反应,在不同温度和催化剂条件下生成不同产物(如图所示).温度较低时以生成为主,900℃时发生主要反应的化学方程式为,当温度高于900℃时,NO产率明显下降的原因是.
-
(6) 若N2、H2合成氨时,H2的转化率为60%,NH3催化氧化制HNO3时的损失20%的氨,其它环节的损失忽略不计.则10tH2最多可以制取 t硝酸铵.
 NH2COONH4 (s) △H=-272kJ·mol-1。某化学兴趣小组利用下图实验装置(部分固定装置已省略)模拟制备NH2COONH4。试回答下列问题:
NH2COONH4 (s) △H=-272kJ·mol-1。某化学兴趣小组利用下图实验装置(部分固定装置已省略)模拟制备NH2COONH4。试回答下列问题: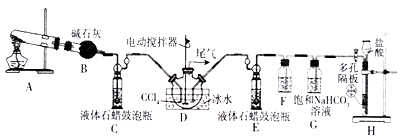
-
(1) 仪器组装完毕后,首先应进行的操作是。
-
(2) 装置A用于实验室制取NH2COONH4的原料气体之一,该反应的化学方程式为。
-
(3) 装置F中试剂的名称为,装置G的作用为。
-
(4) 为提高原料气的利用率,应控制装置C和E中最佳鼓泡速率比为,装置D采用冰水浴的原因为。
-
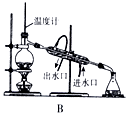
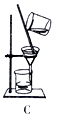
(5) 生成的氨基甲酸铵悬浮于CCl4 中,下列操作可实现产品分离的是。


-
(6) 实验装置中存在明显不足之处的是,有同学认为装置H、G和F组成的装置过于复杂可简化,请简述该方法:。
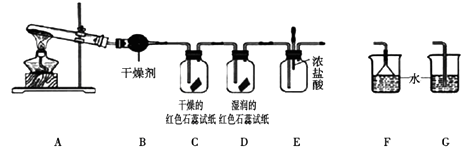
【实验探究】
-
(1) A中发生反应的化学方程式为;
-
(2) B中盛放的干燥剂为,干燥氨气能否用浓硫酸(填“能”或“不能”) ;
-
(3) 若有10.7gNH4Cl固体,最多可制取NH3(标准状况)的体积是L;
-
(4) 实验室收集氨气的方法是;
-
(5) C、D装置中颜色会发生变化的是(填“C”或“D”),红色石蕊试纸变成色;
-
(6) 当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是;
-
(7) 为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是(填“Y”或“G”)。

-
(1) 工业上用氢气和氮气直接合成氨,写出反应的化学方程式。氨气极易溶于水,水溶液显 性,能使酚酞溶液变色,使湿润的红色石蕊试纸变色。
-
(2) 氮的氧化物有多种,一氧化氮和二氧化氮都是大气污染物。氨气在催化剂作用下可被氧化生成一氧化氮,一氧化氮气体与空气变色,原因是(用化学方程式表示);二氧化氮易溶于水并与水反应,此反应的氧化剂是,还原剂是,氧化剂和还原剂的质量之比为
-
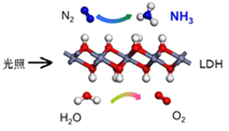
(1) 化学家
 证实了氢气与氮气在固体催化剂表面合成氨的过程,示意图如下:
证实了氢气与氮气在固体催化剂表面合成氨的过程,示意图如下: 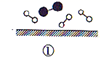

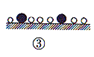
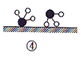
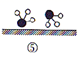
下列说法正确的是____________(填标号)。
A . ①表示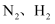 分子中均是单键
B . ②→③需要吸收能量
C . ③→④需要吸收能量
D . 该过程表示了化学变化中包含旧化学键的断裂和新化学键的生成
分子中均是单键
B . ②→③需要吸收能量
C . ③→④需要吸收能量
D . 该过程表示了化学变化中包含旧化学键的断裂和新化学键的生成
-
(2) 合成氨反应在不同压强、使用相同催化剂条件下,初始时氮气和氢气的体积比为
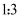 时,平衡时混合物中氨的体积分数
时,平衡时混合物中氨的体积分数  与温度的变化关系如图所示。
与温度的变化关系如图所示。 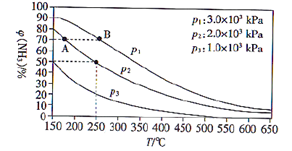
①若分别用
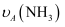 和
和 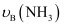 表示从反应开始至达到平衡状态A、B时的化学反应速率,则
表示从反应开始至达到平衡状态A、B时的化学反应速率,则 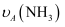 (填“>”“<”或“=”)
(填“>”“<”或“=”) 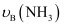 。
。②在250℃、
 时,
时,  的转化率为(结果保留三位有效数字)%。
的转化率为(结果保留三位有效数字)%。 -
(3) 温度为
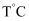 时,在
时,在 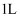 的恒容密闭容器中加入
的恒容密闭容器中加入 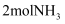 ,此时压强为
,此时压强为  ,用
,用 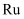 催化氨气分解,若平衡时氨气的转化率为50%,则该温度下反应
催化氨气分解,若平衡时氨气的转化率为50%,则该温度下反应 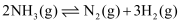 ,用平衡分压代替平衡浓度表示的化学平衡常数
,用平衡分压代替平衡浓度表示的化学平衡常数  (用含
(用含  的代数式表示)。[已知:气体分压
的代数式表示)。[已知:气体分压  气体总压
气体总压  体积分数]
体积分数]
-
(4) 液氨是一种良好的储氢物质,液氨的电离与水的电离相似:
 ,常温下
,常温下 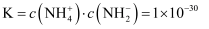 ,常温下,将一定量的金属钠投入
,常温下,将一定量的金属钠投入 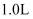 液氨中,待反应结束后,收集到标准状况下
液氨中,待反应结束后,收集到标准状况下 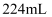 氢气。忽略溶液体积的变化,则恢复到室温时所得溶液中
氢气。忽略溶液体积的变化,则恢复到室温时所得溶液中 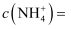
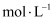 。
。
-
(5) 在一定条件下,可用
 消除
消除  污染,其反应原理为
污染,其反应原理为 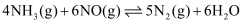 (1)
(1) 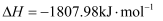 。在刚性容器中,
。在刚性容器中,  与
与  的起始物质的量之比分别为X、Y、Z(其中
的起始物质的量之比分别为X、Y、Z(其中 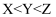 ),在相同时间内不同温度条件下,得到
),在相同时间内不同温度条件下,得到  的脱除率(即
的脱除率(即  的转化率)曲线如图所示。
的转化率)曲线如图所示。 ①
 与
与  的物质的量之比为
的物质的量之比为  时对应的曲线为(填“a”“b”或“c”)。
时对应的曲线为(填“a”“b”或“c”)。②各曲线中
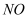 的脱除率均先升高后降低的原因为。
的脱除率均先升高后降低的原因为。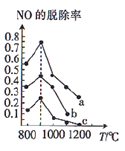
-
(1) 在实际化工生产中,为提高NH3的产率,可以采取的措施有(写两个):,。
-
(2) 氨气与酸反应得到铵盐,某(NH4)2SO4水溶液的pH=5,原因是溶液中存在平衡(用离子方程式表示),该反应对水的电离平衡起到作用(填“促进”“抑制”或“无影响”)。(NH4)2SO4溶液中的离子浓度由大到小的顺序为。
-
(3) 某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对合成NH3反应的影响。实验结果如图所示:(图中T表示温度,n表示起始时H2物质的量)
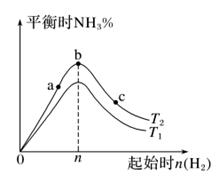
①图像中T2和T1的关系是:T2T1(填“
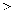 ”“
”“ 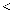 ”“
”“  ”或“无法确定”)。
”或“无法确定”)。②在a、b、c三点所处的平衡状态中,反应物N2的转化率最大的是(填字母)。
③若容器容积为2L,b点对应的n=0.15mol,测得平衡时H2、N2的转化率均为60%,则平衡时N2的物质的量浓度为 mol/L。
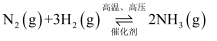
-
(1) 上述反应进行到某时刻t时,n(N2)=6.5mol,n(NH3)=3mol,Z=。
-
(2) 反应达到平衡时,混合气体的体积为358.4L(标准状况下),其中NH3的含量(体积分数)为25%n(NH3)=。
-
(3) 原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始):n(平)=。
-
(4) 原混合气体中Z:W=。
-
(5) 将1molN2和3molH2合成NH3反应时,下列叙述不能说明该反应已达到化学平衡状态的是(填序号)。
a.容器内的总压强不随时间而变化b.反应后混合气体的密度不再发生变化
c.混合气体的平均相对分子质量不再发生变化d.N2的分解速率与生成速率相等
- 2014年6月14日中央纪委获悉,中国人民政治协商会议第十二届全国委员会副主席苏荣涉嫌严重违纪违法,目前正接受组织调查。
- 属于钾肥的是()A. NH3•H2O B. KCl C. NH4Cl D. Ca3(PO4)2
- 一理想自藕变压器的原线圈接有正弦交谈电压,其最大值保持不变,副线圈接有可调电阻R,触头P与线圈始终接触良好,下列判断正
- 下图是tRNA的结构示意图,图中a端是3′端,d端是5′端,反密码子的读取方向为“3′端→5′端”。下表为四种氨基酸对应
- 根据元素周期表和元素周期律分析下面的推断,其中错误的是( ) A.砹的氢化物不稳定
- 下列图示是初中化学中常见的装置,请结合图示回答:(1)请写出仪器①的名称 。 (2)实验室用分解过氧化氢的方法制取氧气,
- 下列由地球自转产生的现象是( ) A.地球上的昼夜现象 B.地球上的昼夜交替现象
- 如图,已知⊙O的两条弦AC,BD相交于点E,∠A=75o,∠C=45o,那么sin∠AEB的值为() A.
- 如图所示,质量M=3.0kg的平板小车静止在光滑水平面上,当t=0时,两个质量均为m=1.0kg的小物体A和B(均可视为
- 为建设“四个襄阳”,加快建设现代化区域中心城市提供强大的精神动力和文化支撑,襄阳市委、市政府决定从今年开始,在每年4月份
- 下图是上海市内苏州河沿岸土地利用类型及其河流水质的变化趋势图(水污染综合指数高表示污染严重),读图完成第4题。4、关于苏
- 右图是某商品的需求曲线(P表示商品价格,Q表示商品需求量)。依据这一图示商品生产者应该
- 在2007年11月5日前后,嫦娥一号进入奔月旅程的最关键时刻――实施首次“刹车”减速。如图所示,在接近月球时,嫦娥一号将
- (本小题满分16分)(1)分解因式①②(2)计算(3)解方程
- 下图这件青铜器,内底有铭文120余字,主要记载了周王将一个贵族分封到宜地,并赐其土地、人口和仪仗等情况。该出土文物的主要
- 下列实验中都要用到玻璃棒,其中玻璃棒的操作相同的是 ( )A.①和②
- .已知函数的图象是折线段,其中、、, 函数()的图象与轴围成的图形的面积为.
- 下列关于细胞结构的叙述,正确的是 A.分泌消化酶的细胞中高尔基体一般比较发达 B.细胞核和细胞器都具有膜结构,均属于生物
- 如图,在△ABC中,D是BC边上的一点,E是AD的中点,过A点作BC的平行线交CE的延长线于F,且AF=BD,连接BF.
- 假设你在自己的班级就学生对校服态度问题进行了调查(survey)。下面是对部分学生调查的统计表。请参照该统计表给校报写一



