铁及其化合物的性质实验 知识点题库
用零价铁(Fe)去除水体中的硝酸盐(NO3﹣)已成为环境修复研究的热点之一.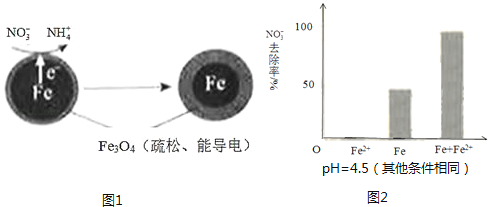
-
(1) Fe还原水体中NO3﹣的反应原理如图1所示.
①作负极的物质是.
②正极的电极反应式是.
-
(2)
将足量铁粉投入水体中,经24小时测定NO3﹣的去除率和pH,结果如下:
初始pH
pH=2.5
pH=4.5
NO3﹣的去除率
接近100%
<50%
24小时pH
接近中性
接近中性
铁的最终物质形态

pH=4.5时,NO3﹣的去除率低.其原因是 .
-
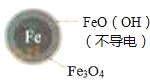
(3) 实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3﹣的去除率.对Fe2+的作用提出两种假设:
Ⅰ.Fe2+直接还原NO3﹣;
Ⅱ.Fe2+破坏FeO(OH)氧化层.
①做对比实验,结果如图2所示,可得到的结论是 .
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4 . 结合该反应的离子方程式,解释加入Fe2+提高NO3﹣去除率的原因:.
-
(4) 其他条件与(2)相同,经1小时测定NO3﹣的去除率和pH,结果如表:
初始pH
pH=2.5
pH=4.5
NO3﹣的去除率
约10%
约3%
1小时pH
接近中性
接近中性
与(2)中数据对比,解释(2)中初始pH不同时,NO3﹣去除率和铁的最终物质形态不同的原因:.
-
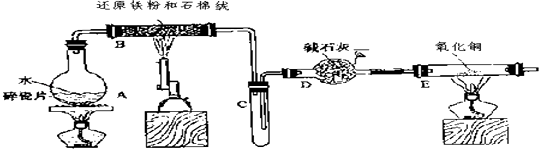
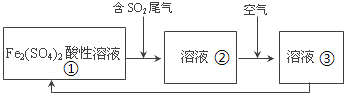
(1) 烧瓶底部放置了几片碎瓷片,
碎瓷片的作用是
装置B中发生反应的化学方程式是.
-
(2) 如果要在C处玻璃管处点燃该气体,则必须对该气体进行,
装置E中的现象是.
-
(3) 停止反应,待B管冷却后,取其中的固体,加入过量盐酸充分反应,过滤.简述检验滤液中Fe3+的操作方法.
-
(4) 该小组学生利用上述滤液制取FeCl3•6H2O晶体,设计流程如下:
滤液
 FeCl3溶液
FeCl3溶液  FeCl3•6H2O晶体
FeCl3•6H2O晶体步骤中通入Cl2的作用是.
-
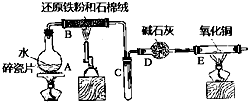
(1) 装置B中发生反应的化学方程式是.
-
(2) E中出现的现象是.
-
(3) 该小组把B中反应后的产物加入足量的盐酸,用该溶液制取FeCl3•6H2O晶体.
①欲检验溶液中含有Fe3+ , 选用的试剂为,现象是.
②该实验小组同学用上述试剂没有检测到Fe3+ , 用离子方程式解释滤液中不存在Fe3+可能的原因:.
③将此滤液中FeCl2完全氧化为FeCl3最好选择下列物质中的.
A.酸性KMnO4溶液 B.Cl2 C.Na2O2 D.FeCl3
④在③所得溶液浓缩结晶前需要用实验证明FeCl2已完全氧化,实验方法是.
实验 | 现象 | 结论 | |
A | 向2 mL 0.01mol/L的 FeCl 3溶液中加入1滴KSCN溶液,再加入足量铁粉,充分振荡 | 溶液变为红色,加入铁粉后红色褪去,变为浅绿色 | Fe3+比Fe2+的氧化性强 |
B | 将一小块金属钠放置在空气中,一段时间后,将其放置在坩埚中加热 | 钠表面变暗,加热时,钠燃烧,发出黄色火焰 | 钠易与氧气反应,加热时生成Na2O的速率加快 |
C | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 湿润的红色石蕊试纸逐渐变蓝 | NH4HCO3分解产生氨气 |
D | 向2支盛有2mL相同浓度银氨溶液的试管中,分别加入2滴相同浓度的NaCl和NaI溶液 | 一支无明显现象,另一支产生黄色沉淀 | 相同条件下,AgI比AgCl的溶解度小 |
-
(1) Ⅰ.铁不能与冷、热水反应,但能与水蒸气反应,完成实验Fe与水蒸气的反应,如图所示。
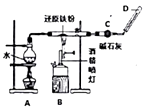
装置A的作用是;
-
(2) B中反应的化学方程式:;
-
(3) 碱石灰的作用是;
-
(4) 在D处玻璃管口点燃生成的气体前,必须对该气体进行,这一操作的目的是;
-
(5) 当有8.4g铁粉参加反应时,生成的气体在标准状况下的体积是L。
-
(6) Ⅱ.制备二氧化硫并研究其性质,如图所示。
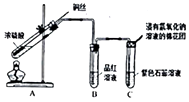
A中铜与浓硫酸反应的化学方程式是;
-
(7) B,C中的实验现象分别是、;
-
(8) 浸氢氧化钠溶液的棉花团的作用是,反应的离子方程式是。
请回答下列问题:
-
(1) 硬质试管中发生反应的化学方程式为 。
-
(2) 该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分一定有,可能有,若溶液未变红色则说明硬质试管中固体物质的成分是。
-
(3) 该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:(用离子方程式表示)。
-
(4) 该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出上述白色沉淀变成红褐色的化学方程式:
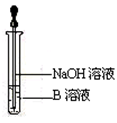
-
(5) 一段时间后,该同学发现(3)中未变红的溶液变成红色,
说明Fe2+ 具有性。由此可知,实验室中含Fe2+的盐溶液现用现配制的原因是,并且配制含Fe2+的盐溶液时应加入少量。
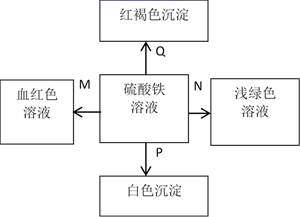
-
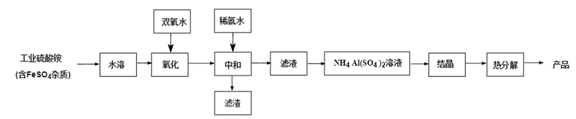
(1) “氧化”步骤发生的离子方程式为:, 使用双氧水作氧化剂优点为:。
-
(2) “热分解”得到的产物除了氧化铝外,还有 NH3、N2、SO2、SO3、H2O 生成,则氧化 产物和还原产物的物质的量之比为。
-
(3) 铵明矾晶体的化学式为NH4Al(SO4)2·12H2O,“热分解”步骤中,其各温度段内受热“失重计算值( 失重计算值(%)=
 )如表所示:
)如表所示: 温度区间(℃)
18→190
190→430
430→505
505→900
失重计算值(%)
39.20
7.80
13.00
26.00
通过上述数据经粗略计算可判断,在温度区间铵明矾基本上失去了全部结晶水。
-
(4) “结晶”步骤中常采用的操作是
-
(5) 该流程中常使用过量的工业硫酸铵,利用硫酸铵水解使溶液显酸性抑制硫酸铝水解, 这样做的目的是:。
-
(6) 通常认为金属离子浓度等于 1×10-5mol/L 即可认为沉淀完全,试计算常温下“中和”步 骤中需要调节溶液 pH=(保留一位小数,已知:Ksp[Fe(OH)3 ]=8.0×10-38 , lg5=0.7)。
-
(1) (一)铁红制备的流程图分析:
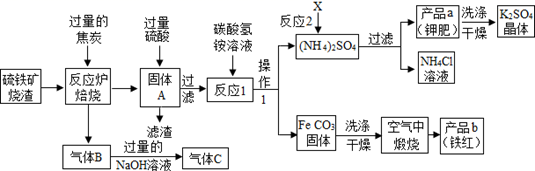
若焙烧中碳与四氧化三铁反应后B中气体的比例恰好是1:1,其化学方程式:。
-
(2) 实验室完成操作1,用到的玻璃仪器有烧杯、玻璃棒和(填仪器名称)。
-
(3) 你认为对气体C最佳的处理方法是________(填选项序号)。A . 冷却后排入空气 B . 燃烧后排放 C . 再通入反应炉
-
(4) 反应1的反应温度一般需控制在35℃以下,其目的是。
-
(5) 反应2中相关物质的溶解度如表,你认为该反应在常温下能实现的原因是:。
物质
X
K2SO4
NH4Cl
(NH4)2SO4
溶解度g(25℃)
34.0
11.1
37.2
19.2
洗涤干燥得到硫酸钾晶体时,可选用下列(选填序号,下同)洗涤剂
A.氯化钾饱和溶液B.水C.硫酸钾饱和溶液
为检验硫酸钾晶体是否洗涤干净,可取最后一次洗涤液,先加入,振荡、静置,再向上层清液中滴加,观察现象即可判断。
A.硝酸银溶液B.过量的氯化钡溶液C.过量的硝酸钡溶液
-
(6) (二)铁红的性质实验
实验装置:已知:草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为H2C2O4·3H2O
 CO2↑+CO↑+4H2O
CO2↑+CO↑+4H2O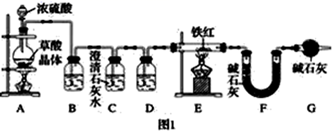
①实验前应先。
②进入E中的气体是纯净、干燥的一氧化碳,则B、D中的试剂依次是、(填字母编号)。
A.浓硫酸B.澄清的石灰水C.氢氧化钠溶液
③C装置的作用是。
已知:①K2FeO4为紫色固体,微溶于KOH溶液;
②  具有强氧化性,在酸性或中性溶液中能快速产生O2 , 在碱性溶液中较稳定。
具有强氧化性,在酸性或中性溶液中能快速产生O2 , 在碱性溶液中较稳定。
-
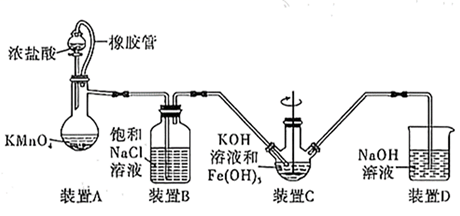
(1) 制备K2FeO4(夹持装置咯)
①如图所示,A为氯气发生装置,装置A中盛放KMnO4的仪器名称是。
②装置C中的KOH溶液需过量,目的是。
③C中得到紫色固体和溶液,则C中Cl2与Fe(OH)3发生反应生成K2FeO4的离子方程式为 ,此外Cl2还与过量的KOH反应。
-
(2) 探究K2FeO4的性质
甲同学取装置C中紫色溶液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl2。该现象不能证明“酸性条件下
 氧化性强于Cl2”,其理由是:。
氧化性强于Cl2”,其理由是:。 -
(3) 测定K2FeO4的产率
若在制备装置C中加入Fe(OH)3的质量为10.7g,充分反应后经过滤、洗涤、干燥得K2FeO4固体10.3g,则K2FeO4的产率为(保留3位有效数值)。
 FeCl3(s)
FeCl3(s)  Fe(OH)3(s)
B . CaCl2(aq)
Fe(OH)3(s)
B . CaCl2(aq)  CaCO3(s)
CaCO3(s)  CaO(s)
C . NaHCO3(s)
CaO(s)
C . NaHCO3(s)  Na2CO3(s)
Na2CO3(s)  NaOH(s)
D . Al2O3(s)
NaOH(s)
D . Al2O3(s)  AlCl3(aq)
AlCl3(aq)  Al(OH)3 (s)
Al(OH)3 (s)
请回答:
-
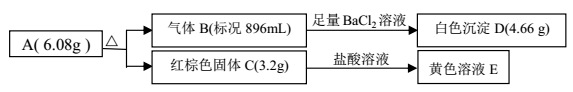
(1) 写出红棕色固体 C 的化学式。
-
(2) 写出 A 受热分解反应的化学方程式。
-
(3) 写出气体 B 与溶液 E 反应的离子方程式。
 与
与  溶液的反应,所用装置如图所示(夹持仪器已略去)。实验过程中发现B试管中溶液黄色逐渐褪去。
溶液的反应,所用装置如图所示(夹持仪器已略去)。实验过程中发现B试管中溶液黄色逐渐褪去。 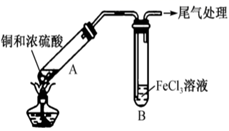
回答下列问题:
-
(1) A试管中发生反应的化学方程式为。
-
(2) 下列不能用来吸收多余
 尾气的是(填字母)。
尾气的是(填字母)。 a.NaOH溶液 b.饱和
 溶液 c.
溶液 c.  溶液
溶液 -
(3) 试管B中发生反应的离子方程式为。
-
(4) 该实验装置存在一种缺陷为:(文字叙述)。
-
(5) SO2是大污染物,空气中若含较多SO2 , 可能导致的环境问题是。
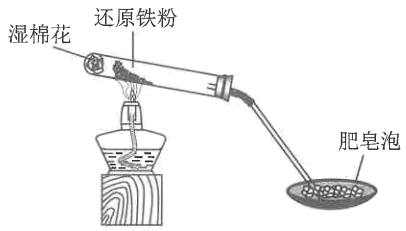
回答下列问题:
-
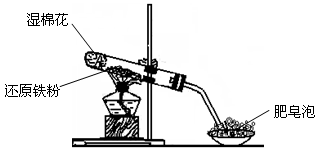
(1) 湿棉花的作用是。
-
(2) 该反应的化学方程式是。
-
(3) 利用上述反应后的固体制备无水
 , 设计流程如图所示:固体
, 设计流程如图所示:固体 滤液
滤液 ……
…… 无水FeCl3
无水FeCl3①固体和盐酸反应的化学方程式是。
②通入
 的作用是。
的作用是。③
 会腐蚀钢铁设备,除
会腐蚀钢铁设备,除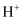 作用外,另一主要原因是(用离子方程式表示)。
作用外,另一主要原因是(用离子方程式表示)。④
 可做净水剂原因是,与处理中性废水相比,
可做净水剂原因是,与处理中性废水相比, 处理强酸性废水的效果(填“更好”“更差”或“无差别”)。
处理强酸性废水的效果(填“更好”“更差”或“无差别”)。
-
(1) 硫酸铁可用于电化浸出黄铜矿精矿工艺,其中有一主要反应:
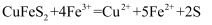 (
(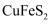 中
中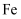 为+2价)。下列说法正确的是____(填标号)
A . 从物质分类的角度看,黄铜矿属于合金 B .
为+2价)。下列说法正确的是____(填标号)
A . 从物质分类的角度看,黄铜矿属于合金 B . 和S是氧化产物
C . 当转移
和S是氧化产物
C . 当转移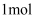 电子时,有
电子时,有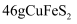 参加反应
D . 反应中,
参加反应
D . 反应中,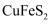 既作氧化剂又作还原剂
既作氧化剂又作还原剂
-
(2) 某小组按照如图步骤从含
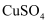 、
、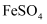 、
、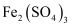 的废液中回收金属铜,并重新获得
的废液中回收金属铜,并重新获得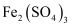 溶液:
溶液: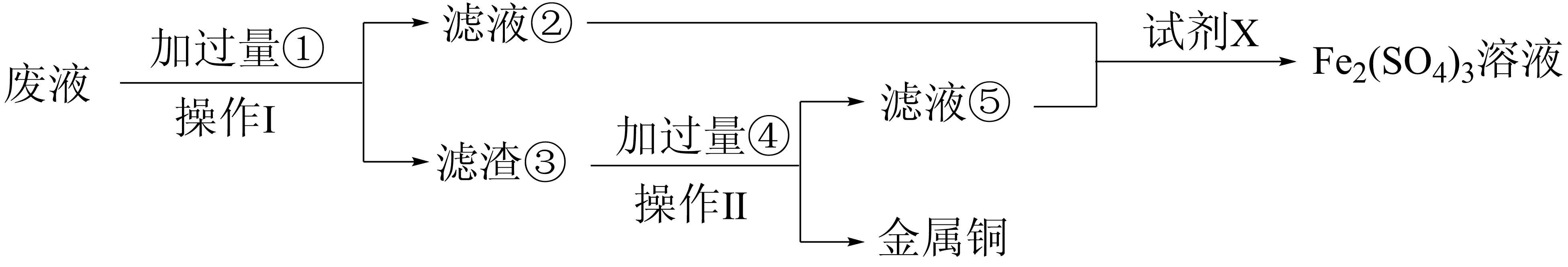
操作Ⅰ的名称为,滤渣③的主要成分为(填化学式),试剂X常用
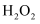 而不用稀硝酸,其原因为。
而不用稀硝酸,其原因为。 -
(3) 实验室里保存
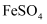 溶液时,常在溶液中加入,其目的为。
溶液时,常在溶液中加入,其目的为。
-
(4) 实验室配制
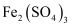 溶液时,为了防止
溶液时,为了防止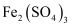 水解,需要将
水解,需要将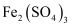 溶于稀硫酸中,再加水稀释。现需配制
溶于稀硫酸中,再加水稀释。现需配制 溶液,需要用托盘天平称量
溶液,需要用托盘天平称量 晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要;如果配制时,俯视定容,那么所配溶液的浓度(填“偏大”、“偏小”或“无影响”)。
晶体,配制该溶液所需玻璃仪器除了烧杯、玻璃棒、量筒外,还需要;如果配制时,俯视定容,那么所配溶液的浓度(填“偏大”、“偏小”或“无影响”)。
- 西北地区气候干旱的主要原因是( ) A、距海较远 B、温度较高 C、纬度较高
- 氯气是有毒气体,曾被德国法西斯制成毒气弹用于侵略战争。当这种毒气弹顺风爆炸时,通常可选用的防御方法是( ) ①人躲到低
- (2011·海南五校联考)补写出下列名篇名句中的空缺部分。 (1)____________,____________。
- It to drive after drinking wine. A.is allowed
- 在细胞生命活动中,小可能发生的过程是( ) A.神经递质山突触小泡分泌到胞外 B.mRNA
- 读我国油料、糖料作物分布图,回答下列问题:(1)图例中A、B、C、D分别代表的经济作物是:A_______、B_____
- 列关于经济技术开发区的表述,不正确的是()A.学习先进管理经验的场所B.以高新技术产业为主 C.具有劳动密集型的特
- 下列关于秦朝历史的评述,哪一项是不正确的( ) A.秦朝是我国历史上第一个统一的多民族的中央集权国家 B.秦朝在地方上推
- 生物分类的单位中,最基本的单位是 ( ) A、门 B、纲 C
- 阅读下面的文言文,完成各题。 梓人传 柳宗元 裴封叔之第,在光德里。有梓人款其门,愿佣隙宇而处焉。所职寻引、规矩、绳墨,
- 据下图所示,回答:(10分)(1)菜豆种子的主要部分是[ ]_______________________。(2)菜
- 甲烷燃料电池(电解质溶液是KOH溶液)的总反应为: CH4+2KOH+2O2 = K2CO3 + 3H2O。 下列有关的
- 图中a为纬线,M是晨线与该纬线的交点。读图完成下列各题。若6月22日,M点不存在,则a纬线度数可能是 (
- 某电脑公司经销甲种型号电脑,今年三月份的电脑售价比去年同期每台降价1000元,如果卖出相同数量的电脑,去年销售额为10万
- 21.1978年家庭联产承包责任制推行后,我国农业产量迅速增加。而在1953年我国从个体生产变成集体生产时,农业生产率也
- 人体安全电压不高于36V,当通过人体的电流接近 30 mA时就会有生命危险.据此可以推断,人体是 (
- 西汉选拔政府官员的主要方法是
- 阅读下面的文字,完成下题。(9分,每小题3分) 彩色头发基因技术 你能想象一只绿色老鼠的样子吗?科学家最近通过基
- 地中海沿岸属于( )A.冬季多雨区 B.夏季
- 有机化合物A和B由碳、氢、氧中的两种或三种元素组成,等物质的量的A和B完全燃烧时,消耗相等物质的量的氧气,则A和B的相对



