铁的氧化物和氢氧化物 知识点题库
①铁能被磁铁吸引,但纯铁易锈蚀 ②在人体的血红蛋白中含有铁元素③铁是地壳中含量最高的金属 ④铁能在氧气中剧烈燃烧,但不能在水蒸气中反应 ⑤能通过化合反应生成FeCl3和Fe(OH)3
Fe2+  Fe3+
Fe3+  FeO42﹣(高铁酸根离子)
FeO42﹣(高铁酸根离子)
请回答下列有关问题:
-
(1) Fe与过量稀盐酸反应可以制取FeCl2 , 若用反应所得的酸性溶液,实现上述①的转化,要求产物纯净,可选用的试剂是(选填序号);
a.KMnO4 b.HNO3 c.H2O2
-
(2) 硫酸铁可用于电化浸出黄铜矿精矿工艺,精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+═Cu2++5Fe2++2S(CuFeS2中S为﹣2价)则下列说法正确的是(选填序号);
a.从物质分类的角度看,黄铜矿属于合金
b.Cu2+和S是氧化产物
c.当转移1mol电子时,46gCuFeS2参加反应
d.反应中,CuFeS2既作氧化剂又作还原剂
-
(3) 在FeCl3、CuCl2混合溶液中,加入一定量的铁屑,反应完全后将固体滤出.
①若滤出的固体中只有铜,则溶液中一定含有的阳离子是,一定不含的阳离子是.
②若滤出的固体中含有铁和铜,则溶液中一定不含的阳离子是.
-
(4) 高酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,和水发生水解反应生成Fe(OH)3胶体等物质,写出FeO42﹣和H2O反应的离子方程式.高酸钾作为水处理剂发挥的作用是、.(用简洁的名词描述即可)
-
(1) 铁酸钠(Na 2FeO4)是一种新型水处理剂,它有比高锰酸钾更强的氧化性,在水中反应被还原为Fe 3+ .
①铁酸钠中铁元素的化合价为.
②铁酸钠用于水处理,除了能消毒杀菌外,还可以像明矾【KAl(SO4)2】一样起到净水作用,请说明明矾的净水原理:.(用离子方程式表示)
-
(2) 反应ⅠFe(s)+CO 2 (g)⇌FeO(s)+CO(g)△H=a kJ・mol ﹣1 , 平衡常数为K;
反应ⅡCO(g)+
 O 2 (g)=CO 2 (g)△H=b kJ・mol ﹣1 测得在不同温度下,K值如下:
O 2 (g)=CO 2 (g)△H=b kJ・mol ﹣1 测得在不同温度下,K值如下:温度/℃
500
700
900
K
1.00
1.47
2.40
①写出反应Ⅰ的K的表达式.
②反应Ⅰ中的a0(填大于、小于、等于).
③若500℃时进行反应Ⅰ,CO 2 起始浓度为2mol・L ﹣1 , CO的平衡浓度为mol・L ﹣1 .
④700℃反应Ⅰ达到平衡,要使得该平衡向右移动,其它条件不变时,可以采取的措施有(填序号).
A.缩小反应器体积 B.通入CO 2
C.升高温度到900℃D.使用合适的催化剂
⑤由反应Ⅰ和Ⅱ可求得,反应2Fe(s)+O 2(g)=2FeO(s)的△H=kJ・mol ﹣1 .
-
(3) 铁红是一种红色颜料,其成分是Fe2O3 . 将一定量的铁红溶于160mL 5mol•L﹣1盐酸中,再加入一定量铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶液中无Fe3+ , 则参加反应的铁粉的质量为g.
 SiO2
SiO2  SiCl4
B . 浓HCl
SiCl4
B . 浓HCl 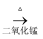 Cl2
Cl2 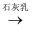 漂白粉
C . Fe
漂白粉
C . Fe 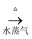 Fe2O3
Fe2O3  FeCl3
D . Mg(OH)2
FeCl3
D . Mg(OH)2  MgCl2(aq)
MgCl2(aq)  无水MgCl2
无水MgCl2
-
(1) 在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化;再向试管中通入空气,溶液逐渐变红。请解释变红的原因。
-
(2) 为测定某绿矾中结晶水含量,按下图组装好仪器并检查气密性。将石英玻璃管(带两端开关K1和K2)(设整个为装置A)称重,记为80.120g。将样品装入石英玻璃管中,再次将装置A称重,记为 107.020g。按下图连接好装置进行实验。
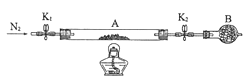
①仪器B的名称是。
②实验操作步骤为: 第一步: 打开K1和K2 , 缓缓通入N2 ;第二步:点燃酒精灯,小心加热;第三步:熄灭酒精灯 ;第四步:冷却到室温 ; 第五步:关闭K1和K2 ;第六步:称量A。 请问: 第一步缓缓通入N2 的目的是。
重复上述操作步骤,直至A恒重,记为95.320g。
③计算绿矾化学式中结晶水n=(保留一位小数)。
-
(3) 同学们查找资料可知,硫酸亚铁在高温下分解产物为Fe2O3 以及SO2和SO3。为了验证硫酸亚铁分解的气体产物,将已恒重的装置A接入下图所示的装置中,打开K1和K2 , 缓缓通入N2 , 加强热充分反应后,管中残留固体为 色粉末。
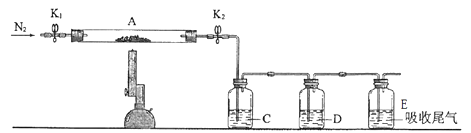
C、D中的溶液依次为 、(填标号)。
a.品红
b.NaOH
c.BaCl2
d.浓硫酸
-
(4) “严谨不仅仅是一种生活态度,更是科学精神”。检查装置气密性是化学实验中的重要操作之一,在上述32题实验装置气密性检查的操作是。
-
(1) SO2和O2反应制取SO3的反应原理为:2SO2+O2
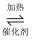 2SO3 , 经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L·s)
2SO3 , 经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L·s)
① 则这段时间为s。
② 该反应达到平衡状态的标志是。
A.容器内硫元素物质的量分数不变
B.混合物的平均相对分子质量不变
C.n(SO2):n(O2):n(SO3)=2:1:2
D.各组分的体积分数不变
-
(2) 利用烧渣制绿矾的过程如下:
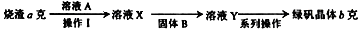
操作I的名称,溶液A的溶质,固体B是。
-
(3) 某科研机构用NaOH溶液吸收废气中的SO2 , 将所得的Na2SO4溶液进行电解,可循环再生NaOH,同时得到H2SO4 , 其原理如图所示,(电极材料为石墨)
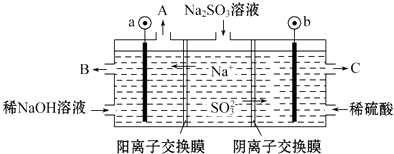
① 图中b极要连接电源的极(填“正”或“负” )
②SO32-放电的电极反应式为。
③ 若用甲烷-空气燃料电池作电源,处理标准状况下40m3的废气(其中SO2的体积分数为0.2 ) ,理论上需要消耗标准状况下甲烷m3。
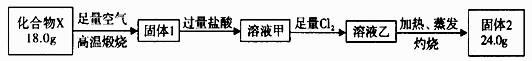
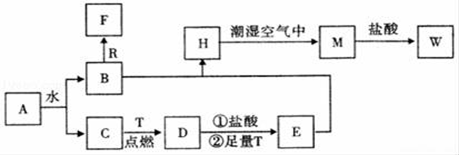
-
(1) 物质A的化学式为,D化学式为,W的化学式为;
-
(2) B与R反应生成F的离子反应式为;
-
(3) A与CO2反应的化学反应方程式为;
-
(4) H转化为M的化学反应方程式为;
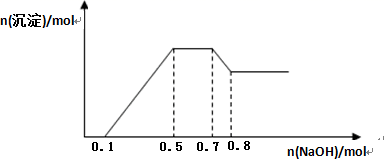
-
(1) I.现有下列10种物质①熔融的氢氧化钠 ②蔗糖 ③纯净的盐酸 ④金属钠 ⑤硫酸 ⑥二氧化硫 ⑦硫粉 ⑧石膏(CaSO4·2 H2O) ⑨酒精溶液 ⑩液氨
属于电解质的有。
-
(2) 属于非电解质的有。
-
(3) 上述状态下能导电的有。
-
(4) 上述状态下的电解质不能导电的有。
-
(5) II.Fe(OH)2长时间露置于空气中发生变化的化学方程式为:。
偏铝酸钠溶液中通入足量二氧化碳反应的离子方程式为:。
-
(6) III.高纯度单晶硅可以按下列方法制备:
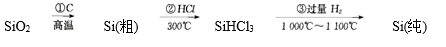
写出步骤①的化学方程式。
步骤②的产物经过冷凝后得到的SiHCl3(沸点33.0℃)中含有少量的SiCl4(沸点57.6℃),提纯SiHCl3主要操作的名称是。
A.NaHCO3 B.Na2CO3 C.Fe2O3 D.Ca(ClO)2 E. KAl(SO4)2·12H2O
-
(1) 俗称铁红的物质;
-
(2) 漂白粉的有效成分;
-
(3) 一种常见净水剂;
-
(4) 常用于焙制糕点的小苏打;
-
(5) 制普通玻璃的原料是石英、石灰石和。
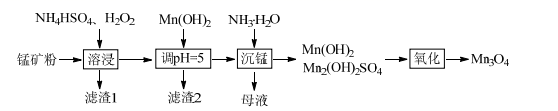
已知:(NH4)2SO4 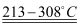 NH3↑+NH4HSO4
NH3↑+NH4HSO4
回答下列问题:
-
(1) MnOOH中Mn的化合价为。
-
(2) “溶浸”中H2O2的作用是。
-
(3) “滤渣2”的主要成分有。
-
(4) “母液”溶质的主要成分是,循环利用该物质的方案是。
-
(5) 氧化”时,将固体加入水中,70℃水浴加热,通空气氧化,将固体全部转化为Mn3O4。Mn(OH)2生成Mn3O4的化学方程式为。反应后溶液pH(填“增大”、“减小”或“不变”)。
-
(1) 某FeO、Fe2O3混合物中,铁、氧的物质的量之比4∶5,其中Fe2+与Fe3+物质的量之比为。
-
(2) 当催化剂中Fe2+与Fe3+的物质的量之比为1∶2时,其催化剂活性最高,此时混合物中铁的质量分数为(保留2位小数)。
-
(3) 写出由C(炭粉)与Fe2O3在高温下反应制备α铁触媒的化学方程式(另一种产物可溶于水)。
-
(4) 为制得这种活性最高的催化剂,理论上应向480 g Fe2O3粉末加入炭粉的质量为,生成实验条件下CO2的体积为(假设此实验条件下,气体摩尔体积为24 L·mol-1)。
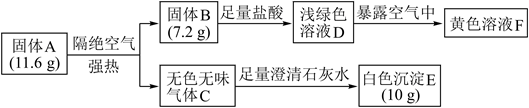
-
(1) A的化学式为。
-
(2) D溶液暴露在空气中颜色逐渐变黄,写出该过程的离子方程式。
-
(3) 设计一个实验方案验证溶液D中的金属阳离子。
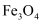 和
和 B .
B . 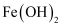 在空气中充分灼烧得到FeO
C . FeO是一种黑色粉末,不稳定,在空气中受热,迅速转化成红棕色粉末
D . 过量铁与氯气或者稀盐酸反应均可制得
在空气中充分灼烧得到FeO
C . FeO是一种黑色粉末,不稳定,在空气中受热,迅速转化成红棕色粉末
D . 过量铁与氯气或者稀盐酸反应均可制得
- 下列属于免疫预防和免疫治疗的分别是() A.注射胸腺素,口服抗体 B.注射卡介苗,输入抗体 C.注射麻疹疫苗,口服
- 已知集合,且,则实数的取值范围是 A. B. C. D.
- .如图所示,能承受最大拉力为10 N的细线OA与竖直方向成45°角,能承受最大拉力为5 N的细线OB水平,细线OC能承受
- “嫦娥一号”是我国自主研制、发射的第一个月球探测器,2007年10月24日搭载着我国首颗探月卫星嫦娥一号的长征三号甲运
- 小明学习滑动变阻器的知识后,决定将自己的台灯改为调光式,于是他买了“1W 2kΩ”的电位器一个,装在了台灯(灯泡为“PZ
- 对某班50人进行智力测验,其得分如下:48 64 52 86 71 48 64 41 86 7971
- 图为“江苏省三大产业产值比重变化统计图”。读图完成下列各题。改革开放以来,江苏省三大产业产值比重变化幅度由大到小排列的是
- 在学习了中国古代政治制度相关知识后,假设甲、乙、丙、丁四位同学回到商周时代,请判断哪一位同学不可能被周武王封为诸侯王(
- 下图是用显微镜观察植物细胞的叶绿体和细胞质流动实验中的两个视野。要把视野中的物像从甲图转为乙图,下列操作步骤正确的是
- 右图是成熟植物细胞结构示意图。请根据图回答问题:(1)对细胞有保护和支持作用的结构是[①] 。(2)水稻
- 等质量的H2S和PH3所含的粒子数不同的是( )A.分子数 B.原子数 C.质子数
- 下列加点词注音有误的一项是 A.长歌当哭(dàng) 尽管(jǐn ) 颤栗(zhàn)
- 咸丰十一年(1861)初,奕訢上疏奏陈:“臣等就今日之势论之:发捻交乘,心腹之害也;俄国壤地相接,有蚕食上国之志,肘腋之
- 不同的历史时期,形成不同的历史话语。在人类科技发展的历程中,先后出现了下列科技词语,按时间顺序排列为 ①电子计算机 ②
- 某物理学习小组的同学在研究性学习过程中,通过一块电压表和一块多用电表的欧姆挡接成电路就能一次性既能测出电压表的内阻又能测
- 阅读下面一诗,回答其后问题。蒹葭(节选)蒹葭苍苍,白露为霜。所谓伊人,在水一方。溯洄从之,道阻其长。溯游从之,宛在水中央
- I’vefinally finished my paper and it me anentire month
- 已知函数f(x)是(0,+∞)上的减函数,则f(a2-a+1)与f()的大小关系是__________.
- 亚欧板块和印度板块相碰撞形成了: A、阿尔卑斯山脉 B、喜马拉雅山脉 C、马里亚纳海沟 D、 日本群岛
- (16分)一对平行金属板水平放置,板间距离为d,板间有磁感应强度为B的水平向里的匀强磁场,将金属板连入如图所示的电路,已



