电离方程式的书写 知识点题库
下列电离方程式正确的是
A . H2S 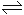 2H+ + S2-
B . HF = H+ + F-
C . NaHSO3 = Na+ + H+ +SO32-
D . H2CO3+ H2O
2H+ + S2-
B . HF = H+ + F-
C . NaHSO3 = Na+ + H+ +SO32-
D . H2CO3+ H2O H3O+ + HCO3-
H3O+ + HCO3-
 2H+ + S2-
B . HF = H+ + F-
C . NaHSO3 = Na+ + H+ +SO32-
D . H2CO3+ H2O
2H+ + S2-
B . HF = H+ + F-
C . NaHSO3 = Na+ + H+ +SO32-
D . H2CO3+ H2O H3O+ + HCO3-
H3O+ + HCO3-
化学用语是学习化学的工具和基础.下列有关化学用语的使用正确的是( )
A . 食醋呈酸性的原因是:CH3COOH+H2O=CH3COO﹣+H3O+
B . 纯碱溶液呈碱性的原因是:CO32﹣+2H2O⇌H2CO3+2OH﹣
C . 用铁作阳极,电解饱和食盐水的离子方程式:Fe+2H2O  Fe(OH)2+H2↑
D . 表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H=﹣571.6KJ•mol﹣1
Fe(OH)2+H2↑
D . 表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H=﹣571.6KJ•mol﹣1
 Fe(OH)2+H2↑
D . 表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H=﹣571.6KJ•mol﹣1
Fe(OH)2+H2↑
D . 表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H=﹣571.6KJ•mol﹣1
下列电离方程式中,不正确的是( )
A . Ba(OH)2⇌Ba2++2OH﹣
B . NH3•H2O⇌NH  +OH﹣
C . CH3COOH⇌CH3COO﹣+H+
D . AgCl=Ag++Cl﹣
+OH﹣
C . CH3COOH⇌CH3COO﹣+H+
D . AgCl=Ag++Cl﹣
 +OH﹣
C . CH3COOH⇌CH3COO﹣+H+
D . AgCl=Ag++Cl﹣
+OH﹣
C . CH3COOH⇌CH3COO﹣+H+
D . AgCl=Ag++Cl﹣
水溶液中下列电离方程式书写正确的是( )
A . Ca(OH)2⇌Ca2++2OH﹣
B . NaHCO3═Na++H++CO32﹣
C . H2CO3⇌2H++CO32﹣
D . Na2SO4═2Na++SO42﹣
按要求完成下列各题:
①Na2SO4在水溶液中的电离方程式:
②NaHCO3在水溶液中的电离方程式:
③硫酸和氢氧化钡溶液反应的离子方程式:.
下列电离方程式中,书写错误的是( )
A . Ca(OH)2=Ca2++2OH﹣
B . NaOH=Na++O2﹣+H+
C . HCl=H++Cl﹣
D . K2SO4=2K++SO42﹣
净水剂能够改善水质,给人们的生活、健康带来很大的益处。
-
(1) 明矾[KAl(SO4)2·12H2O]是常见的净水剂。其在水中的电离方程式为;明矾可净水是因为在天然水中生成胶状Al(OH)3 , Al(OH)3具有的作用。
-
(2) 碱式氯化铝(简称BAC)是高效净水剂的主要成分。实验室模拟利用铝土矿(主要含Al2O3 , 还含少量Fe2O3及其他不溶杂质)制取碱式氯化铝[Al2(OH)nCl6-n]的过程如下:
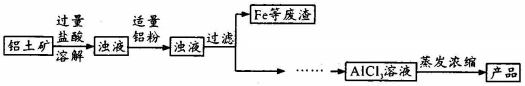
①盐酸溶解铝土矿过程中,发生反应的离子方程式为、;溶解过程中需不断搅拌,目的是。
②加适量铝粉的主要作用是。
③蒸发浓缩所需玻璃仪器为。
按要求填写下列各空白
-
(1) Ⅰ.写出下列物质的电离方程式
MgCl2 。
-
(2) Fe2(SO4)3 。
-
(3) Na2CO3 。
-
(4) Ⅱ写出下列反应的离子方程式
氢氧化钡溶液和稀硫酸 。
-
(5) 铝与盐酸 。
下列物质在水中的电离方程式正确的是( )
A . NaHSO4=Na++HSO4-
B . K2CO3=2K++  C . KClO3=K++Cl-+3O2-
D . Al2(SO4)3=2Al3++
C . KClO3=K++Cl-+3O2-
D . Al2(SO4)3=2Al3++ 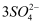
 C . KClO3=K++Cl-+3O2-
D . Al2(SO4)3=2Al3++
C . KClO3=K++Cl-+3O2-
D . Al2(SO4)3=2Al3++ 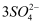
以下说法中错误的是( )
A . 物质的量的单位是摩尔
B . 三角洲的形成与胶体的性质有关
C . KHSO4在水溶液中的电离方程式为KHSO4 = K+ + H+ + SO42-
D . 氯化钠水溶液在电流的作用下电离出Na+和Cl-
下列电离方程式错误的是( )
①NaHCO3= Na++H++ CO32- ② NaHSO4 = Na++H++ SO42-
③H2SO4 = 2H++ SO42- ④KClO3 = K++ Cl++3O2-
A . ①②
B . ①
C . ①④
D . ③④
下列有关化学用语表示正确的是( )
A . 过氧化氢的电子式: 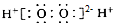 B . 质子数为16、中子数为17的硫原子:
B . 质子数为16、中子数为17的硫原子: 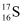 C . NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-
D . 乙烯的结构简式:CH2==CH2
C . NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-
D . 乙烯的结构简式:CH2==CH2
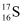 C . NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-
D . 乙烯的结构简式:CH2==CH2
C . NaHCO3在水中的电离方程式:NaHCO3=Na++H++CO32-
D . 乙烯的结构简式:CH2==CH2
-
(1) 按要求写出方程式:
①HNO3(电离方程式) 。
②Fe2(SO4)3(电离方程式) 。
③硫酸钠和氯化钡溶液反应(离子方程式) 。
④二氧化碳通入足量氢氧化钠溶液(离子方程式)。
-
(2) 以下为中学化学中常见的几种物质:①二氧化碳 ②熔融KCl ③NaHSO4固体 ④铜 ⑤稀硫酸 ⑥澄清石灰水,其中属于电解质的有,属于非电解质的有(填序号)。
某酸HX是一元弱酸,25℃时的电离平衡常数K a= 4.0×10-8。
-
(1) 写出该酸的电离方程式,其电离平衡常数表达式K a =。
-
(2) 25℃时,向1 mol·L-1 HX 溶液中加入1 mol·L-1 盐酸,会(“抑制”或“促进”)HX的电离,c(H+)(填“增大”、“减小”或“不变”), 电离平衡常数K a (填“增大”、“减小”或“不变”)。
-
(3) 25℃时,若HX的起始浓度为0.01 mol·L-1 , 则平衡时c(H+)=mol/L, 由水电离的出的c(H+)=mol/L。
下列物质在水中的电离方程式书写正确的是( )
A . H2CO3  2H++CO32-
B . Al(OH)3=Al3+ +3OH-
C . NH3·H2O
2H++CO32-
B . Al(OH)3=Al3+ +3OH-
C . NH3·H2O  NH4+ +OH-
D . NaHSO4=Na++HSO4-
NH4+ +OH-
D . NaHSO4=Na++HSO4-
 2H++CO32-
B . Al(OH)3=Al3+ +3OH-
C . NH3·H2O
2H++CO32-
B . Al(OH)3=Al3+ +3OH-
C . NH3·H2O  NH4+ +OH-
D . NaHSO4=Na++HSO4-
NH4+ +OH-
D . NaHSO4=Na++HSO4-
下列物质在水中的电离方程式书写错误的是( )
A . H2SO4=  +
+  B . KCl=K++Cl-
C . Na2SO4=2Na++
B . KCl=K++Cl-
C . Na2SO4=2Na++  D . Ca(OH)2=Ca2++2OH-
D . Ca(OH)2=Ca2++2OH-
 +
+  B . KCl=K++Cl-
C . Na2SO4=2Na++
B . KCl=K++Cl-
C . Na2SO4=2Na++  D . Ca(OH)2=Ca2++2OH-
D . Ca(OH)2=Ca2++2OH-
下表中对应关系错误的是( )
| A | NaCl=Na++Cl-; NH3·H2O | 均属于电离方程式 |
| B | Ba2++SO HCO | 均可表示一类反应 |
| C | SO2使酸性高锰酸钾溶液褪色; SO2使碱性酚酞溶液褪色 | 均利用SO2的同一性质 |
| D | Cl2+2NaOH=NaCl+NaClO+H2O; 3S+6NaOH=2Na2S+Na2SO3+3H2O | Cl2和S在反应中既作氧化剂又作还原剂 |
A . A
B . B
C . C
D . D
下列方程式不正确的是( )
A . 乙烯与溴水化学方程式: 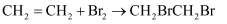 B . 乙醇在铜催化下氧化:
B . 乙醇在铜催化下氧化: 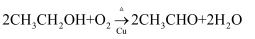 C . 氯化铵水解的离子方程式:
C . 氯化铵水解的离子方程式: 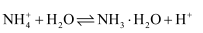 D . 碳酸氢钠在水中的电离方程式:
D . 碳酸氢钠在水中的电离方程式: 
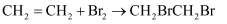 B . 乙醇在铜催化下氧化:
B . 乙醇在铜催化下氧化: 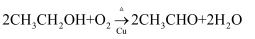 C . 氯化铵水解的离子方程式:
C . 氯化铵水解的离子方程式: 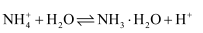 D . 碳酸氢钠在水中的电离方程式:
D . 碳酸氢钠在水中的电离方程式: 
下列指定化学用语正确的是( )
A . NaHCO3水解的离子方程式:HCO3-+H2O = CO32-+H3O+
B . Ba(OH)2的电离方程式:Ba(OH)2  Ba2++2OH-
C . NaHSO4在水中的电离方程式:NaHSO4= Na++H++SO42-
D . Na2S水解的离子方程式:S2-+2H2O = H2S+2OH-
Ba2++2OH-
C . NaHSO4在水中的电离方程式:NaHSO4= Na++H++SO42-
D . Na2S水解的离子方程式:S2-+2H2O = H2S+2OH-
 Ba2++2OH-
C . NaHSO4在水中的电离方程式:NaHSO4= Na++H++SO42-
D . Na2S水解的离子方程式:S2-+2H2O = H2S+2OH-
Ba2++2OH-
C . NaHSO4在水中的电离方程式:NaHSO4= Na++H++SO42-
D . Na2S水解的离子方程式:S2-+2H2O = H2S+2OH-
下列物质在水溶液中的电离方程式书写正确的是( )
A . Ca(OH)2=Ca2++(OH)  B . Na2CO3=Na
B . Na2CO3=Na 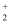 +CO
+CO  C . KAl(SO4)2=K++Al3++2SO
C . KAl(SO4)2=K++Al3++2SO  D . Al2(SO4)3=2Al2++3SO
D . Al2(SO4)3=2Al2++3SO 
 B . Na2CO3=Na
B . Na2CO3=Na 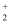 +CO
+CO  C . KAl(SO4)2=K++Al3++2SO
C . KAl(SO4)2=K++Al3++2SO  D . Al2(SO4)3=2Al2++3SO
D . Al2(SO4)3=2Al2++3SO 
最近更新
- 25. The article is too long, please cut _____ some unimporta
- 已知:如图,AD=BC,AC=BD.求证:OD=OC
- 比较过氧化氢在不同条件下的分解实验中,滴入过氧化氢酶的试管内:( ) A.产生的气泡多,燃烧得不猛烈
- Someonewho lacks staying power and perseverance is unlikely
- 已知函数 恰有两个零点,则实数 的取值范围是( )A .B .C .( 0 , 1 )D .( 0 , 1]
- 下面关于“2”的含义的解释中,正确的是 ( ) A Zn2+中的“2+”表示
- 在用显微镜观察人的口腔上皮细胞的实验中,下列说法正确的是 ( )A.制作临时装片时要在载玻片的中央滴一滴清水B.盖
- 全国动漫企业座谈会指出,动漫产业的发展关键靠创意,动漫创作者要立足于我国极为丰厚的民族传统文化资源和生活实践,创作出为人
- 下述说法正确的是:( ) A.根据E = F/q,可知电场中某点的场强与电场力成正比。 B.根据E = kQ/
- 细胞核是细胞结构中最重要的部分之一,有关细胞核的叙述错误的是 A.细胞核是细胞这一生命系统的控制中心 B.人和其他哺乳动
- 我国下列科技成就出现的先后顺序是 ①第一颗原子弹爆炸成功 ②第一颗人造地球卫星发射成功 ③中国自行设计的第一枚火箭发射成
- 根据拼音填写下文中空缺的汉字。(2分) 作为时代青年,任何情形都阻è ▲ 不了我们前行的步伐,无论是月明风qīng ▲
- 古代许多杰出人物都留下了千古传诵的诗章,激励着无数的热血青年奋发有为。请你写出能激励思想和鼓舞斗志的古诗文句子:
- 一物块受到如图所示的拉力F的作用,F与水平方向的夹角为q ,若将力F分解为水平向右的分力F1和竖直向上的分力F2,则F1
- 诗词歌赋是我国传统文化瑰宝,许多诗词蕴含着生物学知识。下列诗句能体现生态系统中物质循环的是 A.人间四月芳菲尽,山寺桃花
- 下列各项中,标点符号的使用合乎规范的一项是( ) A.“生存?还是毁灭?”莎士比亚的这句名言揭示出一个最基本的哲学
- 求证:不论m为任何实数,关于x的一元二次方程x2+(4m+1)x+2m-1=0总有实数根.
- 13、林肯总统在一次内阁会议就某个问题征询意见,结果7名阁员都表示反对,但林肯在宣布会议结束时却说:“七票反对,一票赞成
- 下列四种图形中,一定是轴对称图形的有( ) ① 等腰三角形 ②等边三角形 ③ 直角三角形 ④ 等腰直
- 如图,AB为⊙O的弦,⊙O的半径为5,OC⊥AB于点D,交⊙O于点C,且CD=l,则弦AB的长是
 +OH-
+OH- =BaSO4↓;
=BaSO4↓; +OH-=CO
+OH-=CO  +H2O
+H2O


