电离方程式的书写 知识点题库
下列电离方程式正确的是( )
A . H2SO4⇌2H++SO 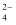 B . BaCl2═Ba2++2Cl﹣
C . NH3•H2O═NH
B . BaCl2═Ba2++2Cl﹣
C . NH3•H2O═NH  +OH﹣
D . Na2CO3═Na++CO
+OH﹣
D . Na2CO3═Na++CO 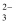
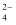 B . BaCl2═Ba2++2Cl﹣
C . NH3•H2O═NH
B . BaCl2═Ba2++2Cl﹣
C . NH3•H2O═NH  +OH﹣
D . Na2CO3═Na++CO
+OH﹣
D . Na2CO3═Na++CO 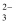
完成下列化学用语:
-
(1) 书写电离方程式:H2SO4:;NH4NO3:.
-
(2) 从电子得失角度,用双线桥法分析下列氧化还原反应中化合价变化的关系,标出电子转移的方向和数目并配平氧化还原反应式:
K2Cr2O7+HCl=KCl+CrCl3+Cl2↑+H2O
氧化剂:,被氧化的元素:;盐酸体现的性质是:.
-
(3) 工业上用电解饱和食盐水制Cl2 , 写出化学反应方程式:.
下列有关化学用语表示正确的是( )
A . Al3+的结构示意图: 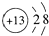 B . 甲酸甲酯的结构简式:C2H4O2
C . 醋酸的电离方程式:CH3COOH═CH3COO﹣+H+
D . 中子数为145、质子数为94的钚(Pu)原子:
B . 甲酸甲酯的结构简式:C2H4O2
C . 醋酸的电离方程式:CH3COOH═CH3COO﹣+H+
D . 中子数为145、质子数为94的钚(Pu)原子:  Pu
Pu
 Pu
Pu
联氨(又称肼,N2H4 , 无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
-
(1) 联氨分子的电子式为.
-
(2) ①2O2(g)+N2(g)=N2O4(l)△H1②N2(g)+2H2(g)=N2H4(l)△H2
③O2(g)+2H2(g)=2H2O(g)△H3
④2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H4=﹣1048.9kJ/mol
上述反应热效应之间的关系式为△H4=,联氨和N2O4可作为火箭推进剂的主要原因为.
-
(3) 联氨为二元弱碱,在水中的电离方式与氨相似,联氨第一步电离方程式为:.
下列物质在水溶液中的电离方程式正确的是( )
A . H2SO4═2H++SO42﹣
B . NaHCO3═Na++HCO3﹣
C . Na2CO3═2Na++CO32﹣
D . CH3COOH═H++CH3COO﹣
写出下列物质在水溶液中的电离方程式:
碳酸氢钠:;硫酸铝:;
氢氧化钡:;硫酸氢钾:.
下列物质溶于水,其电离方程式正确的是( )
A . NaHCO3=Na++H++CO32-
B . (NH4)2SO4= NH4++SO42-
C . NH4Cl = NH4+ + Cl-
D . Ba(OH)2 = Ba2+ + OH2-
下列电离方程式,书写正确的是( )
A . H2SO4=2H++SO42-
B . NH3·H2O=NH4++OH-
C . H2CO3=H2O+CO2↑
D . H2CO3  2H++CO32-
2H++CO32-
 2H++CO32-
2H++CO32-
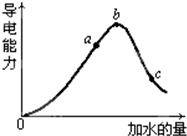
在一定温度下,冰醋酸加水稀释过程中溶液的导电能力如下图所示,请回答:
-
(1) 写出醋酸的电离方程式。
-
(2) a、b、c三点溶液中氢离子浓度由小到大的顺序为。
-
(3) a、b、c三点中醋酸的电离程度最大的是。
-
(4) 取甲、乙两份等体积c点的溶液,甲用蒸馏水稀释10倍,乙用蒸馏水稀释100倍,则稀释后甲、乙两溶液中的H+浓度:c(H+)甲10c(H+)乙(填“大于”、“小于”或“等于”)
-
(5) 醋酸与氨水反应的离子方程式:。
-
(1) 写出下列物质的电离方程式
① NaOH
② CuCl2
③ Fe2(SO4)3
-
(2) 写出与下列离子方程式相对应的化学方程式
① H+ + OH- = H2O
② 2 H+ + Ca CO3 = Ca2+ + H2O + CO2↑
③ Cu2+ + 2 OH- = Cu(OH)2↓
下列方程式书写正确的是( )
A . NaHSO4在熔融状态下的电离方程式:NaHSO4=Na++HSO4-
B . H2SO4溶液与NaOH溶液发生中和反应的热化学方程式为(已知H2SO4 溶液与NaOH溶液发生反应的中和热为57.3 kJ/mol):H2SO4(aq)+2NaOH(aq)=2H2O(l)+Na2SO4(aq) △H=-57.3kJ/mol
C . CO32-的水解方程式:CO32-+2H2O  H2CO3+2OH-
D . CaCO3的沉淀溶解平衡方程式:CaCO3(s)=Ca2+(aq)+CO32-(aq)
H2CO3+2OH-
D . CaCO3的沉淀溶解平衡方程式:CaCO3(s)=Ca2+(aq)+CO32-(aq)
 H2CO3+2OH-
D . CaCO3的沉淀溶解平衡方程式:CaCO3(s)=Ca2+(aq)+CO32-(aq)
H2CO3+2OH-
D . CaCO3的沉淀溶解平衡方程式:CaCO3(s)=Ca2+(aq)+CO32-(aq)
现有以下物质:①Cu②熔融NaCl③NaHSO4固体④NH3⑤蔗糖⑥CaO⑦盐酸,请按下列分类标准回答问题(用序号填写)。
-
(1) 能导电的是;
-
(2) 属于电解质的是,属于非电解质的是;
-
(3) 写出③在水溶液中的电离方程式;
-
(4) 向⑥中滴加⑦溶液的离子方程式为。
下列化学用语正确的是( )
A . 氢氧化铝电离:Al(OH)3=Al3++3OH-
B . 氯气溶于水:Cl2+H2O=2H++Cl-+ClO-
C . 氯气与石灰乳反应制漂白粉:2Cl2+Ca2++2OH-=2Cl-+Ca(ClO)2+2H2O
D . 向Mg(OH)2悬浊液中滴酚酞后溶液变红:Mg(OH)2(s)  Mg2+(aq)+2OH-(aq)
Mg2+(aq)+2OH-(aq)
 Mg2+(aq)+2OH-(aq)
Mg2+(aq)+2OH-(aq)
25℃时,两种常见酸的电离平衡常数如表所示。
|
Ka1 |
Ka2 |
|
|
H2SO3 |
1.3×10-2 |
6.3×10-8 |
|
H2CO3 |
4.2×10-7 |
5.6×10-11 |
-
(1) ①HCO
 的电离平衡常数表达式K=。
的电离平衡常数表达式K=。 ②SO
 、HSO
、HSO  、CO
、CO  、HCO
、HCO  结合H+的能力由强到弱的顺序为;向Na2SO3溶液中通入CO2反应的离子方程式为。
结合H+的能力由强到弱的顺序为;向Na2SO3溶液中通入CO2反应的离子方程式为。 -
(2) 已知HnA为n元弱酸。
①写出HnA与足量NaOH反应的离子方程式:。
②HnA的电离方程式为(写第一步电离)。
现有以下浓度均为0.1mol·L-1的溶液:①KNO3溶液②CH3COONa溶液③NH4Cl溶液④NaOH溶液⑤氨水⑥CH3COOH溶液⑦盐酸⑧NaHCO3溶液⑨NaHC2O4溶液;已知常温下相关电离平衡常数如表:
|
弱电解质 |
CH3COOH |
NH3•H2O |
H2CO3 |
H2C2O4 |
|
Ka或Kb |
1.8×10-5 |
1.8×10-5 |
Ka1=4.3×10-7 |
Ka1=5.6×10-2 Ka2=5.0×10-5 |
回答下列有关小题:
-
(1) 写出NaHCO3的电离方程式;列出NH
 的水解平衡常数表达式Kh(NH
的水解平衡常数表达式Kh(NH  )=,计算常温下Kh(NH
)=,计算常温下Kh(NH  )=。
)=。
-
(2) ②中各离子浓度由大到小的顺序为。
-
(3) 常温下:若将④和⑥混合,并使混合后溶液pH=7,则所需体积V④V⑥(填“>”“<”或“=”);若将④和⑦混合,并使混合后溶液pH=12,则V④:V⑦=;将④和⑦等体积混合得w溶液,⑤和⑥等体积混合得Z溶液,混合后溶液pH值WZ(填“>”、“<”或“=”,下同);
-
(4) ⑧和⑨混合如果能反应,写出离子反应方程式,如果不能反应,则该小题不填。
下列各方程式中,属于正确的电离方程式的是( )
A . HCO  +H2O
+H2O  H2CO3 + OH-
B . HCO
H2CO3 + OH-
B . HCO  +OH-=H2O + CO
+OH-=H2O + CO  C . NH3 + H+=NH
C . NH3 + H+=NH  D . H2CO3
D . H2CO3  HCO
HCO  +H+
+H+
 +H2O
+H2O  H2CO3 + OH-
B . HCO
H2CO3 + OH-
B . HCO  +OH-=H2O + CO
+OH-=H2O + CO  C . NH3 + H+=NH
C . NH3 + H+=NH  D . H2CO3
D . H2CO3  HCO
HCO  +H+
+H+
下列物质的电离方程式或水解方程式书写正确的是( )
A . HCN=H++CN-
B . 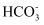 +H2O⇌H3O++
+H2O⇌H3O++ C .
C .  +2H2O⇌H2SO3+2OH-
D . Al2(SO4)3⇌2Al3++3
+2H2O⇌H2SO3+2OH-
D . Al2(SO4)3⇌2Al3++3
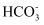 +H2O⇌H3O++
+H2O⇌H3O++ C .
C .  +2H2O⇌H2SO3+2OH-
D . Al2(SO4)3⇌2Al3++3
+2H2O⇌H2SO3+2OH-
D . Al2(SO4)3⇌2Al3++3
下列物质在水溶液中的电离方程式书写正确的是( )
A .  B .
B .  C .
C . 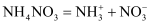 D .
D . 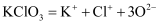
 B .
B .  C .
C . 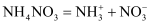 D .
D . 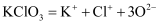
下列化学用语表示正确的是( )
A . 乙烯的结构简式:CH2CH2
B . H2O的电子式: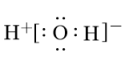 C . 氧原子的结构示意图:
C . 氧原子的结构示意图: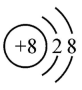 D . K2SO4的电离方程式:K2SO4=2K++SO
D . K2SO4的电离方程式:K2SO4=2K++SO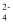
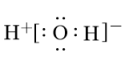 C . 氧原子的结构示意图:
C . 氧原子的结构示意图: D . K2SO4的电离方程式:K2SO4=2K++SO
D . K2SO4的电离方程式:K2SO4=2K++SO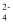
离子反应在物质分离、提纯、鉴定等方面有广泛的应用。实验室里需要纯净的氯化钠溶液,但现在只有混有硫酸钠、碳酸氢铵的氯化钠固体。某学生设计了如图方案,请回答下列问题。
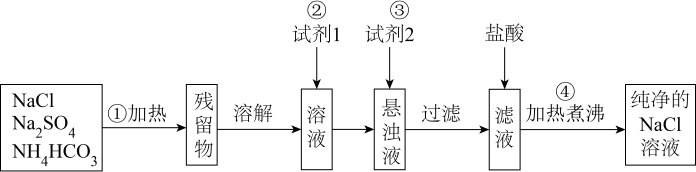
已知:操作①中发生的化学反应方程式为: ;操作②和③中,试剂1是
;操作②和③中,试剂1是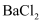 溶液,试剂2是
溶液,试剂2是 溶液,且二者均过量。
溶液,且二者均过量。
-
(1) 写出
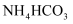 在水溶液中的电离方程式:;
在水溶液中的电离方程式:;
-
(2) 加入试剂1发生时反应的离子方程式:;
-
(3) 试剂2的目的是;
-
(4) 如何检验NaCl溶液产品中的
 ?
?
最近更新
- .下列说法中正确的是 A.不同的元素可以组成不同的物质,同种元素只能组成同一种物质B.使用无铅汽油,禁止含铅物质排放,是
- 若,,则 满足 ( ) A. B.C.D.
- 孟子云:“人不可以无耻,无耻之耻,无耻矣。”,这句古诗告诫我们①做人不可有耻辱感②不知羞耻,就永远不会有自尊③知耻就会失
- 下图是气体制取装置,下列能用此装置制取气体并能随开随用、随关随停的是()。A.大理石和稀硫酸制取二氧化碳B.锌粒和稀硫酸
- 同学们走进医务室时,常闻到酒精的气味,这一现象涉及的物理知识有 A.升华 凝华 B.汽化 扩散
- 当组成缓冲溶液的物质浓度越_________,缓冲溶液的pH(pOH)等于______时,缓冲溶液的缓冲能力越大.
- 在最崎岖的山路上点燃知识的火把,在最寂寞的悬崖边拉起孩子们求学的小手,19年的清贫、坚守和操劳,沉淀为精神的沃土,让希望
- 关于两个互成角度的初速度不为零的匀变速直线运动的合运动,下列说法正确的是
- —How about __________ Christmas evening party? —I should say
- 2012年,某县农民种植的土豆产量大增,但市场没有相应扩大,农民不得不低价销售,收入不增反降。下图的①②③④中,能够反映
- 下列说法正确的是() A. 乳酸菌与噬菌体在结构上相似 B.原核细胞和真核细胞最明显的区别在于有无核物质 C. 在你苦思
- ___but fools, in my opinion, will believe what he said. A.
- A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如下图所示。A是短周期中原子半径最小的元素,A、B、
- 计算:(-3)0-()-1+
- 下列命题中正确的是( )A.终边在y轴非负半轴上的角是直角B.第二象限角一定是钝角C.第四象限角一定是负角D.若β
- 在日常生活中,只见鸟类排出粪便,未见鸟类排出尿液的原因是( ) A.体内没有产生尿液的器官 B.体内产生的尿液经体表
- 下列各组词语中书写全都正确的一项是( ) A.仿徨 守拙 陆离 视死如归 B.樊笼
- 大蒜中含有的一种有效成分“硫化丙烯”(C3H6S),具有一定的杀菌食疗价值。下列有关C3H6S的说法正确的是( ) A
- 2013年9月27日江苏省第十届村委会换届选举正式启动,近1.6万个村委会将换届选“村官”,2900万农村选民将参与选举
- 下列哪种主张是韩非子的思想( ) A.施仁政于民 B.实行“法治” C.



