实验装置综合 知识点题库
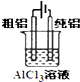 用图所示装置可以电解精炼铝
B .
用图所示装置可以电解精炼铝
B . 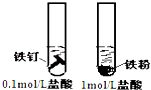 用图探究固体表面积对反应速率的影响
C .
用图探究固体表面积对反应速率的影响
C . 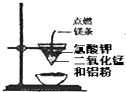 用图所示装置可以制得金属锰
D .
用图所示装置可以制得金属锰
D . 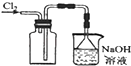 用图所示装置可以收集Cl2
用图所示装置可以收集Cl2
 CrN+3HCl。回答下列问题:
CrN+3HCl。回答下列问题:
-
(1) 制备无水氯化铬。氯化铬有很强的吸水性,通常以氯化铬晶体(CrCl3·6H2O)的形式存在。直接加热脱水往往得到Cr2O3 , 有关反应的化学方程式为。以氯化铬晶体制备无水氯化铬的方法是。
-
(2) 制备氮化铬。某实验小组设计制备氮化铬的装置如下图所示(夹持与加热装置省略):
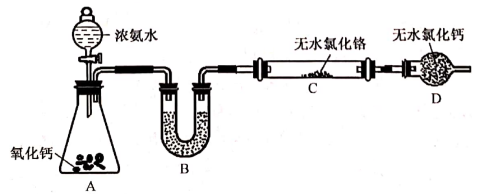
①装置A中发生反应的化学方程式为。
②实验开始时,要先打开装置A中活塞,后加热装置C,目的是。
③装置B中盛放的试剂是,装置D的作用是。
④有同学认为该装置有一个缺陷,该缺陷是。
-
(3) 氮化铬的纯度测定。制得的CrN中含有Cr2N杂质,取样品14.38g在空气中充分加热,得固体残渣(Cr2O3)的质量为16.72g,则样品中CrN与Cr2N的物质的量之比为。
-
(4) 工业上也可用Cr2O3与NH3在高温下反应制备CrN。相关反应的化学方程式为,提出一条能降低粗产品中氧含量的措施:。
(沉淀制备)
称取12.5 g胆矾溶于87.4mL蒸馏水中,滴4滴稀硫酸,充分搅拌后得到CuSO4溶液。向其中加入适量Na2CO3溶液,将所得蓝绿色悬浊液,过滤,沉淀用蒸馏水洗涤,再用无水乙醇洗涤。
-
(1) 滴加稀硫酸的作用是。所得硫酸铜溶液的溶质质量分数约为。
-
(2) 用无水乙醇洗涤的目的是。
(实验探究)同学们设计了如图装置,用制得的蓝绿色固体进行实验:
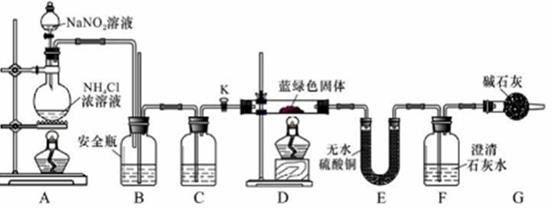
-
(3) D装置加热前,需要首先打开活塞K,用A装置制取适量N2 , 然后关闭K,点燃D处酒精灯。A中产生N2的作用是,C中盛装的试剂应是。
-
(4) 装置A中发生反应的离子方程式为。
-
(5) 若蓝绿色固体的组成为xCuCO3·yCu(OH)2 , 实验能观察到的现象是。
-
(6) 同学们查阅文献知:Ksp[CaCO3]=2.8×10-9 , Ksp[BaCO3]=5.1×10-9 , 经讨论认为需要用Ba(OH)2代替Ca(OH)2来定量测定蓝绿色固体的化学式,其原因是。(填序号)。
a.Ba(OH)2的碱性比Ca(OH)2强
b.Ba(OH)2溶解度大于Ca(OH)2 , 能充分吸收CO2
c.相同条件下,CaCO3的溶解度明显大于BaCO3
d.吸收等量CO2生成的BaCO3的质量大于CaCO3 , 测量误差小
待D中反应完全后,打开活塞K,再次滴加NaNO2溶液产生N2 , 其目的是。若所取蓝绿色固体的质量为27.1g,装置F中使用Ba(OH)2溶液,实验结束后,装置E的质量增加2.7g,F中产生沉淀19.7g。则该蓝绿色固体的化学式为。
已知:①二氧化锰与浓盐酸反应可制备氯气,同时生成MnCl2
②氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6NaOH ![]() 5NaCl+NaClO3+3H2O
5NaCl+NaClO3+3H2O
该兴趣小组设计了下列实验装置,进行实验。
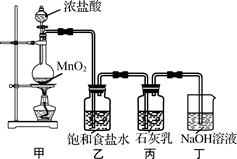
请回答下列问题:
-
(1) ①甲装置用于制备氯气,乙装置的作用是 。
②实验室用足量NaOH溶液吸收从浓盐酸和MnO2反应体系中导出的气体。当吸收温度不同时,生成的产物可能是NaClO、NaClO3、NaCl中的两种或三种。下列说法错误的是。(填字母)
A.若产物为NaClO3、NaCl,则参加反应的氧化剂和还原剂的物质的量之比为1∶5
B.若产物为NaClO、NaCl,则吸收后的溶液中n(NaClO)=n(NaCl)
C.若产物为NaClO、NaClO3、NaCl,则NaOH与Cl2相互反应的物质的量之比为2∶1
-
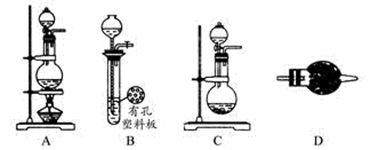
(2) 小组成员发现,产物中Ca(ClO)2的质量明显小于理论值。他们讨论后认为,其可能原因是部分氯气未与石灰乳反应而逸出,以及温度升高。为了探究反应条件对产物的影响,他们另取一定量的石灰乳,缓慢匀速地通入足量氯气,得出了Ca(ClO)2、Ca(ClO3)2两种物质的物质的量(n)与反应时间(t)的关系曲线,粗略表示为如图(不考虑氯气和水的反应)。
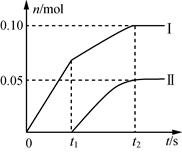
①图中曲线II表示(填物质的化学式)的物质的量随反应时间变化的关系;
②所取石灰乳中含有Ca(OH)2的物质的量为mol;
-
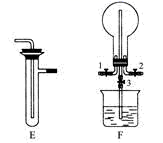
(1) Ⅰ.探究氯气与氨气的反应
为制取干燥氨气,可将装置C与(填装置名称)连接;装置C中的烧瓶内固体宜选用。
a.氯化钙 b.碱石灰 c.五氧化二磷 d.生石灰
-
(2) 装置A、E、E连接可制取纯净、干燥的氯气,则两个E装置内的药品依次是。
-
(3) 装置F可用于探究氯气与氨气的反应。实验时打开开关1、3,关闭2,先向烧瓶中通入(填名称),然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体。实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子,F的烧杯中所装液体为,所起的作用是。
-
(4) Ⅱ.探究某些物质的性质
利用装置A、E,可设计实验比较Cl-和Br-的还原性强弱。将装置A中产生的气体通入盛有NaBr溶液的装置E中,充分反应后取下E,加入CCl4 , 静置后观察到的实验现象,则证明Br-的还原性强于Cl-。
-
(5) 将装置B、C分别与F相连后,进行H2S与SO2反应的实验。简述检查装置B气密性的操作,F的烧瓶中发生反应的化学方程式为。
步骤Ⅰ用氨气与适量氯气反应制取NH4Cl
-
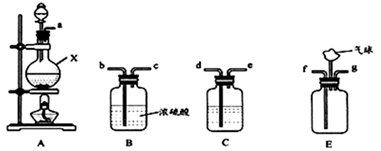
(1) 装置A中仪器X的名称为;若用浓盐酸与MnO2反应制取氯气,则该反应的离子方程式为。
-
(2) C中盛放的试剂是;要得到干燥纯净的氯气,按照气流由左到右的顺序,上述A、B、C装置连接依次为a→(用小写字母表示)。
-
(3) 氨气与适量氯气混合反应可生成NH4Cl和一种无污染的气体,利用E装置模拟该反应。氨气应从(用小写字母表示)通入,反应的化学方程式为;观察到的现象是。
-
(4) 步骤Ⅱ天然脑砂中NH4Cl含量的测定
准确称取一定质量脑砂,与足量的氧化铜混合,如图所示进行实验。
已知:2NH4Cl+3CuO
 3Cu+N2↑+2HCl↑+3H2O
3Cu+N2↑+2HCl↑+3H2O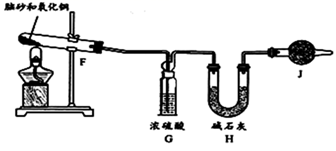
为完成NH4Cl含量的测定,请完成下列实验步骤:
加热前,称量H装置的总质量;当观察到现象时,停止加热,冷却,。
-
(5) 如果不用J装置,测出NH4Cl的含量将(填“偏高”、“偏低”或“无影响”)。
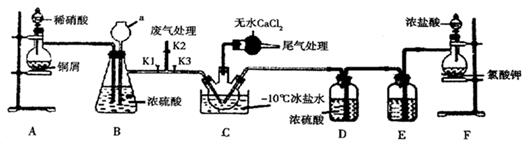
-
(1) 装置B中仪器a的名称是,装置E中的试剂为。
-
(2) 实验开始时,先打开K1、K2 , 关闭K3 , 再打开分液漏斗活塞滴入适量稀硝酸,当观察到B中时关闭K1、K2。向装置C三颈瓶中通入干燥Cl2 , 当瓶中充满黄绿色气体时,再打开K1、K3 , 制备NOCl。
-
(3) 装置B、D除可干燥NO、Cl2外,另一个作用是;若装置C中去掉盛CaCl2的干燥管,则C中NOCl可能发生反应的化学方程式为。
-
(4) 制得的NOCl中可能含有少量N2O4杂质,为测定产品纯度进行如下实验:将所得亚硝酰M(NOCl)产品13.10g溶于水,配制成250mL溶液;取出25.00mL,K2CrO4溶液为指示剂,用0.8mol•L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。(已知:Ag2CrO4为砖红色固体)
滴定时应将AgNO3标准溶液加入(填“酸式”或“碱式”)滴定管中;亚硝酰氯(NOCl)的质量分数为;若滴定开始时仰视读数,滴定终点时正确读数,则测定结果(填“偏高”“偏低”或“不变”果)。
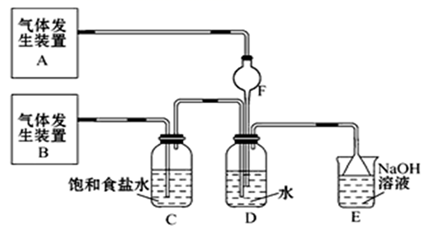
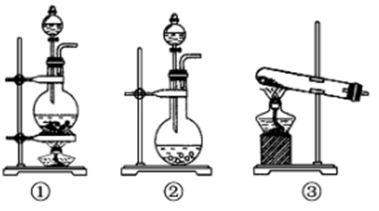
-
(1) 该化学兴趣小组的同学现采用Na2SO3与70%的硫酸为原料制取SO2 , 采用MnO2和浓盐酸(12mol/L)为原料制取Cl2,在此实验中,F仪器的作用是;气体发生装置B应选择以上三种装置中的(填序号)。
-
(2) 装置D中主要反应的离子方程式为。
-
(3) 为验证通入装置D中的气体是Cl2过量还是SO2过量,兴趣小组的同学准备了以下试剂:
①氯化铁溶液②氯化亚铁溶液③硫氰化钾溶液④品红溶液
若Cl2过量,取适量D中溶液滴加至盛有(填一个序号)的试管内,再加入(填一个序号)。产生的现象是。
若SO2过量,取适量D中溶液滴加至盛有(填一个序号)的试管内,产生的现象是。
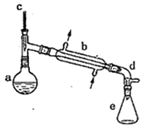
可能用到的有关数据如下:
| 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
按下列实验步骤回答问题:
-
(1) Ⅰ.产物合成:在a中加入10.0g环己醇和2片碎瓷片,冷却搅拌下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度接近90℃。
碎瓷片的作用是;
-
(2) a中发生主要反应的化学方程式为;
-
(3) 本实验最容易产生的有机副产物的结构简式为。
-
(4) Ⅱ.分离提纯:将反应粗产物倒入分液漏斗中,依次用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过操作X得到纯净的环己烯,称量,其质量为6.15g。
用碳酸钠溶液洗涤的作用是,操作X的名称为。
-
(5) Ⅲ.产物分析及产率计算:
①核磁共振氢谱可以帮助鉴定产物是否为环己烯,环己烯分子中有种不同化学环境的氢原子。
②本实验所得环己烯的产率是。
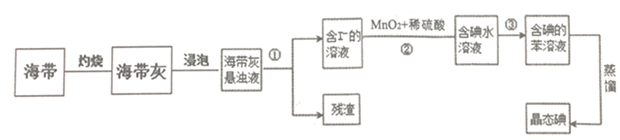
-
(1) 灼烧海带时,除需要三脚架、泥三角外,还需要用到的实验仪器是___(填字母);A . 烧杯 B . 蒸发皿 C . 坩埚 D . 试管 E . 酒精灯
-
(2) 提取碘的过程中有关的实验操作名称:①,③;
-
(3) ②对应的离子反应方程式为;
-
(4) 请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:__;
-
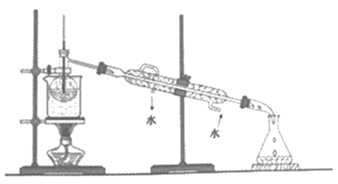
(5) 从含碘的有机落液中提取碘和回收有机溶液,还需要经过蒸馏,装置如图。使用水浴的优点是,最后晶态碘在里聚集(填仪器名称)。

 B .
B .  C .
C . 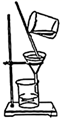 D .
D . -
(1) 向21.6g铁粉和铜粉的混合物中加入1L1mol/L硝酸溶液,充分反应,放出NO气体且金属有剩余。则反应后溶液中
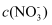 可能为。
可能为。
-
(2) 某化学兴趣小组为了探究
 、
、  同时通入
同时通入  中发生的反应,设计了如图所示的实验装置。
中发生的反应,设计了如图所示的实验装置。 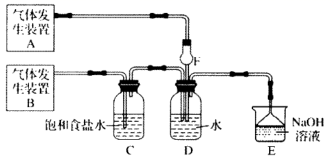
该化学兴趣小组的同学为制取
 、
、  气体,现采用
气体,现采用  与70%的硫酸为原料制取
与70%的硫酸为原料制取  ,采用
,采用  和浓盐酸(12mol/L)为原料制取
和浓盐酸(12mol/L)为原料制取  。发生装置A应选择以下三种装置中的(填序号)。装置A中发生反应的化学方程式为。D装置中主要反应的离子方程式为。
。发生装置A应选择以下三种装置中的(填序号)。装置A中发生反应的化学方程式为。D装置中主要反应的离子方程式为。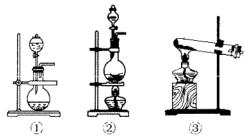
-
(3)
 和
和  具有相似的化学性质,能使酸性
具有相似的化学性质,能使酸性  溶液褪色,反应的离子方程式为。
溶液褪色,反应的离子方程式为。 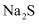 也能使酸性
也能使酸性  溶液褪色且溶液仍澄清,反应的离子方程式为。
溶液褪色且溶液仍澄清,反应的离子方程式为。
-
(4)
 用于工业制硫酸时,涉及反应的化学方程式是。
用于工业制硫酸时,涉及反应的化学方程式是。
-
(1) I.利用废铜屑制备CuCl2(实验装置如下图所示)
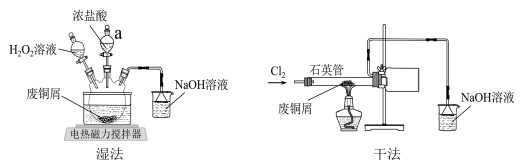
仪器a的名称为。
-
(2) “湿法”制备CuCl2的化学方程式为。
-
(3) ①石英管内可能观察到的现象为。
②石英管直接伸入收集装置,该管较粗,其优点是。
-
(4) 除上述两种方法外,实验室中还可先将铜粉(填试剂及操作),再加入适量稀盐酸反应得到CuCl2溶液。
-
(5) II.探究Al与CuCl2溶液的反应
将铝片放入盛有0.1mol·L-1CuCl2溶液的试管中,观察到现象为:铝片表面析出疏松的紫红色固体,产生无色无味气体,溶液颜色变浅。
紫红色固体为(填化学式)。
-
(6) 经检验产生的气体为H2.在CuCl2溶液中存在Cu2++2H2O=Cu(OH)2+2H+、2Al+6H+=2Al3++3H2↑,小组成员认为应产生Cu(OH)2 , 但实际实验中并未观察到蓝色沉淀。于是他们提出了以下两种猜测并进行相关验证。完成下列表格:
猜测
实验
现象
结论
i.①。
取少量Cu(OH)2悬浊液,加入打磨过的铝片,振荡
无明显现象
猜想i不成立
ii.Cu(OH)2与Al3+发生了反应
②。
固体立即溶解,溶液呈浅绿色
猜想ii成立
③在猜测ii成立的基础上,该小组成员查阅文献发现体系中可能存在反应:2Al3++3Cu(OH)2=2Al(OH)3+3Cu2+ , 列式计算平衡常数分析该反应进行的趋势。(已知:Ksp[Cu(OH)2]=2.2×10-20;Ksp[Al(OH)3]=1.3×10-33。一般认为,K>105时反应进行较完全,K<10-5时反应难以进行)文献显示生成的Al(OH)3可能以胶体形式存在,这是未观察到白色沉淀的可能原因,但仍需进一步深入研究。
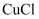 用于石油工业脱硫与脱色,是一种不溶于水和乙醇的白色粉末,在潮湿空气中可被迅速氧化。实验室用
用于石油工业脱硫与脱色,是一种不溶于水和乙醇的白色粉末,在潮湿空气中可被迅速氧化。实验室用  混合溶液与
混合溶液与  溶液反应制取
溶液反应制取 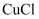 ,相关装置如图。回答以下问题:
,相关装置如图。回答以下问题: 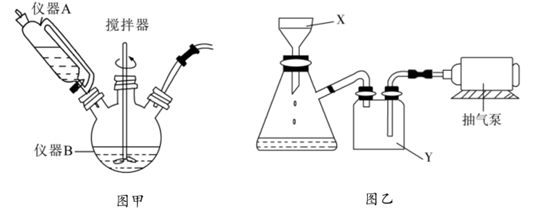
-
(1) 图甲中仪器B的名称是,制备过程中
 过量会发生副反应生成
过量会发生副反应生成  ,为提高产率,仪器A中所加试剂应为;
,为提高产率,仪器A中所加试剂应为;
-
(2) 丙图是体系pH随时间变化关系图,制取
 反应的离子方程式为,丁图是产率随pH变化关系图,实验过程中往往用
反应的离子方程式为,丁图是产率随pH变化关系图,实验过程中往往用  混合溶液代替单一
混合溶液代替单一  溶液,其中
溶液,其中  的作用是;
的作用是; 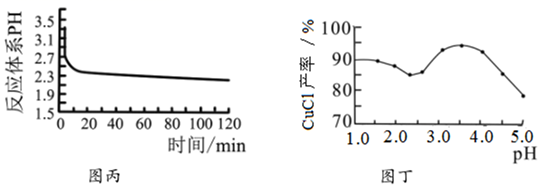
-
(3) 反应完成后经抽滤、洗涤、干燥获得产品。抽滤装置如图乙所示,抽滤所用的仪器包括布氏漏斗、吸滤瓶、安全瓶和抽气泵。其中抽气泵的作用是使吸滤瓶与安全瓶中的,跟常规过滤相比,采用抽滤的优点是(写一条);洗涤时,用“去氧水”作洗涤剂洗涤产品,作用是。
-
(4)
 不稳定易分解为
不稳定易分解为  ,
, 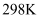 时
时 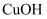 的
的 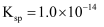 ,
, 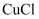 的
的 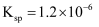 ,把
,把 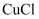 固体和
固体和  溶液混合,加热,得到红色沉淀,该沉淀的化学式为。
溶液混合,加热,得到红色沉淀,该沉淀的化学式为。
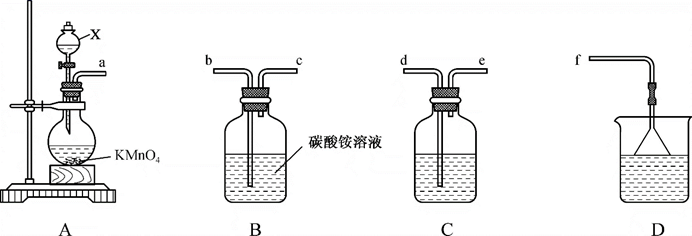
回答下列问题:
-
(1) 装置A中仪器X的名称是,盛放的试剂是,装置A中发生反应的离子方程式为。
-
(2) 整个装置的导管连接顺序为a→→→→→。
-
(3) 装置B中发生反应的化学方程式为。
-
(4) 装置C的作用为。装置D的作用为。
-
(5) 三氯化氮浓度的测定:准确量取20mL装置B中反应后的溶液,置于100mL容量瓶中,用水稀释至刻度,摇匀,吸取25.0mL于烧杯中,加入足量V1mLc1mol·L-1亚硫酸钠溶液,充分反应后,向烧杯中加入足量V2mLc2mol·L-1盐酸酸化的氯化钡溶液,得沉淀mg。
已知:i._ Na2SO3+_ NCl3 +_=_Na2SO4 +_ HCl+ _NH4Cl;
ii. BaCl2 +Na2SO4=BaSO↓+ 2HCl。
①请完成反应i的化学方程式:
②装置B反应后的溶液中三氯化氮的浓度为mol·L-1。
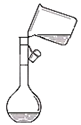 向容量瓶中转移溶液
B .
向容量瓶中转移溶液
B . 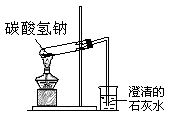 碳酸氢钠受热分解
D .
碳酸氢钠受热分解
D . 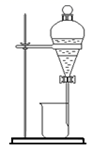 萃取、分液
萃取、分液
 。
。 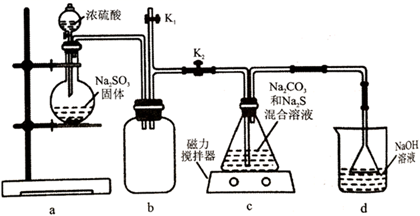
回答下列问题:
-
(1) 装置a中盛装浓
 的仪器名称是。
的仪器名称是。
-
(2) 装置b的作用是。
-
(3) 实验结束后,装置d中的溶质有NaOH、
 ,还可能有(填化学式)。
,还可能有(填化学式)。
-
(4) 装置c中反应的化学方程式为。
-
(5) 实验结束后,装置c的溶液中溶质主要是
 ,还含有
,还含有  、
、  等成分。为了证明
等成分。为了证明  的存在,设计如下实验。
的存在,设计如下实验。 供选试剂:A.品红溶液:B.酸性高锰酸钾溶液;C.
 溶液;D.澄清石灰水;E.稀硫酸
溶液;D.澄清石灰水;E.稀硫酸①取c中溶液少许,滴加足量(填试剂标号)
②将①产生的气体依次通过(填试剂标号),实验现象和结论为。
已知:ClO2常温下为黄绿色气体,11℃时液化成红棕色液体,易溶于水,ClO2溶于碱溶液生成亚氯酸盐和氯酸盐。
下列说法错误的是( )
 与
与  反应生成无毒物质。某同学采用以下装置和步骤模拟工业上氮氧化物的处理过程。
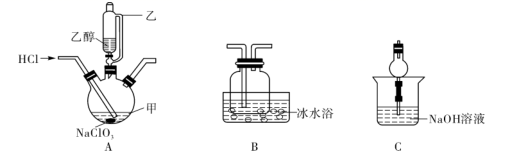
反应生成无毒物质。某同学采用以下装置和步骤模拟工业上氮氧化物的处理过程。 I.提供的装置
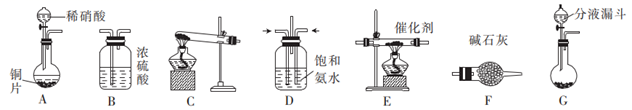
Ⅱ.  的制取
的制取
-
(1) 下列有关实验室制备氨气的说法正确的有(填序号)。
①用氮气与氢气反应制取氨气
②用排饱和食盐水的方法收集氨气
③实验室制氨气有时需要加热,有时不需要加热
④用无水氯化钙干燥氨气
-
(2) 若选择装置G制取氨气,则分液漏斗中盛装的液体试剂是。
-
(3) 若选择装置C制取氨气,则反应的化学方程式是。
-
(4) Ⅲ.模拟尾气的处理
选用上述部分装置,按下列顺序连接成模拟尾气处理装置,回答有关问题:
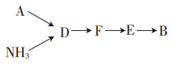
A装置中反应的离子方程式为。
-
(5) D装置中的液体可换成___________(填字母)。A .
 B .
B .  C . 浓硫酸
C . 浓硫酸
-
(6) 该同学所设计的模拟尾气处理实验存在的明显缺陷是。
-
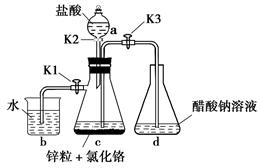
(1) 实验中所用蒸馏水均需经煮沸后迅速冷却,目的是,仪器a的名称是。
-
(2) 将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开K1、K2 , 关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为。
②同时c中有气体产生,该气体的作用是。
-
(3) 打开K3,关闭K1和K2。c中亮蓝色溶液流入d,其原因是;d中析出砖红色沉淀,为使沉淀充分析出并分离,需采用的操作是、、洗涤、干燥。
-
(4) 指出装置d可能存在的缺点。
- 中共十一届三中全会后,我国在农村经济体制改革方面的突极性举措是( ) A.直接选举农村的基层干部
- 依次填入下列各组横线处的词语,恰当的一组是( ) ①其结果就是在脑海中 了一种真正狂热的自由思想,并
- (14分)生活中我们通常会用到一些描述生物与生物、生物与环境之间关系的谚语或诗句,这些谚语或诗句同时也蕴含了一定的人生哲
- 太阳从东边升起西边落下是地球上的自然现象但在某些条件下在纬度较高的地区上空飞行的飞机上乘客可以看到太阳从西边升起的奇妙现
- --- Where did Jane gojust now? ---I don’tknow. When
- 说:“自从有了中国,中国革命的面目就焕然一新了。”对此理解正确的是 A.中国进入新民主主义革命时期 B.中国革命从此有了
- 2006年下半年至2007年年底以前选举的县、乡两级人大代表的任期陆续届满,需要依法选举产生新一届县、乡两级人大代表。2
- 《义猴》 某山隅有一老圃,早失偶,惟一女远适他乡。猎者怜其孤,赠以猴。老这爱如赤子,每出必从,不链不掣,
- 在农作物的盛花期遭遇连续暴雨,正常受粉受到影响,为防止减产,农民采取了喷洒一定浓度的生长素类似物溶液的措施。这种措施对哪
- 下列动物中:海马、青蛙、蛇、龟、鸡、兔都是哪种类群的动物?
- 前面是一条路,先生没有走完就倒下了, ,继续前进。
- (09年雅礼中学月考理)给出定义:若(其中m为整数),则m 叫做离实数x最近的整数,记作= m. 在此基础上给出下列关于
- 观察下面显微镜结构图,回答下列问题:(1)具有放大物像功能的结构[ 1 ] _________ 和[ 6] ______
- 读“极地投影太阳光照图”,虚线表示极圈和回归线,阴影部分表示黑夜,完成下列问题。 (1)该图反映的日期是
- (本小题满分12分) 某几何体的直观图与三视图如下,其中主视图、俯视图都是直角三角形,左视图是等边 三角形.(Ⅰ)证明:
- 时间过得好快,看到那些蹦蹦跳跳、满脸稚气的小学生,蓦然回首,我们已经是一名光荣的中学生了……在这十三四岁的生命里,是谁
- 昔日的北大荒--三江平原如今成为了中国的“北大仓”,三江源被誉为“中华水塔”,三江并流地区则被称为“世界生物基因库”。读
- 健康的生活离不开化学,下列做法正确的是( ) A.用工业盐腌制食品 B.不食用用霉变的食物 C.用
- “China Daily”, whose editorial office is in Beijing, also ha
- 东南亚流经国家最多的河流是( ) A.伊洛瓦底江B.红河C.湄公河D.湄南河



