固体溶解度曲线及其作用 知识点题库
从右图中,可以获得多项与甲、乙两物质溶解度有关的信息:
(1)在t2℃时,向50mL水中加入18g甲物质,充分溶解后可得到溶液g,是(选填“饱和”或“不饱和”)溶液;
(2)如甲物质中混有少量乙,可以用方法提纯;
(3)两曲线的交点A表示;
(4)你还能获得的一项信息是:。
如图1所示,A、B、C为三种物质的溶解度曲线,请根据图示信息回答下列问题.

-
(1) t1℃时,100克A的饱和溶液中含溶质的质量是.
-
(2) t1℃时,将30g B物质投入100g水中,充分溶解,温度不变,所得溶液为溶液(填“饱和”或“不饱和”)
-
(3) 下列说法正确的是 .A . t2℃时,将A和C的混合溶液(两者均已达到饱和),降温至t1℃,析出晶体含有A和C B . t2℃,将A,B,C的饱和溶液分贝降温至t1℃,所得溶液中溶质质量分数的大小关系是B>A>C C . 从混有少量A的C物质中提取较纯净的C,可通过升温结晶的方法来实现 D . t1℃时,欲用A的饱和溶液配制10%的A溶液,只需要烧杯、量筒、胶头滴管三种玻璃仪器
-
(4) 如图2所示,向放有镁片的试管中滴加稀盐酸后,锥形瓶中C中的饱和溶液变浑浊,请解释原因.
甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图。下列说法中正确的是( )

A . 甲的溶解度比乙大
B . t1℃时,将等质量的乙、丙分别配成饱和溶液,所得溶液质量:乙>丙
C . 将甲、丙的饱和溶液分别由t1℃升温到t2℃,两种溶液中溶质的质量分数相等
D . 将t3℃时甲、乙、丙的饱和溶液分别恒温蒸发等量的水,析出溶质的质量:甲>乙>丙
A,B,C三种固体物质的溶解度曲线如图所示,下列说法正确的是( )

A . t1℃时,三种物质的溶解度由大到小的顺序是A>B>C
B . t2℃时,A和C的溶解度相等
C . 将B的饱和溶液变为不饱和溶液可采用升高温度的方法
D . A,B,C三种物质的溶解度都随温度的升高而增大
20℃时,将等质量的甲、乙两种不与水反应的固体物质(不含结晶水),分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3.则下列说法中错误的是()

A . 图1中乙的溶液可能是不饱和溶液
B . 图2中两溶液溶质质量分数一定相等
C . 图3中 M表示的是甲的溶解度曲线
D . 图2中两溶液降温至30℃都会析出晶体
如图是硝酸钾和氯化钠的溶解度曲线,下列有关叙述正确的是( )

A . 硝酸钾的溶解度大于氯化钠的溶解度
B . 40℃时,硝酸钾饱和溶液比氯化钠饱和溶液的浓度大
C . 40℃时,100克硝酸钾饱和溶液中含有硝酸钾63.9克
D . KNO3中混有少量的NaCl可以采用蒸发结晶得到KNO3晶体
PbO能溶解在不同浓度的NaOH溶液中,其溶解度曲线如图所示。下列叙述错误的是()

A . 100℃时,PbO在35%NaOH溶液中的溶解度为100g·L-1
B . 60℃时,PbO在35%NaOH溶液中的溶解度大于在10%NaOH溶液中的溶解度
C . 20℃时,PbO在10%NaOH溶液中所溶解的质量,一定小于在35%NaOH溶液中所溶解的质量
D . 80℃时,将PbO溶解在10%NaOH溶液中达到饱和,然后降温至40℃,该过程中一定析出固体
如图是A,B,C三种不含结晶水的固体的溶解度曲线图。下列说法不正确的是( )

A . t3℃时,取30gA加入50g水中,可得到溶液75g
B . P点表示t2℃时,A,B的溶解度相等
C . t3℃时,等质量的A,B,C三种物质加入水中,配制饱和溶液,所得溶液的质量大小关系为C>B>A
D . t1℃时, A,B,C三种饱和溶液的质量关系为B>A=C
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答。

-
(1) t3℃时,甲的溶解度为g。
-
(2) 将丙的饱和溶液变为不饱和溶液的一种方法是。
-
(3) t1℃时,甲、乙的饱和溶液各100g,分别蒸发掉10g水,析出固体的质量:甲(填“>”“<”或“=”)乙。
-
(4) t2℃时,在各盛有甲、乙、丙25g固体的三个烧杯中,分别加入100g水,充分搅拌后,能形成饱和溶液的是;将三个烧杯中的物质均升温至t3℃,此时,溶液中溶质的质量分数的大小关系为。
下列说法正确的是( )

A . 烧杯a中加入的固体为N
B . 40℃时烧杯a中溶液一定是饱和溶液
C . 40℃时烧杯b和20℃时烧杯b中溶质质量不相等
D . 40℃时烧杯a和20℃烧杯b中溶液的溶质质量分数相等
甲、乙两种固体物质的溶解度曲线如右下图所示。  时,进行了如下图所示的实验,下列叙述正确的是:
时,进行了如下图所示的实验,下列叙述正确的是:
 时,进行了如下图所示的实验,下列叙述正确的是:
时,进行了如下图所示的实验,下列叙述正确的是: 

-
(1) 甲和乙的溶解度相等时的温度为
 ;
;
-
(2) 上述实验过程中,属于不饱和的溶液的是(填字母,下同);溶液中溶质的质量分数相同的是。
-
(3) 将
 时,等质量的甲、乙饱和溶液降温至
时,等质量的甲、乙饱和溶液降温至  ,所得溶液中溶剂的质量甲乙(填“
,所得溶液中溶剂的质量甲乙(填“ 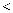 ”、“
”、“  ”或“
”或“  ”)。
”)。
-
(4) 将
 时,
时,  甲的饱和溶液降温至
甲的饱和溶液降温至  时,析出晶体的质量
时,析出晶体的质量  .
.
分析如图溶解度曲线,下列说法错误的是( )

A . t1℃时,甲和乙的溶解度相等
B . t2℃时,在100g水里加入100g甲固体,得到200g甲溶液
C . t2℃时,等质量的两种物质的饱和溶液同时降温至t1℃,盛有甲溶液的烧杯中析出较多晶体
D . 将t1℃时两种物质的饱和溶液升温至t2℃,溶质质量分数:甲>乙
如图是A、B两种物质的溶解度曲线,二者溶解度相同的温度是℃;“冬天捞碱,夏天晒盐”,其中“碱”的溶解度曲线与图中物质(填字母)的溶解度曲线相似;t2℃时,把150gA的饱和溶液稀释为溶质质量分数为20%,需加水g。

如图1是A、B、C三种物质的溶解度曲线,请回答。

-
(1) t2℃时,将30gA物质放入50g水中,充分溶解后所得溶液中溶质与溶剂的质量之比为(填最简整数比);向该溶液中继续加入25g水,则此时溶液中溶质质量分数为(计算结果保留至0.1%)。
-
(2) A物质中混有少量B物质,若提纯A物质,可采取的结晶方法是。
-
(3) 如图2所示,t1℃时,取等质量的A、C饱和溶液分别置于甲、乙两支试管中,在大烧杯中加入一定质量的硝酸铵固体溶解后,所得A、C溶液的溶质质量分数大小关系为AC(填“>”“<”或“=”)。
-
(4) 实验室配制一定溶质质量分数的A溶液,若实际配得的溶液中溶质质量分数偏大,则可能是量取水时(填“俯视”或“仰视”)量筒读数所致。
-
(5) 下列说法正确的是(填序号)。
①将A物质的饱和溶液变为不饱和溶液,其溶质的质量分数一定减小
②将t1℃时C物质的饱和溶液升温到t2℃,其溶液的质量一定减小
③t2℃时,A、B、C三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序为A>B>C
根据如图的溶解度曲线,判断下列说法正确的是( )

A . 甲中含有少量的乙时,宜采用蒸发结晶的方式提纯甲
B . t2℃时,甲、乙溶液溶质的质量分数相等
C . t3℃时,将甲、乙的饱和溶液都蒸发10g水,甲析出的晶体质量一定大于乙
D . 将t3℃时甲、乙的饱和溶液降温至t1℃时,一定是甲析出的质量多
如图是A、B、C三种物质的溶解度曲线。下列叙述错误的是( )

A . t1℃时,三种物质的溶解度大小顺序为A<B<C
B . 将t3℃时,A,B,C的饱和溶液降温到t2℃所得溶液的溶质质量分数由大到小的顺序为B>A=C
C . t3℃时A的饱和溶液中含有少量B物质时,可以采取冷却的方法提纯A
D . t3℃时B的饱和溶液降温到t1℃,会有晶体析出
“侯氏制碱法”生产纯碱的主要反应是NaCl+NH4HCO3=NaHCO3↓+NH4Cl。如图是三种物质的溶解度曲线。下列叙述正确的是( )

A . 0℃时,NH4Cl的溶解度大于NaCl的溶解度
B . 20℃时,NaHCO3饱和溶液中溶质的质量分数一定大于NH4Cl不饱和溶液中溶质的质量分数
C . 20℃时,100g水中加入5.85g NaCl和7.9g NH4HCO3固体,肯定有NaHCO3晶体析出
D . NH4Cl固体中含有少量的NaCl,可用降温结晶的方法提纯NH4Cl
10℃时,将3g甲、乙两种可溶性固体分别放入盛有10mL水的试管中。两种物质的溶解情况(见图I),两种物质的溶解度随温度的变化(见图Ⅱ)。下面对甲、乙两物质的判断,不正确的是( )

A . 10℃时,甲、乙两物质的溶液都是饱和溶液
B . 温度升高至25℃时,甲、乙两物质的溶液都是不饱和溶液
C . 甲物质对应的溶解度曲线为a
D . 可用降温结晶法分离甲、乙两种物质的混合物
NaCl和KNO3溶解度曲线如图所示,下列说法正确的是( )

A . KNO3的溶解度大于NaCl的溶解度
B . KNO3的溶解度随温度的升高而增大
C . 20℃时,40 gKNO3 可完全溶解在100 g水中
D . NaCl溶液的溶质质量分数与KNO3溶液的溶质质量分数不可能相等
甲、乙两种物质的溶解度曲线如图所示。下列说法错误的是( )

A . t1℃时,甲、乙的溶解度相等
B . t1℃时,甲、乙的饱和溶液中溶质质量相等
C . t2℃时,在100g水中加入25g甲,形成甲的不饱和溶液
D . 当甲中混有少量乙时,可采用降温结晶的方法提纯
最近更新
- 下列有关环境和能源的说法错误的是( ) A. 回收处理废旧电池既可节约金属资源又可减少环境污染 B. 过量使用农
- 移栽植物时,常常去掉一些叶片,其目的是为了( ) A.降低光合作用 B.减少呼吸作用 C.降
- 在不透明的口袋中,有四只形状、大小完全相同的小球,四只小球上分别标有数字1,2,3,4. 小明先从盒子里随机取出一只小球
- 在A、B两支大试管中分别依次加入苯、H2O,再用长颈漏斗小心加入CCl4。两试管中都明显分为三层,将A试管振荡后静置(已
- 读“中国东部地区梅雨期起讫等日期线图”,回答问题。(1)在多年平均情况下,福州梅雨起始日是_______,徐州梅雨终止日
- 在“验证牛顿第二定律”的实验中,打出的纸带如图3-44(a)所示,相邻计数点间的时间间隔是t.(1)测出纸带各相邻计数点
- 观察细胞内某生理过程示意图(图中甲表示甲硫氨酸,丙表示丙氨酸),回答问题:(1)该图所示生理过程的原料是________
- 被动屋(图1)即被动式超低能耗绿色建筑,起源于德国,是国际认可的一种集高舒适度、低能耗、经济性于一体节能建筑技术
- 1925年,一位外国游客来到上海,他不可能看到的现象有( ) A.报童叫卖《申报》创刊号
- 沿直线运动的一辆汽车以速度v匀速行驶了全程的一半,然后匀减速行驶另一半路程,恰好至停止。则汽车通过全程的平均速度是A.
- 已知函数. (1)求函数f(x)的单调区间; (2)已知a、b∈R,a>b>e,(其中e是自然对数的底数),
- 已知:A=,B= (1)求A+B的值; (2)若3A+6B的值与无关,求的值
- 如图所示,轻绳两端分别与A、C两物体相连接,mA=1kg,mB=2kg,mC=3kg,物体A、B、C及C与地面间的动摩擦
- 下列各句中,标点符号使用正确的一项是 A.第二代无绳电话采用了数字技术,主要有泛欧数字无绳电话、个人便携式电话、个人接入
- 一对夫妇第一胎生了一个女孩,那么第二胎生男孩的几率是 ( )A.100%B.50%C.25%D.0
- 下列说法正确的是 A. 的结构中含有脂基 B.顺-2-丁烯和反-2-丁烯的加氢产物不同 C.1葡萄糖可水解生成2乳酸()
- 已知直线,当k变化时,所有直线都过定点( )A. B. C.(3,1)
- Julia saw a purse on the ground her way home yeste
- Ask Dr ?Jeffers This month Dr. Jeffers is answering question
- 化学与我们的生活息息相关。(1)为了全民健康,卫生部推广使用强化加铁酱油,这里的“铁”指的是 (填“单质”、“元素



