金属的化学性质 知识点题库
序号 | 物质(括号内为杂质) | 除杂试剂 | 分离方法 |
A | 氯化钠固体(碳酸钠) | 稀盐酸 | 蒸发结晶 |
B | 氯化铜溶液(氯化锌) | 金属铜 | 过滤 |
C | 二氧化碳(一氧化碳) | 氢氧化钠溶液 | 洗气 |
D | 二氧化锰粉末(碳粉) | 水 | 过滤 |
(1)若得到的滤液为浅绿色,则滤液中的溶质一定含有 (填写化学式,下同),可能含有 .
(2)若得到的滤液为无色,则滤渣中至少含有 种金属.
(3)反应后得到滤渣的质量 (选填“小于”、“大于”或“等于”)反应前加入镁粉的质量.
步骤1:将镁条用砂纸打磨至光亮,分成两等份.
步骤2:将一份光亮的镁条置于冷水中,几乎没有观察到任何现象.
步骤3:将另一份光亮的镁条置于热水中,观察到有气泡产生.
(1)将镁条用砂纸打磨至光亮的原因是 .
(2)经百度可知,活泼金属与水反应生成对应的碱和氢气.如果金属活动性越强,生成碱的碱性就越强.某同学向步骤③的烧杯中滴加酚酞试液,观察到镁条的表面有明显的红色出现.该反应的化学方程式为 ,该反应是反应(填基本反应类型).
(3)步骤2和3对比可知,影响镁与水反应速率的因素是 .
(4)根据以上信息,若将金属钠加到硫酸铜溶液中,推测可能观察到的现象是 .
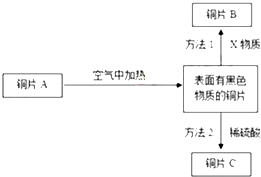
图为铜片A的系列变化,据图回答问题:
-
(1) 若方法1中的X物质为常见气体,且发生置换反应,则X是(填化学式);
-
(2) 写出方法2的化学方程式;
-
(3) 铜片A、铜片B、铜片C的质量分别为mA、mB、mC , 其中方法1和方法2均完全反应,则mA、mB、mC的大小关系为.

甲同学方案:合金粉末 ![]() 过滤,将得到固体洗涤、干燥、称量,称得质量为a克.
过滤,将得到固体洗涤、干燥、称量,称得质量为a克.
乙同学方案:合金粉末 ![]() 过滤,将得到的固体洗涤、干燥、称量,称得质量为b克.
过滤,将得到的固体洗涤、干燥、称量,称得质量为b克.
请回答下列问题:
-
(1) 甲同学方案中,反应开始发生时的明显现象是.
-
(2) 实验结束后,甲同学计算出合金中铜的质量分数为:
 ;
;乙同学计算出合金中铜的质量分数为:
 .
.经过同学们讨论,一致认为同学的计算结果是错误的,原因是.
 B .
B .  C .
C .  D .
D . 
提出问题:涂料添加剂“银粉”是什么金属?
建立假设:“银粉”可能是 Ag、Al、Zn、Cu 四种金属中的一种
获取事实与证据:①观察“银粉”呈银白色,则“银粉”一定不是金属。
②取一定量“银粉”加少量稀盐酸,有大量气泡产生,则“银粉”肯定也不是金属。
③取②中少量液体,投入一小块镁条,充分反应后,过滤,测得反应后溶液质量比反应前增加了,则“银粉”一定是 金属。
【提出问题】锡纸中的金属是什么?
【建立猜想】根据锡纸有银白色金属光泽,并结合金属活动性、价格等因素,猜想其中的金属可能是锌、铁、铝、锡中的一种。
-
(1) 【探究过程】
步骤 活动内容 收集证据 分析并得出结论 步骤一 ①查阅资料:金属锌在室温下很脆
②取锡纸反复折叠锡纸未破损 锡纸中金属不是锌 步骤二 用磁铁靠近锡纸 锡纸没有被磁铁吸引 锡纸中金属不是
步骤三 ①取锡纸条放入浓度为20%的盐酸中除去可能存在的氧化膜。当观察到现象时,取出锡纸条并用蒸馏水清洗。
②将处理过的锡纸条放入试管中,加入饱和硫酸锌溶液,静置观察。②中锡纸条表面无明显现象 说明锡纸中的金属活动性比锌弱,则锡纸中金属不是铝,而是锡 -
(2) 【交流评价】小科对实验结论提出质疑:“无明显现象”并不代表没有发生反应,因为铝与硫酸锌反应[2Al+3ZnSO4=3Zn+Al2(SO4)3]生成的金属锌为银白色,与铝颜色相同,因此无法得出结论。请在不改变化学反应的前提下增加定量实验完善实验方案,并根据预期结果得出相应结论:。

-
(1) 1625年格劳贝尔发现将金属放入稀盐酸中会“消失",这为发现金属活动性顺序奠定了基础。小嘉选用锡、铜、锌三种金属重温实验,则会“消失”的金属有。
-
(2) 1766年卡文迪许用金属与酸反应制取了一种可燃性气体,他称之为“可燃空气”,其实该气体就是。从此为探索金属活动性打开了新思路。
-
(3) 1865年贝开托夫经过大量的实验得出了金属活动性规律。小嘉运用该规律开展实验,向硝酸铜和硝酸银的混合溶液中逐渐加入铁粉,溶液质量变化如图所示,则B点时溶液中所含的金属阳离子有。
-
(1) 铜常用来做导线,这是因为铜具有良好的。
-
(2) 将一定质量的锌粒投入含有Cu(NO3)2和Fe(NO3)2的混合溶液中,充分反应后过滤,若滤液中只含一种溶质,则滤渣中一定含有。
-
(3) 将等质量的镁和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量和反应时间的关系如图所示,下列说法正确的是。(选填字母代号)

A.0-t1时段,镁的反应速度比铁小
B.反应结束后,产生氢气的质量镁比铁少
C.反应结束后,镁一定有剩余
D.反应消耗稀盐酸的总质量一定相等
 H2
H2  Cu ②CuO
Cu ②CuO  CuSO4
CuSO4  Cu,若用这两种方法制得的铜的质量相等,下列叙述符合实验结果的是( )
Cu,若用这两种方法制得的铜的质量相等,下列叙述符合实验结果的是( )
- 如图是某生态系统示意图,当一种生物的全部同化量来自两种生物时,则同化量各占一半,下列叙述不正确的是() A. 该生态系统
- 下列依据热化学方程式得出的结论正确的是 ( )A. 已知2H2(g)+O2(g)=2H2O(l) ΔH=-483.6
- 阅读下面短文,掌握其大意,然后从各题所给的四个选项(A、B、C和D)中,选出最佳选项,并在答题卡上将该项涂黑。 My f
- 下列各句中,没有语病,句意明确的一句是 A.如何防备展览会的贵重物品免遭盗窃,这是西方国家深感头痛的问题。 B.改革开放
- 有两个事件,事件A:367人中至少有2人生日相同;事件B:抛掷一枚均匀 的骰子,朝上的面点数为偶数.下列说法正确的是【
- 继“西部大开发”、“中部崛起”后,我国又制订了“实现东部新跨越”的战略方针,环渤海经济圈作为东部的一个重要组成部分,正在
- 若是(,,)展开式中 项的二项式系数,则
- 判断下列各句所用修辞方法完全正确的一项(2分) ( ) (1)上野的樱花烂熳的时节,望去
- 如图,在△ABC中,点D在BC上,在下列四个条件:①∠BAD=∠C;②∠ADC+∠BAC=180°; ③BA2=BD·B
- 胶体区别于其他分散系的本质特征是 ( ) A 光束穿过胶体时形成一条
- 如图所示,试管中盛有某种液体,将气球中的某种固体小心的倒入试管中,不能观察到气球变大的一组物质是() A. 氯化钠和水
- 2011年我国城乡居民人民币储蓄存款余额达35.2万亿元,人均储蓄25548元,分别比2010年增长16%和15.3%
- 综合性学习(8分)书是人类知识的宝库,书是人类精神的殿堂。在这里我们认识了多彩的世界,在这里我们读懂了喜怒哀乐,在这里我
- 一个静止的物体在显微镜下观察到的物像若在视野左下方,要想将物像置于视野正中央,应将装片移向 ( )
- 已知a>b>0,则下列各式中成立的是( )A. B.C.
- 已知与之间的一组数据:则与的线性回归方程必过点( ) A. B.
- 认真分析测定相对原子质量的示意图,推断A原子的相对原子质量约为() A.12 B. 16
- 如图,在平面直角坐标系中,△ ABC的三个顶点的坐标分别为A(0,1),B(-1,1),C(-1,3)。 (1)画出△A
- 已知函数f(x)= 则f[f()]的值是 ( ) A.9
- (6分)写出下列反应的化学方程式。(1)检验乙醇中是否混有乙醛:



