晶体熔沸点的比较 知识点题库
选项 | 参数 | 比较 | 解释 |
A | 沸点 | HF<HCl<HI | 组成结构相似的物质,相对分子质量越大沸点越高 |
B | 半径 | Na+<Mg2+<Al3+ | 同一周期粒子半径随原子序数的递增逐渐减小 |
C | 酸性 | H2SO3>H2CO3 | 元素的非金属性越强,其含氧酸的酸性越强 |
D | 还原性 | P3﹣>S2﹣>Cl﹣ | 元素的非金属性越强,简单阴离子的还原性越弱 |
-
(1) 氯酸钾熔化,粒子间克服了 ;二氧化硅熔化,粒子间克服了;碘的升华,粒子间克服了。三种晶体的熔点由高到低的顺序是。
-
(2) 下列六种晶体①CO2 ②NaCl ③Na
④Si ⑤CS2 ⑥金刚石,它们的熔点按从低到高的顺序为(填序号)。
-
(3) 在H2、(NH4)2SO4、SiC、CO2、HF中,能形成分子晶体的物质是(填化学式),含有氢键的晶体的化学式是,属于离子晶体的是,属于原子晶体的是,五种物质的熔点由高到低的顺序是。
-
(1) 电负性ZnTe(填“>”或“<”或“=”)。
-
(2) O、S、Se与Te元素位于同一主族。基态碲(Te)原子核外电子排布式为[Kr],有个未成对电子。
-
(3) H2O、H2S、H2Se沸点由低到高顺序为,推断的依据是;SO2分子中S原子采取杂化;用价层电子对互斥理论解释SO42-的键角大于SO32-的原因是。
-
(4) 向氯化锌溶液中加入过量的氨水,得到[Zn(NH3)4]Cl2 , 此配位化合物中含有的化学键有共价键、、。
-
(5) 碲化锌晶体有两种结构,其中一种晶胞结构如下图:
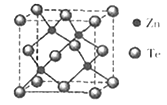
晶胞中含有个Te原子;与Te原子距离最近的Te原子有个;若两个距离最近的Te原子间距为apm.则晶体密度为g/cm3。
-
(1) 基态Fe原子价层电子排布式是。
-
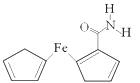
(2) 已知二茂铁甲酰胺熔点是176℃,沸点是249℃,难溶于水,易溶于氯仿、丙酮等有机溶剂。据此可推断二茂铁甲酰胺晶体为晶体。
-
(3) 二茂铁甲酰胺中碳原子的杂化方式为,H、C、N、O四种元素的电负性由大到小的顺序是。
-
(4) 碳、氮元素对应的最简单氢化物分别是CH4和NH3 , 相同条件下CH4的沸点比NH3的沸点(填“高”或“低”),主要原因是。
-
(5) 氢、氮、氧三种元素按照4:2:3的原子个数比形成离子化合物。该离子化合物中,阳离子空间构型是,1 mol阴离子含有σ键的数目为。
-
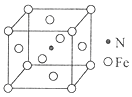
(6) 氮和铁能形成一种磁性材料,其晶胞如图所示,该磁性材料的化学式为。已知晶胞参数为a nm,则该晶胞密度的计算式为ρ=g/cm3(用NA表示阿伏加德罗常数的值)。
-
(1) Ⅰ.已知元素M的气态原子逐个失去第1至第4个电子所需能量(即电离能,用符号
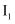 至
至  表示)如表所示:
表示)如表所示: I1
I2
I3
I4
电离能(kJ/mol)
578
1817
2745
11578
元素M的常见化合价是_____________。
A .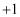 B .
B . 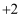 C .
C . 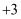 D .
D . 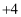
-
(2) 如图折线表示ⅣA~ⅦA族中某一族元素氢化物的沸点变化,每个小黑点代表一种氢化物,其中a点代表的是_________。
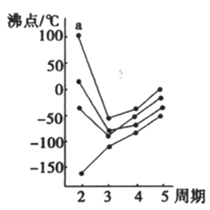 A .
A . B .
B .  C .
C .  D .
D . 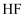
-
(3) 某共价化合物
 ,两个
,两个 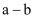 键间的夹角为180°,由此可判断
键间的夹角为180°,由此可判断  属于____。
A . 由极性键形成的极性分子 B . 由极性键形成的非极性分子 C . 由非极性键形成的极性分子 D . 由非极性键形成的非极性分子
属于____。
A . 由极性键形成的极性分子 B . 由极性键形成的非极性分子 C . 由非极性键形成的极性分子 D . 由非极性键形成的非极性分子 -
(4) 下列关于物质熔点高低的比较,错误的是________。A . 金刚石
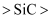 晶体硅
B .
晶体硅
B . 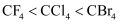 C .
C . 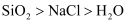 D .
D . 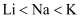
-
(5) 下列关于
 晶体的叙述中,错误的是_______。
晶体的叙述中,错误的是_______。 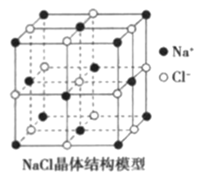 A .
A .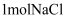 中有
中有  个
个  分子
B . 每个晶胞中平均含有4个
分子
B . 每个晶胞中平均含有4个  和4个
和4个  C .
C .  晶体中,
晶体中,  和
和  的配位数都是6
D .
的配位数都是6
D .  晶体中,每个
晶体中,每个  周围有12个与它最近且等距离的
周围有12个与它最近且等距离的 
-
(6) Ⅱ.第四周期的多种元素及其化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
基态
 原子的核外电子排布式为。
原子的核外电子排布式为。 -
(7) 琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成
 。从核外电子排布角度来看,
。从核外电子排布角度来看,  易被氧化成
易被氧化成  的原因是。
的原因是。
-
(8)
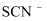 离子可用于
离子可用于  的检验。
的检验。 ①
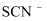 中C原子的杂化方式为。(已知:
中C原子的杂化方式为。(已知: 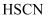 的结构式为
的结构式为 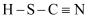 )
)②写出与
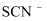 互为等电子体的一种分子。
互为等电子体的一种分子。③S、C、N三种元素中,电负性最小的是。
-
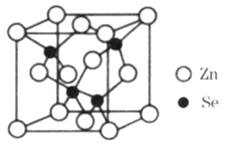
(9)
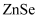 的晶胞结构如图所示,该晶胞边长为
的晶胞结构如图所示,该晶胞边长为 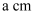 ,
, 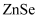 的摩尔质量为
的摩尔质量为 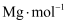 。用
。用  代表阿伏加德罗常数的数值,则该晶胞密度(ρ)的计算列式为ρ=
代表阿伏加德罗常数的数值,则该晶胞密度(ρ)的计算列式为ρ= 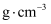 。
。 
-
(1) Z在元素周期表中的位置是,R 的一种核素中质子数与中子数相等,则该核素的名称为
-
(2) 请用“> ”、 “<”或“=”填空。
非金属性: UV;简单气态氢化物的沸点:V X ;最高价氧化物对应的水化物的酸性: X Y
-
(3) V、X、Z 三种元素的简单离子半径由大到小的顺序为(用离子符号填空)
-
(4) R、U、V 三种元素形成的离子化合物为(填化学式)用电子式表示 Z2X的形成过程
-
(5) W的最高价氧化物与Z 的最高价氧化物对应的水化物反应的化学反应方程式为 。
-
(6) 实验室中,做过银镜反应的试管内壁会附着一层金属银,常用稀的RUV3 溶液进行洗涤 ,则该反应的离子反应方程式为
-
(1) 下列状态的铝中,能量较小的是,其原因是。
A.[Ne]3s13p2 B.[Ne]3s23p1
-
(2) 由元素周期律,推出元素电负性Al(填“大于”、“小于”)Si。
-
(3) 科学家合成了“N4H4”离子晶体。阴离子为“
 ”,其空间构型为,阳离子的中心原子轨道杂化方式为。
”,其空间构型为,阳离子的中心原子轨道杂化方式为。
-
(4) AlF3熔点远高于AlCl3的原因是;AlCl3晶体变成气体时,测得气体的相对分子质量接近267,其中氯只有两种化学环境,比例为2:1,试画出该气体分子的结构式。
-
(5) 原子晶体AlN的晶胞参数为a=x pm,它的晶体的晶胞结构如图。
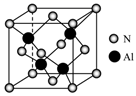
①该晶胞内存在共价键数目为;
②紧邻的N原子之间距离为b,紧邻Al、N原子间距离为d,则b:d=;
③该晶体的密度为g·cm-3(阿伏加德罗常数的值用NA表示)。
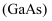 是当前最重要、技术成熟度最高的半导体材料之一、我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
是当前最重要、技术成熟度最高的半导体材料之一、我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。 
-
(1) 基态
 原子核外电子排布式为,最高能级电子的电子云形状为。
原子核外电子排布式为,最高能级电子的电子云形状为。
-
(2)
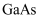 和
和 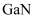 为结构相似的原子晶体,沸点
为结构相似的原子晶体,沸点 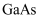
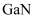 (填“>”或“<”,下同),第一电离能
(填“>”或“<”,下同),第一电离能 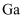
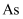 。
。
-
(3) 成语“信口雌黄”中雌黄的分子式为
 ,分子结构如图1,
,分子结构如图1, 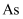 原子的杂化方式为。
原子的杂化方式为。
-
(4)
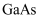 的晶胞结构如图2,在
的晶胞结构如图2,在 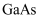 晶体中,与
晶体中,与 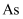 原子最近且等距离的
原子最近且等距离的 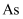 原子数为,
原子数为, 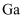 原子位于
原子位于 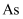 形成的空隙中。
形成的空隙中。
-
(5) 若砷化镓晶胞边长为
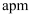 ,则
,则 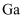 与最近
与最近 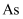 的核间距为
的核间距为 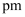 。
。
-
(1) 写出氯碱工业中阳极的电极反应式。
-
(2) 石英的熔点远高于干冰的原因是。
-
(3) 离子化合物 MgO2可用于治疗消化道疾病,各原子均满足8电子稳定结构。写出 MgO2的电子式。
-
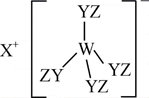
(4)
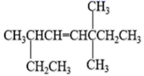 可与H2反应,请用系统命名法对其产物命名。
可与H2反应,请用系统命名法对其产物命名。
 的相对分子质量比
的相对分子质量比 大,分子间作用力也大
B .
大,分子间作用力也大
B .  晶体中所含的化学键只有离子键
C .
晶体中所含的化学键只有离子键
C .  、
、 、
、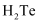 熔沸点依次增大
D . 硫酸氢钠溶于水只破坏了离子键
熔沸点依次增大
D . 硫酸氢钠溶于水只破坏了离子键
-
(1) 路易斯酸碱电子理论认为:凡是能接受电子对的物质(离子、分子或原子团)都称为路易斯酸;凡是能给出电子对的物质(离子、分子或原子团)都称为路易斯碱。根据信息判断,H2O属于(填“酸”或“碱”,下同),Ag+属于。
-
(2) 查表可知,金属铝(Al)的三卤化物晶体的熔点如下:
物质
AlF3
AlCl3
AlBr3
熔点/℃
1290
192.4
97.8
AlF3为什么熔点比AlCl3高得多,请分析原因。
-
(1) 基态
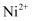 的M层电子排布式为;下列现象与核外电子跃迁有关的是(填字母)。
的M层电子排布式为;下列现象与核外电子跃迁有关的是(填字母)。a.金属Ni导电 b.
 燃烧放热 c.日光灯通电发光 d.乙醇挥发
燃烧放热 c.日光灯通电发光 d.乙醇挥发 -
(2) 镍能形成多种配合物,其中
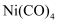 和
和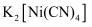 的相关信息如下:
的相关信息如下:配合物
状态
溶解性
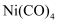
无色挥发性液体
不溶于水,易溶于苯、四氯化碳等有机溶剂
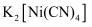
红黄色单斜晶体
易溶于水
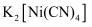 熔点高于
熔点高于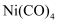 的原因是;
的原因是;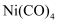 为分子(填“极性”或“非极性”),Ni提供的空轨道数目为。
为分子(填“极性”或“非极性”),Ni提供的空轨道数目为。 -
(3) 科学家研究发现,在含镍催化剂作用下可利用三聚氰胺制备石墨相光催化材料
 。已知三聚氰胺在冷水中溶解度小而加热时溶解度增大,从氢键的角度解释原因;
。已知三聚氰胺在冷水中溶解度小而加热时溶解度增大,从氢键的角度解释原因;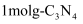 中含有的σ键的物质的量为mol。
中含有的σ键的物质的量为mol。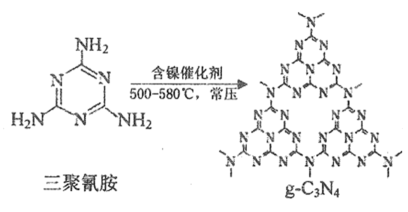
-
(4) 镍能形成多种氧化物,一种镍的氧化物的结构特征:氧离子形成面心立方结构,镍离子位于氧离子构成的八面体空隙。下图中的(填字母)是从该晶胞中分割出来的结构。
a.
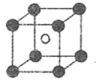 b.
b. 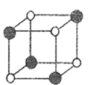 c.
c. 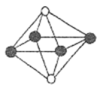 d.
d. 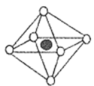 e.
e. 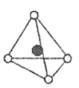
已知该晶体密度为
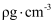 , NA为阿伏加德罗常数的值,则晶胞中两个镍离子之间的最短距离为pm(用含ρ和NA的代数式表示)。
, NA为阿伏加德罗常数的值,则晶胞中两个镍离子之间的最短距离为pm(用含ρ和NA的代数式表示)。
 的空间构型为平面三角形
C .
的空间构型为平面三角形
C . 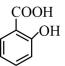 的沸点比
的沸点比- 由1分子磷酸、1分子碱基和1分子化合物a构成了化合物b,如右图所示,则叙述正确的是 ( )
- 已知点在表示的区域内(包含边界),且目标函数取得最大值的最优解有无穷多个,则的值为( )
- 19世纪中期,资本主义列强对外扩张不断加剧,其基本的推动力是 A.资本主义制度的确立
- 24.阅读下面的材料,根据要求作文。 酿酒师把米蒸熟,再把蒸熟的米放进缸里,拌上酒曲,然后把缸密封起来,让米与外界隔绝,
- 20 1 0年1月14日,由山东省委宣传部、省文联等主办的电视剧《南下》研讨会在济南市举行,《南下》从人性化角度突破,活
- 电视剧《西游记》的主题曲《敢问路在何方》中唱道:“你挑着担,我牵着马,迎来日出,送走晚霞”。那么我国最早“迎来日出”的地
- 橡胶树原产于巴西亚马逊河流域马拉岳西部地区,现已布及40多个国家和地区。种植面积较大的国家有:印度尼西亚、泰国、马来西亚
- 北京时间2011年11月17日19时32分,在太空翱翔了17天,行程1100万公里,完成两次完美对接的神舟八号,乘着红白
- 在探究杠杆平衡条件的实验中。 (1)如图甲所示,为了使杠杆在水平位置平衡,可以向________移动左端的螺母。(选填“
- 设变量满足约束条件:,则的最小值为( ) A. B. C.
- (1)已知x=,y=,试求代数式2x2-5xy+2y2的值. (2)先化简,再求值:,其中x=,y=.
- 13.下列各句中,没有语病的一句是(3分) A.被誉为互联网领域“达沃斯论坛”的“乌镇峰会”,全球网络界的许多领军
- 阅读下面的文言文,完成后面问题。 叶清臣字道卿,苏州长洲人。清臣幼敏异,好学善属文。天圣二年,举进士,知举刘筠奇所对策,
- (2010年12月辽宁铁岭高三六校联考34题)英国哲学家怀特海在《科学与近代世界》一书中写道:“伽利略说地球是动的,太阳
- 艾滋病是由于感染人类免疫缺陷病毒(HIV)引起的,该病毒与大肠杆菌最明显的区别是( ) A.无成形的细胞核
- 阅读下面诗歌,完成后面的问题(4分)雾卡尔 桑德堡雾来了――蹑着猫的细步。它静静地弓腰蹲着俯瞰港湾和城市再向前走去。诗
- 根据右上图中小磁针N极的指向,标出通电螺线管电源的“+”、“-”极。
- 广州地铁5号线的列车到站时间间隔是5分钟,某人进站到达列车上车口等车时间超过2分钟的概率是 () A.
- 细菌质粒分子上往往带有一个抗菌素抗性基因,该抗性基因在基因工程中的主要作用是 A.提高受体细胞在自然环境中的耐药性 B.
- 下列句子中括号里的成语,使用恰当的一句是( )A、要在打基础、管长远、固根本的工作上多动脑筋,花气力,坚决摒弃(急功近利



