晶体熔沸点的比较 知识点题库
-
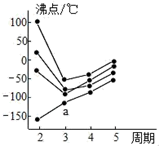
(1) 元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为 nm(填标号).A . 404.4 B . 553.5 C . 589.2 D . 670.8 E . 766.5
-
(2) 基态K原子中,核外电子占据的最高能层的符号是,占据该能层电子的电子云轮廓图形状为.K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是.
-
(3) X射线衍射测定等发现,I3AsF6中存在I3+离子.I3+离子的几何构型为,中心原子的杂化类型为.
-
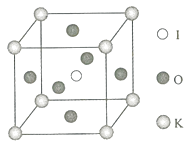
(4) KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示.K与O间的最短距离为nm,与K紧邻的O个数为.
-
(5)
在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于位置,O处于位置.
W | X | |||
Y | Z |
-
(1) 现有:①氯化钠晶体;②金刚石;③晶体硅;④干冰;⑤白磷,其熔点由高到低的顺序为(填序号);
-
(2) 对硝酸进行一系列的实验,其中部分实验(包括现象)如下:
①浓硝酸中滴入紫色石蕊试液,溶液先呈红色后褪色;
②两根玻璃棒分别蘸有浓硝酸和浓氨水,靠近(不接触)两根玻璃棒出现白烟;
③将铜片投入浓硝酸中,溶液变绿色并产生大量红棕色气体;
④在稀硝酸中逐渐加入铁粉,溶液颜色先变棕黄色后变浅绿色,且开始有气泡出现后来无气泡;
⑤浓硝酸中加入红热的炭,产生大量混合气体
上述实验中,硝酸既表现强氧化性又表现酸性的实验是(填实验序号,下同),既表现酸性又表现挥发性的是,只表现强氧化性的是.
-
(3) 有等体积混合而成的四组气体:①NO2+NO;②NO2+O2;③HCl+N2;④NO+N2 ,
将其分别通入体积相同的试管,并立即倒立于水槽中,试管内水面上升的高度分别为H1 , H2 , H3 , H4 , 其中高度关系正确的是 .
A . H2>H3>H1>H4 B . H3>H2>H1>H4 C . H1=H2=H3=H4 D . H1>H2>H3>H4 .
-
(1) 元素X在元素周期表中位于区,单质X的晶体类型为,其中X原子的配位数为。
-
(2) Z的氢化物在乙醇中的溶解度大于Y的氢化物,其原因是。
-
(3) X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2 , 1mol该配合物中含有σ键的数目为。
-
(4) X与Y形成的一种化合物的立方晶胞如图所示。
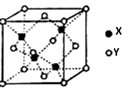
该化合物的化学式为,已知此晶体的密度为ρg·cm–3 , 阿伏加德罗常数为NA , 则此晶胞中X与Y的最近距离是cm。(写出计算式,不要求计算结果。)
-
(1) 请将下列变化过程中破坏的微粒间作用力名称的编号填在横线上:
A.共价键 B.离子键 C.金属键 D.分子间作用力
①氢氧化钠熔化;②干冰升华;
③二氧化硅熔化;④钠熔化。
-
(2) 单质硼有无定形和晶体两种,参考下表数据。
金刚石
晶体硅
晶体硼
熔点(K)
>3823
1683
2573
沸点(K)
5100
2628
2823
硬度
10
7.0
9.5
①根据表中数据判断晶体硼的晶体类型属于晶体;
②请解释金刚石的熔沸点高于晶体硅的原因是。
-
(1) 常温下,乙醇在(填“环己烷或乙酸”)中溶解度更大,主要原因是。
-
(2) Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是。
化合物
TiF4
TiCl4
TiBr4
TiI4
熔点/℃
377
-24.12
38.3
155
-
(1) 钒(V)及其化合物广泛应用于工业催化、新材料和新能源等领域。
①基态钒原子的外围电子排布式为。
②V2O5的结构式如图所示,则V2O5分子中σ键和π键数目之比为。
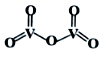
-
(2) Co(NH3)5Cl3是钴的一种配合物,中心离子的配位数为6,向100mL0.2mol·L-1该配合物的溶液中加入足量AgNO3溶液,生成5.74g白色沉淀。
①
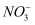 的空间构型为。
的空间构型为。 ②则该配合物中配离子的化学式为。
-
(3) ZnF2是生成良好的光学基质材料KZnF3的原料,ZnF2、KZnF3两种晶体的晶胞结构如图所示:
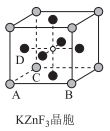
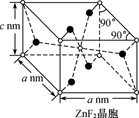
①已知:ZnF2的熔点为872℃,ZnCl2的熔点为275℃,ZnBr2的熔点为394℃,ZnBr2的熔点高于ZnCl2的原因为。
②KZnF3晶体(晶胞顶点为K+)中,与Zn2+最近且等距离的F-数为。
③若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为g/cm3(用含a、c、NA的代数式表示)。
-
(1) 太阳能电池板主要材料为单晶硅或多晶硅。Si的最外层电子排布式为,已知3种原子晶体的熔点数据如下表:
金刚石
碳化硅
晶体硅
熔点/℃
>3550
2600
1415
金刚石熔点比晶体硅熔点高的原因是。
-
(2) CS2是一种重要的化工原料。工业上可以利用硫(S8)与CH4为原料制备CS2 , S8受热分解成气态S2 , 发生反应2S2(g)+CH4(g)
 CS2(g)+2H2S(g),CS2分子的空间构型为,用燃煤废气(含N2、O2、SO2、CO2、H2O、NOx等)使尾气中的H2S转化为单质硫,可实现废物利用,保护环境,写出其中一个反应的化学方程式。
CS2(g)+2H2S(g),CS2分子的空间构型为,用燃煤废气(含N2、O2、SO2、CO2、H2O、NOx等)使尾气中的H2S转化为单质硫,可实现废物利用,保护环境,写出其中一个反应的化学方程式。
-
(3) 中国传统的农具、兵器曾大量使用铁,铁器的修复是文物保护的重要课题。铁器表面氧化层的成分有多种,性质如下:
成分
Fe3O4
FeO(OH)
FeOCl
性质
致密
疏松
疏松
在有氧条件下,Fe3O4在含Cl–溶液中会转化为FeOCl,将相关反应的离子方程式补充完整,4Fe3O4 +O2 + +H2O→FeOCl + , 若4mol Fe3O4完全转化为FeOCl,则转移的电子数目为。
-
(4) 化学修复可以使FeOCl转化为Fe3O4致密保护层:用Na2SO3和NaOH混合溶液浸泡锈蚀的铁器,一段时间后取出,再用NaOH溶液反复洗涤。
①FeOCl在NaOH的作用下转变为FeO(OH),推测溶解度FeOClFeO(OH)(填“>”或“<”)。
② Na2SO3的作用是。
③ 检验FeOCl转化完全的操作和现象是。
-
(1) 一些氧化物的熔点如表所示:
氧化物
Li2O
MgO
P4O6
SO2
熔点/℃
1570
2800
23.8
-75.5
解释表中氧化物之间熔点差异的原因:。
-
(2) Cr2O
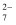 的结构如图所示。则该离子中σ键与π键的个数比为。
的结构如图所示。则该离子中σ键与π键的个数比为。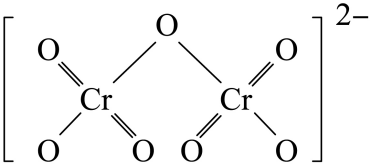
-
(3) [Cr(NH3)3(H2O)2Cl]2+中配体分子NH3、H2O的空间结构和相应的键角如图所示。
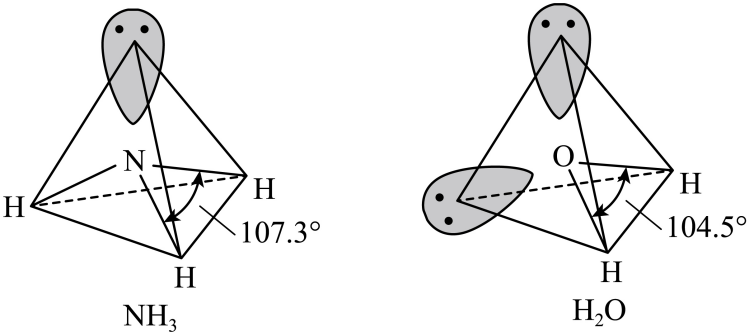
H2O的键角小于NH3的键角,原因是。
-
(4) 钛某配合物可用于催化环烯烃聚合,其结构如图所示。
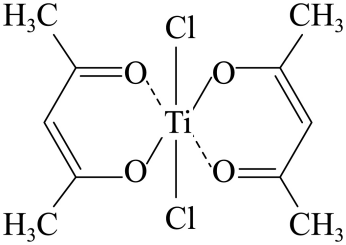
该配合物中存在的化学键有____(填字母代号)。
A . 离子键 B . 配位键 C . 金属键 D . 共价键 E . 氢键 -
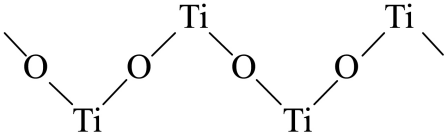
(5) 已知TiO2与浓硫酸反应生成硫酸氧钛,硫酸氧钛晶体中阳离子为链状聚合形式的离子,结构如图所示,该阳离子的化学式为,阴离子的空间构型为。
-
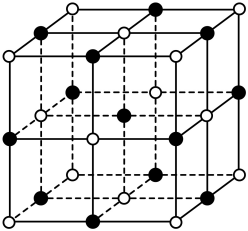
(6) 已知TiN晶体的晶胞结构如图所示,若该晶胞中Ti原子与N原子的最近距离为apm,阿伏加德罗常数的值为NA , 则晶胞的密度为g·cm-3。[M(TiN)=62g·mol-1 , 用含a、NA的代数式表示]。
-
(1) 某浓度的HF溶液中,氟化氢主要以(HF)2缔合形式存在。使氟化氢分子缔合的作用力是;气态氟化氢分子的热稳定性大于氯化氢的原因是。
-
(2) 氯元素有多种含氧酸根离子。
 中氯原子的杂化类型为,
中氯原子的杂化类型为,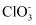 的空间结构为。
的空间结构为。
-
(3) 几种卤化锌的熔点见表:
物质

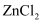
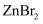
熔点/℃
872
283
x
则x(填“大于”或“小于”)283,
 熔点远高于
熔点远高于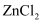 , 原因为。
, 原因为。 -
(4) 2-碘酰基苯甲酸是典型的高价碘试剂,在有机合成中用作氧化剂,结构如图:
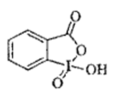
其分子中
 键个数为,基态碘原子的价电子轨道式为。
键个数为,基态碘原子的价电子轨道式为。
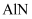 、
、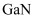 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在
属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在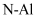 键、
键、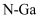 键。下列说法错误的是( )
键。下列说法错误的是( )
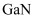 的熔点高于
的熔点高于 B . 晶体中所有化学键均为极性键
C . 晶体中所有原子均采取
B . 晶体中所有化学键均为极性键
C . 晶体中所有原子均采取 杂化
D . 晶体中所有原子的配位数均相同
杂化
D . 晶体中所有原子的配位数均相同
 B . 最简单氢化物的稳定性:W>Z>Y
C .
B . 最简单氢化物的稳定性:W>Z>Y
C .  和
和 分子的VSEPR模型不同
D . 工业上通常利用电解熔融XW的方法来制备X的单质
分子的VSEPR模型不同
D . 工业上通常利用电解熔融XW的方法来制备X的单质
- 下列混合气体不论它们的组分以何种比例混合,只要总质量一定,经过完全燃烧后,产生的CO2为一定量的是A.丙烯和乙烯 B
- 阅读下面的文字,完成1―3题。古汉字的形声相益世界上古史与现代考古学的研究成果表明:文明发达较早地区产生的一些古老文字系
- 如图所示的电场中正、负电荷的电荷量相等,电场中有相互对称分布的a、b两点(a、b两点到o点的距离相等),a、b两点在两电
- 如图所示过程中,只发生物理变化的是() A. 燃放烟花 B. 光合作用 C. 冰山
- 2008年9月,三鹿牌奶粉重大食品安全事故发生,造成大量婴幼儿住院治疗。事件发生后,党中央、国务院高度重视,立即启动国家
- 区分横波和纵波是根据( ) A.沿水平方向传播的叫做横波 B.质点振动的方
- 下列各表述与示意图一致的是 A.图①表示25℃时,用0.1 mol·L-1盐酸滴定10
- 秦朝修建咸阳,运用了天体观念。把渭河比作银河“天汉”,把各座宫殿比作星座,咸阳宫居中,四周有许多通道,形成了众星拱辰、屏
- 下列关于合金的说法不正确的是A.合金的硬度大于组成它的纯金属的硬度B.合金的熔点高于组成它的纯金属的熔点C.在金属中加热
- 实验室用硝酸钾配制50.0 g溶质的质量分数为20%的硝酸钾溶液, 下列说明正确的是 A.用托盘天平称取5.0 g硝酸钾
- —Jason, do you know a famous band called the Monkees ?
- 下列关于细胞结构和功能的叙述中,正确的是 A.精子细胞、神经细胞、根尖分生区细胞不是都有细胞周期,但化学成分却都不断更新
- (08广西柳州北海)以下实例,力对物体做功的是 A.举重运动员举着杠铃不动 B.小明将水桶从地面上提起 C.吊车吊
- 小明在向别人介绍日本时,有如下一些表述,其中正确的是A.日本是一个海陆兼备的国家B.日本很少有地震、火山活动C.日本是一
- 下列说法错误的是( ) A. 线粒体是有氧呼吸的主要场所,葡萄糖不能进入线粒体可能由于膜上缺少葡萄糖载体 B. D
- 如图在边长为1的小正方形网格中,A、B、P、Q四点均在正方形网格的格点上,线段AB、PQ相交于点M,则线段AM的长为__
- 2.下列各句中,没有错别字的一项是( ) A.不要问我为何飘泊异乡,有水的地方是家的方向;不要问我到过多少
- 子弹以900m/s的速度从枪筒射出,汽车在北京长安街上行使,时快时慢,20min行使了18km,汽车行驶的速度是54km
- 血燕是燕窝中的极品,营养价值极高,价值千金,但数量稀有。目前国内市场上的血燕大多是人造血燕。浙江省工商局发布的抽检报告显
- 下列加点的熟语使用不正确的一项是 A.一部作品,开头和中段尽管精彩,结尾贫弱,就成了狗尾续貂,令人扼腕。 B.福利彩票投



