金属晶体 知识点题库
下列事实中,一般不能用于判断金属性强弱的是( )
A . 金属间发生的置换反应
B . 1mol金属单质在反应中失去电子的多少
C . 金属元素的最高价氧化物对应水化物的碱性强弱
D . 金属元素的单质与水或酸置换出氢的难易程度
下列说法错误的是( )
A . 在金属晶体中有阳离子无阴离子
B . 金属晶体通常具有良好导电性、导热性和延展性
C . 金属晶体中存在共价键
D . 分子晶体的熔、沸点与化学键无关
某物质的熔融状态可导电,固态能导电,将其投入水中后水溶液也可导电,则该物质可能是( )
A . 金刚石
B . NaOH
C . 金属晶体
D . 分子晶体
下列不属于金属晶体共性的是( )
A . 易导电
B . 易导热
C . 有延展性
D . 高熔点
下列有关金属晶体的判断正确的是( )
A . 简单立方堆积、配位数6、空间利用率68%
B . 体心立方堆积、配位数6、空间利用率68%
C . 六方最密堆积、配位数8、空间利用率74%
D . 面心立方最密堆积、配位数12、空间利用率74%
Cu2O在稀硫酸中生成Cu和CuSO4 , 铜晶胞结构如图所示,铜晶体中每个铜原子周围距离最近的铜原子数目为
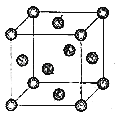
金属的性质与其结构有密切的关系,金属晶体由于某些结构上的相似点导致了金属具有一些共同的性质;同样由于结构上的不同点,导致了每种金属都具有各自的特性.
-
(1) 请指出金属具有延展性的原理是
-
(2) 金属的紧密堆积有不同的形式,请画出金属钠的晶胞,并指出一个晶胞含有几个钠原子?
-
(3) 计算该晶胞的空间利用率?
你认为下列对化学知识概括合理的组合是( )
①金属晶体中存在离子,但却不存在离子键
②原子晶体、离子晶体、金属晶体、分子晶体中都一定存在化学键
③原子晶体硬度一般比分子晶体大,分子晶体熔点不一定比金属晶体低
④固态能导电的一定是金属晶体
⑤NF3的沸点比NH3的沸点低是因为N﹣F比N﹣H键的键能小
⑥原子晶体一定由原子构成,由原子构成的晶体不一定是原子晶体
⑦共价化合物中可能含有离子键
⑧金属晶体中简单立方堆积的配位数是8,空间利用率最低.
A . 只有②③④
B . 只有②③⑦
C . 只有①③⑥
D . 只有⑤⑥⑧
下列有关金属的说法正确的是( )
A . 金属原子的核外电子在金属晶体中都是自由电子
B . 金属晶体是由金属阳离子和自由电子通过金属键而形成
C . 金属原子在化学变化中失去的电子数越多,其还原性越强
D . 金属导电的实质是金属阳离子在外电场作用下的定向移动
下列有关晶体的说法中一定正确的是( )
①原子晶体中只存在非极性共价键
②稀有气体形成的晶体属于原子晶体
③干冰晶体升华时,分子内共价键会发生断裂
④金属元素和非金属元素形成的化合物一定是离子化合物
⑤分子晶体的堆积均为分子密堆积
⑥离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键
⑦金属晶体和离子晶体都能导电
⑧依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体
A . ①③⑦
B . ⑥
C . ②④⑤⑦
D . ⑤⑥⑧
下图为金属铜的晶胞,请完成以下各题。
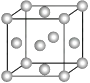
-
(1) 该晶胞“实际”拥有的铜原子是个。
-
(2) 该晶胞称为 (填序号)。A . 六方晶胞 B . 体心立方晶胞 C . 面心立方晶胞
-
(3) 铜晶体的堆积方式称为最密堆积,配位数为。
-
(4) 此晶胞立方体的边长为a cm,Cu的相对原子质量为64,金属铜的密度为ρ g·cm-3 , 则阿伏加德罗常数为(用a、ρ表示)。
下列对各组物质性质的比较中,正确的是( )
A . 熔点:Li<Na<K
B . 导电性:Ag>Cu>Al>Fe
C . 密度:Na>Mg>Al
D . 空间利用率:体心立方堆积<六方最密堆积<面心立方最密堆积
下列关于金属晶体的叙述正确的是( )
A . 用铂金做首饰不能用金属键理论解释
B . 固态和熔融时易导电,熔点在1000℃左右的晶体可能是金属晶体
C . 金属晶体最密堆积方式只有面心立方堆积方式
D . 金属导电和熔融电解质(或电解质溶液)导电的原理一样。
在下列有关晶体的叙述中错误的是( )
A . 离子晶体中,一定存在离子键
B . 原子晶体中,存在共价键
C . 金属晶体的熔沸点均很高
D . 稀有气体的原子能形成分子晶体
构成金属晶体的基本微粒是( )
A . 分子
B . 原子
C . 阳离子与阴离子
D . 阳离子与自由电子
四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是( )
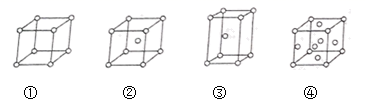
A . 金属Zn采用②堆积方式
B . ①和③中原子的配位数分别为:6、8
C . 对于采用②堆积方式的金属的晶胞质量为  g
D . 金属锻压时,会破坏密堆积的排列方式
g
D . 金属锻压时,会破坏密堆积的排列方式
 g
D . 金属锻压时,会破坏密堆积的排列方式
g
D . 金属锻压时,会破坏密堆积的排列方式
已知钼(Mo)的晶胞如图所示,钼原子半径为a pm,相对原子质量为M,以NA表示阿伏加德罗常数的值。
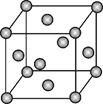
-
(1) 钼晶体的堆积方式为,晶体中粒子的配位数为。
-
(2) 构成钼晶体的粒子是,晶胞中所含的粒子数为。
-
(3) 金属钼的密度为g·cm-3。
金晶体的晶胞如图所示,设金原子的直径为d,用NA表示阿伏加德罗常数,在立方体的各个面的对角线上,3个金原子彼此两两相切,M表示金的摩尔质量。则下列说法错误的是( )

A . 金晶体每个晶胞中含有4个金原子
B . 金属键无方向性,金晶体属于最密堆积
C . 晶体中金原子的配位数是12
D . 一个晶胞的体积是 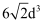
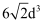
下列叙述错误的是( )
A . 构成金属的粒子是金属阳离子和自由电子
B . 金属晶体内部都有自由电子
C . 金属晶体内自由电子分布不均匀,专属于某个特定的金属离子
D . 同一类晶体间熔点(或沸点)相差最大的是金属.晶体
-
(1) Ⅰ.铁是地壳中含量第二位的金属元素,其单质、合金及众多的化合物在生产生活中都有广泛的应用,请回答下问题:
写出铁元素在周期表中的位置:;写出Fe2+的价电子排布式。
-
(2) 某种铁的化合物俗称“绿矾”,化学式为FeSO4•7H2O,“绿矾”中SO
 的空间构型为(用文字描述),其中S的杂化轨道类型为。
的空间构型为(用文字描述),其中S的杂化轨道类型为。
-
(3) Ⅱ.铁能形成多种配合物,其中一种配合物Fe(CO)5的熔点为-20℃,沸点为103℃,可用于制备纯铁,请回答下列问题:
Fe(CO)5晶体类型属于晶体,配体为:。
-
(4) 价电子数和原子数相同的分子、离子或原子团互称为等电子体,往往具有相似的化学键和构型,请写出与CO互为等电子体的一种阴离子的电子式:。
-
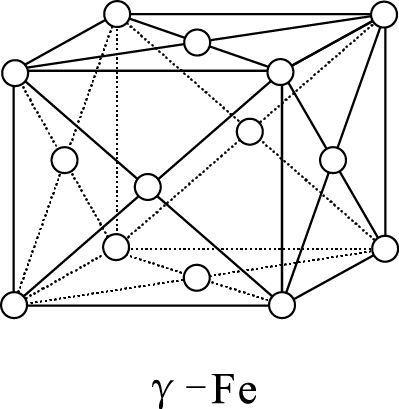
(5) γ—Fe晶体的晶胞为立方晶胞,结构如图所示,其晶胞边长为apm,则γ—Fe单质的密度为g/cm3(设NA为阿伏加德罗常数的值,列出算式即可)
最近更新
- 我国满族人的祖先是 ( )A. B.回纥 C.吐蕃
- 某有机物的结构简式如图:则此有机物可发生的反应类型有:①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和() A.仅
- 引入“总电阻”概念时运用的科学方法是______________(选填“等效替代”或“控制变量”)法。阻值为10Ω和40
- 有关乙炔分子中的化学键描述不正确的是 A.两个碳原子采用sp杂化方式 B. 两个碳原子采用
- 2015年10月,我国科学家屠呦呦因发现并研究青蒿素(化学式C15H22O5)治疗疟疾的成果而被授予诺贝尔生理学或医学奖
- 《得道多助,失道寡助》一文中,指出决定战争胜负的三要素及其关系的句子是:“ ,
- 放在水平地面上的物体受到水平拉力的作用,在0—6 s内速度与时间和拉力的功率与时间图象如图所示,则物体的质量为_____
- 下列成语出自淝水之战的有 () ①风声鹤唳 ②三顾茅庐 ③纸上谈兵 ④
- 阅读下面一段文字,回答后面的问题(6分) 生长在非洲荒漠地带的依米花,默默无闻,许多旅人以为它只是一株草而已。但是,它会
- 乙炔(C2H2)是一种难溶于水、密度比空气略小,在实验室里,实验室制取乙炔应选择的最佳收集装置是() A.排水法 B
- 奉献是一种精神。我们可用“ , ”来颂扬这种精神。
- 某容器真空时,称量其质量为60.4g,此容器充满N2时总质量为66.0g,在相同状况下,充满另一气体时,总质量为70g,
- 妈妈烘培蛋糕时散发出阵阵香味,说明分子具有的性质是() A.分子体积很小 B.分子间间隔很小 C.分
- 现代科技的高度快速发展离不开C和Si元素。 (1)写出Si的基态原子核外电子排布式__________________。
- 下列各组词语中没有错别字的一项是( ) A.疏浚 竣工以儆效尤不能越雷池一步 B.奖掖 赋与翻然醒悟小不忍
- 默写填空(8分) ① 子曰:“_______________,可以为师矣。”(《<论语>十则》)②
- 下列关于碳和碳的氧化物的说法中不正确的是( ) A.金刚石、石墨和C60都是由碳元素组成的单质 B.金刚石和石墨的结构
- 某河道两旁有甲、乙两个化工厂。它们排放的澄清工业废水中,共含有Na+、Ag+、Fe3+、C1-、OH- 、NO3- 六种
- 2009年10月16日上午,海峡两岸环渤海经贸合作论坛在南开大学举行。出席论坛的有关专家表示,继珠江三角洲、长江三角洲经
- 《资治通鉴》记载:西汉初期,匈奴“往往入盗于汉边,不可胜数,然尚贪乐关市(边境贸易),嗜汉财务,汉亦关市不绝,以中其意”



