原子核外电子的跃迁及应用 知识点
原子核外电子的跃迁及应用:核外电子离核越远,能量越高,当电子吸收能量后,会从能量低的能级跃迁到能量高的能级上,然后会自发的从高能级上跃迁到低能级上以光子的形式释放能量。这也焰色反应的实质,由于金属元素原子焰色反应不同而进行鉴别所含元素。
原子核外电子的跃迁及应用 知识点题库
当镁原子由1s22s22p63s2→1s22s22p63p2时,以下认识正确的是( )
A . 镁原子由基态转化成激发态,这一过程中吸收能量
B . 镁原子由激发态转化成基态,这一过程中释放能量
C . 转化后位于p能级上的两个电子处于同一轨道,且自旋方向相同
D . 转化后镁原子与硅原子电子层结构相同,化学性质相似
对充有氖气的霓红灯管通电,灯管发出红色光.产生这一现象的主要原因( )
A . 电子由激发态向基态跃迁时以光的形式释放能量
B . 电子由基态向激发态跃迁时吸收除红光以外的光线
C . 氖原子获得电子后转变成发出红光的物质
D . 在电流作用下,氖原子与构成灯管的物质反应
电子由3d能级跃迁至4p能级时,可通过光谱仪直接摄取( )
A . 电子的运动轨迹图象
B . 原子的吸收光谱
C . 电子体积大小的图象
D . 原子的发射光谱
以下现象与核外电子的跃迁有关的是( )
①霓虹灯发出有色光;
②棱镜分光;
③激光器产生激光;
④石油蒸馏;
⑤凸透镜聚光;
⑥燃放的焰火,在夜空中呈现五彩缤纷;
⑦日光灯通电发光;
⑧冷却结晶;
⑨焰色反应.
A . ②④⑤⑧⑨
B . ①③⑥⑦⑨
C . ①③⑤⑥⑦
D . ①②③⑤⑥⑦
电子由3d能级跃迁至4p能级时,可通过光谱仪直接摄取到( )
A . 电子的运动轨迹图像
B . 原子的吸收光谱
C . 电子体积大小的图像
D . 原子的发射光谱
以下对核外电子运动状态的描述正确的是( )
A . 电子的运动与行星相似,围绕原子核在固定的轨道上高速旋转
B . 能量低的电子只能在s轨道上运动,能量高的电子总是在f轨道上运动
C . 能层序数越大,s电子云的半径越大
D . 在同一能级上运动的电子,其运动状态肯定相同
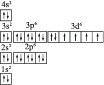
以下是表示铁原子和铁离子的3种不同化学用语。
结构示意图 | 电子排布式 | 电子排布图 | |
铁 原 子 | | 1s22s22p63s23p63d64s2 |
|
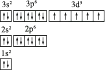
铁 离 子 |
| 1s22s22p63s23p63d5 |
|
-
(1) 铁原子最外层电子数为,铁在发生化学反应时,参加反应的电子可能是。
-
(2) 请你通过比较、归纳,分别说出3种不同化学用语所能反映的粒子结构信息。
-
(1) 许多金属元素有焰色反应,金属存在焰色反应的原因是。
-
(2) 基态铝原子中,有种电子运动状态,其中p轨道的电子云轮廓图的形状为。
-
(3) 我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。
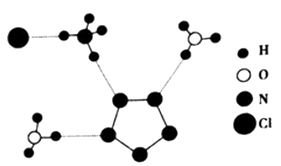
①图中R中阳离子是(填写化学式),相对分子质量较大的阳离子中心原子的杂化类型是。
②图中R中阴离子N5-中的σ键总数为个。分子中的大π键可用符号
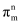 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为  ),则N5- 中的大π键应表示为。
),则N5- 中的大π键应表示为。 -
(4) 氮与铝之间形成化合物X,具有耐高温抗冲击等性能。X的晶体结构如图所示。
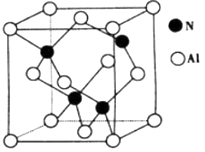
①已知氮化硼与X晶体类型相同,推测氮化硼的熔点比X的熔点(填“高”、“低“ ) ,可能的原因是。
②若X的密度为ρg·cm-3 , 则晶体中最近的两个Al原子的距离为cm。(阿伏加德罗常数的值用NA表示)
下列原子的电子跃迁能释放光能形成发射光谱的是( )
A . 1s22s22p63s2→1s22s22p63p2
B . 1s22s22p33s1→1s22s22p4
C . 1s22s2→1s22s12p1
D . 1s22s22p1x →1s22s22p1 y
下列有关叙述中正确的是( )
A . 原子轨道和电子云都是用来形象地描述电子运动状态的
B . 因为 s 轨道的形状是球形的,所以 s 电子做的是圆周运动
C . 3px、3py、3pz 的差异之处在于三者中电子(基态)的能量不同
D . 电子云图上的每一个点都代表一个电子
下列发生的现象与电子的跃迁无关的是( )
A . 燃放焰火 B . 霓虹灯广告
B . 霓虹灯广告 C . 燃烧蜡烛
C . 燃烧蜡烛 D . 平面镜成像
D . 平面镜成像
 B . 霓虹灯广告
B . 霓虹灯广告 C . 燃烧蜡烛
C . 燃烧蜡烛 D . 平面镜成像
D . 平面镜成像
当碳原子的核外电子排布由1s22s22p2 转变为1s2s12p3时(能级上的数字代表该能级的电子数),下列说法正确的是( )
A . 碳原子由基态变为激发态
B . 碳原子由激发态变为基态
C . 该过程将产生吸收光谱
D . 碳原子要向外界环境释放能量
Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题: .
-
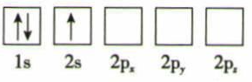
(1) 下列Li原子电子排布图表示的状态中,能量最低和最高的分别为、(填序号)。
A.
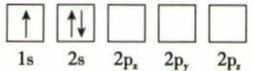
B.
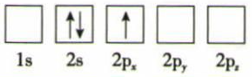
C.
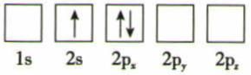
D.
-
(2) Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是。
下列有关原子光谱的说法中,错误的是( )
A . 通过光谱分析可以鉴定某些元素
B . 电子由低能级跃迁至较高能级时,一定发生的是化学变化
C . 燃放的焰火在夜空中呈现五彩缤纷的礼花与原子核外电子的跃迁有关
D . 原子中的电子在跃迁时能量的表现形式之一是光,这也是原子光谱产生的原因
下列有关叙述不正确的是( )
A . 分子、原子和离子是构成物质的基本微粒
B . 带有单电子的原子或原子团是自由基
C . 一个非可逆化学反应是一个基元反应
D . 处于最低能量状态的原子是基态原子
中国科学家经过光谱分析发现了一颗锂元素含量极高的恒星。下列说法不正确的是( )
A . LiOH的碱性弱于Be(OH)2
B . 在碱金属元素中,锂元素的第一电离能最大
C . 依据对角线规则,锂元素和镁元素的有些性质相似
D . 原子光谱的产生与电子跃迁有关,可利用原子光谱中的特征谱线来鉴定锂元素
由中国工程物理研究院应用电子学研究所牵头负责的高平均功率太赫兹自由电子激光装置(简称CTFEL装置)首次饱和出光并实现稳定运行。这标志着我国太赫兹源正式进入自由电子激光时代。下列有关原子核外电子跃迁说法正确的是( )
A . 电子仅在激发态跃迁到基态时才会产生原子光谱
B . 元素钾的焰色呈紫色,紫色对应的辐射波长在可见光中是最长的
C . 激光、烟火、霓虹灯光的产生都与原子核外电子跃迁释放能量有关
D . 对充有氖气的霓虹灯管通电,灯管发出的红色光是电子由基态向激发态跃迁时吸收除红光以外的光线而产生
信息、材料和能源是现代社会赖以发展维系的基础,这些都是化学的重要研究领域。能量的研究不仅仅包括宏观物质的能量变化,也包括微观粒子的能量研究,下列说法正确的是( )
A . 激光的产生、焰色反应和荧光现象都存在核外电子跃迁过程
B . Co原子第4能层中的电子能量一定比第3能层中的能量高
C .  比
比 的热稳定性好的原因是
的热稳定性好的原因是 分子之间存在氢键,而破坏氢键需要吸收能量
D .
分子之间存在氢键,而破坏氢键需要吸收能量
D . 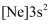 、
、 和
和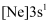 三种状态的Mg中,失去最外层一个电子所需能量最少的是
三种状态的Mg中,失去最外层一个电子所需能量最少的是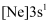
 比
比 的热稳定性好的原因是
的热稳定性好的原因是 分子之间存在氢键,而破坏氢键需要吸收能量
D .
分子之间存在氢键,而破坏氢键需要吸收能量
D . 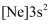 、
、 和
和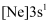 三种状态的Mg中,失去最外层一个电子所需能量最少的是
三种状态的Mg中,失去最外层一个电子所需能量最少的是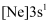
[化学——选修3:物质结构与性质]
卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
-
(1) 氟原子激发态的电子排布式有,其中能量较高的是。(填标号)
a.
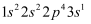 b.
b. c.
c. d.
d.
-
(2) ①一氯乙烯
 分子中,C的一个杂化轨道与
分子中,C的一个杂化轨道与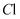 的
的 轨道形成
轨道形成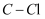 键,并且
键,并且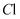 的
的 轨道与C的
轨道与C的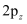 轨道形成3中心4电子的大
轨道形成3中心4电子的大 键
键 。
。②一氯乙烷
 、一氯乙烯
、一氯乙烯 、一氯乙炔
、一氯乙炔 分子中,
分子中,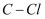 键长的顺序是,理由:(ⅰ)C的杂化轨道中s成分越多,形成的
键长的顺序是,理由:(ⅰ)C的杂化轨道中s成分越多,形成的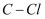 键越强;(ⅱ)。
键越强;(ⅱ)。 -
(3) 卤化物
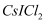 受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为。解释X的熔点比Y高的原因。
受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。X为。解释X的熔点比Y高的原因。
-
(4)
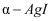 晶体中
晶体中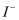 离子作体心立方堆积(如图所示),
离子作体心立方堆积(如图所示),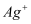 主要分布在由
主要分布在由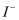 构成的四面体、八面体等空隙中。在电场作用下,
构成的四面体、八面体等空隙中。在电场作用下,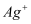 不需要克服太大的阻力即可发生迁移。因此,
不需要克服太大的阻力即可发生迁移。因此,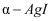 晶体在电池中可作为。
晶体在电池中可作为。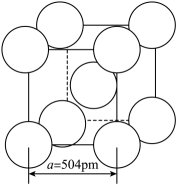
已知阿伏加德罗常数为
 , 则
, 则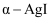 晶体的摩尔体积
晶体的摩尔体积
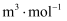 (列出算式)。
(列出算式)。
下列有关原子结构的说法正确的是( )
A . 霓虹灯发光与原子核外电子跃迁释放能量有关
B . 氖原子与钠离子两粒子的2p能级上的电子离核的距离相同
C . M能层中有3s、3p、3d、3f四个能级,共16个轨道
D . 基态镁原子核外电子的轨道表示式为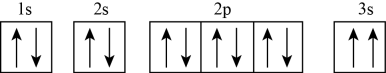

最近更新
- 下列物质能使品红褪色的是①活性炭 ②过氧化钠 ③氯水 ④二氧化硫 ⑤臭氧A.
- 对文章的理解,不正确的两项是( ) A.孟子认为只有实行“仁政”,才能以“王道”统一天下。 B.“狗彘食人食而不知
- 下面一段文字中,画有横线的句子,如果用最简单通俗的语言来表达的话,你将如何表述 ?( 表述的文字不超过 20 个字 )
- 下图为某些概念间的相互关系,下列概念与a、b、c、d、e依次相对应的一组是A.个体、系统、器官、组织、细胞 B.能量供应
- 读下列有关瑞士的图文资料,回答问题。材料一:2010年上海世博会的瑞士国家馆(右囤)主体结构由两个承重的大小圆柱组成,左
- ......
- 下列关于美国独立战争和美园内战相同点的归纳,不正确的是 A.引起战争的经济原因都与英国有关 B.都是资
- 集合A={N}的真子集的个数是 A.1
- 读图,回答下列各题。甲、乙、丙、丁四地中最有可能形成瀑布的是 A.甲 B.乙
- 6.对下面句子中加线词的用法判断正确的一项是( ) ①苏子与客泛舟游于赤壁之下 ②此非孟德之困于周郎者乎
- (本题满分12分)已知抛物线的焦点为,过作两条互相垂直的弦、,设、 的中点分别为、.(1)求证直线恒过定点; (2)求的
- 下列实验现象描述正确的是( ) A.磷在空气中燃烧,产生大量的烟雾 B.电解水的实验中,负极产生的气体能使带火星的木
- 随着现代天文学家的发展,天体位置历表的精度不断提高,只要能算出太阳、月球和地球这三者在某时刻的相对位置,就能精确预报日、
- It seems today more and more girls like to dress like boys.
- 如图所示,Q1、Q2为两个固定点电荷,其中Q1带正电,它们连线的延长线上有a、b两点。一正试探电荷以一定的初速度沿直线从
- Welcome to the Amazing kids Website! Here you can read about
- 在密闭容器中A与B反应生成C,其反应速率分别为v(A)、v(B)、v(C)表示。已知v(A)、v(B)、v(C)之间有以
- 误食亚硝酸钠会造成人畜中毒。亚硝酸钠像食盐一样有咸味,但有很强的毒性。实验证明,它还有很强的氧化性。(1)已知亚硝酸钠溶
- 小麦植株中能使ADP含量增加的是( ) ①产生O2的过程 ②叶绿体中[H]被消耗的过程 ③线粒体中[H]
- 学习了二氧化锰对过氧化氢分解有催化作用的知识后,某兴趣小组同学在课外进行了有关过氧化氢分解反应的再探究。 【探究一】影响