原子核外电子的跃迁及应用 知识点题库
①霓虹灯发出有色光
②棱镜分光
③激光器产生激光
④石油蒸馏
⑤凸透镜聚光
⑥燃放的焰火在夜空中呈现五彩缤纷的礼花
⑦日光灯通电发光
⑧冷却结晶.
元素代号 | Y | X | W | M | Z |
原子半径(×10﹣12m) | 64 | 73 | 78 | 96 | 113 |
主要化合价 | ﹣1 | +5、﹣3 | +7、﹣1 | +4、﹣4 | +3 |
(1)下列现象和应用与电子跃迁无关的是 .
A.激光 B.焰色反应 C.原子光谱 D.燃烧放热 E.石墨导电
(2)A、B两种短周期元素,A是原子半径最小的元素,B原子最外层电子数是次外层的两倍.某平面正六边形分子由A、B两种元素组成且原子个数比为1:1,该分子中含有 个σ键.
(3)元素铬化合物(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应.
①与铬同周期的基态原子中最外层电子数与铬原子相同的元素有 (填元素符号)
②在a:苯 b:CH3OH c:HCHO d:CS2 e:CCl4五种有机溶剂中,碳原子采取sp3杂化的分子有 (填字母),CS2分子的键角是 .
③过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色.据此判断,[Mn(H2O)6]]2+ (填“无”或“有”)颜色
(4)请写出HClO的电子式: ;在下图配合物离子[Cu(NH3)4]2+中的画出配位键: 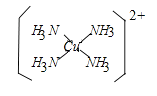
(5)A、B均为短周期金属元素.依据下表数据和已学知识,
电离能/KJ•mol﹣1 | I1 | I2 | I3 | I4 |
A | 932 | 1821 | 15390 | 21771 |
B | 738 | 1451 | 7733 | 10540 |
判断金属B的价电子电子排布式 ,写出金属B与二氧化碳反应的化学方程式:
-
(1) 福州大学王新晨教授以氨基氰(CH2N2)为原料制得类石墨相氮化碳(g-C3N4),其单层结构如图1。
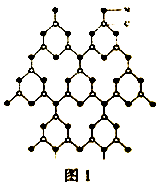
①氨基氰CH2N2)分子中C、N 原子均满足8电子稳定结构,则该分子的结构式为;该分子为(填“极性”或“非极性”)分子。
②氨基氰易溶于水或乙醇,其主要原因是。
③关于g- C3N4的叙述正确的是。
A.电负性:C>N
B.该物质的熔点比石墨更高
C.该物质属于原子晶体
D.该物质中C和N原子均采取SP2杂化
-
(2) NH3与Zn2+可形成[Zn(NH3)6]2+离子,部分结构如图2。
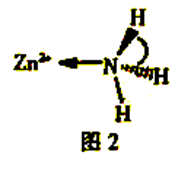
①NH3的空间构型为。
②[Zn(NH3)6]2+离子中存在的化学键类型有;NH3分子中H-N-H键角为107.3°,判断[Zn(NH3)6]2+离子中H-N-H 键角107.3°( 填">”、"<”或“=”)。
③肼(N2H4)可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。与N2H4互为等电子体的分子有。(写一种)
-
(3) N元素形成的简单离子N3-与Xn+形成的晶体的是立方体结构,边长为anm,如图3所示。
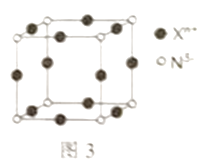
①Xn+中所有的电子恰好充满K、L、M 三个电子层,则基态X原子的价电子的轨道表示式为。
②已知该晶体的密度为5.84g·cm-3 , 则阿伏加德罗常数NA的计算表示式为(含a)。
-
(1) 聚四氟乙烯商品名称为“特氟龙”,可做不粘锅涂层。它是一种准晶体,该晶体是一种无平移周期序、但有严格准周期位置序的独特晶体。可通过方法区分晶体、准晶体和非晶体。
-
(2) 基态锑(Sb)原子价电子排布的轨道式为。[H2F]+[SbF6]—(氟酸锑)是一种超强酸,存在[H2F]+ , 该离子的空间构型为,依次写出一种与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是、。
-
(3) 硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序(填元素符号)。
②H3BO3本身不能电离出H+ , 在水中易结合一个OH﹣生成[B(OH)4]﹣ , 而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为。
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在(填序号):
A 离子键 B σ键 C π键 D 氢键 E 范德华力
-
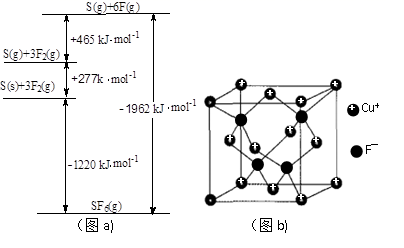
(4) SF6被广泛用作高压电气设备绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图(见图a)计算相联系的键能。则S—F的键能为kJ·mol-1。
-
(5) CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g·cm-3。
①CuF比CuCl熔点高的原因是;
② 已知NA为阿伏加德罗常数。CuF的晶胞结构如上“图b”。则CuF的晶胞参数a=nm (列出计算式)。

①氧原子的轨道表示式(电子排布图):![]() 违背了泡利不相容原理
违背了泡利不相容原理
②处于最低能量状态原子叫基态原子,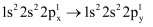 过程中形成的是发射光谱
过程中形成的是发射光谱
③1~36号元素中,基态原子的价电子层有3个未成对电子的元素有5种
④非极性分子中一定有非极性键,极性分子中一定有极性键
⑤金属键和氢键都有方向性和饱和性
⑥在有机化合物中,碳原子和碳原子之间形成的σ键比π键更牢固
 右上角的3表示该能级有3个轨道
D .
右上角的3表示该能级有3个轨道
D .  的VSEPR模型和离子的空间构型一致
的VSEPR模型和离子的空间构型一致
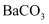 可作为造影剂用于X射线检查胃肠道疾病
D . 将硬水加热或向其中加入
可作为造影剂用于X射线检查胃肠道疾病
D . 将硬水加热或向其中加入 均可以降低硬水中
均可以降低硬水中 、
、 的浓度
的浓度
- 复数(为虚数单位),为的共轭复数,则下列结论正确的是 A. 的实部为 B. 的虚部为 C. D.
- 据了解,野生扬子鳄种群的雌雄比例一般稳定在5︰1左右,这样的性别比是由孵化时的温度所决定的;繁殖季节雄性扬子鳄发出“轰”
- 若,则的取值范围是( ) A. B. C.
- 下列各句中,加点的成语使用恰当的一句是 A.你们到北京去的事,让我去找领导也没有用,因为师出无名,让他怎么批呢? B.除
- 一个正方体的展开图如图所示,A、B、C、D为原正方体的顶点,则在原来的正方体中( ) A.AB∥CD B.
- 为迎接中招体育加试,需进一步了解九年级学生的身体素质,体育老师随机抽取九年级一个班共50名学生进行一分钟跳绳次数测试,
- 读读某区域经纬网图(图一)和地球公转(图二),完成下列各题。⑴A点的经纬度是______________,该点一年中有_
- A. recently B.affects C.pattern D.var
- 元素X的气态氢化物的化学式为H2X,则X最高价氧化物的水化物的化学式( ) A.H2XO3
- 下列溶液中各微粒浓度关系判定不正确的是A.10mL 0.2 mol·L-1的氨水与l0mL 0.1mol·L-1的盐酸充
- 北极地区的土著居民主要是( )人和( )人。
- 有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列事实不能说明上述观点的是
- 把长为8cm的矩形按虚线对折,按图中的虚线剪出一个直角梯形,找开得到一个等腰梯形,剪掉部分的面积为6cm2,则打开后梯形
- “穿花蛱蝶深深见,点水蜻蜓款款飞”的诗句分别描绘了这两类昆虫的()A.防御行为、取食行为B.防御行为、迁徙行为C.取食行
- 在Rt△ABC中,∠C=90°,AC=4,BC=3,则以2.5为半径的⊙C与直线AB的位置关系是__________.
- 我们的生活是由一个又一个日子组成的。寻常的日子似乎平静无波,单调无奇,但生活中总有一些日子注定会因为一些不寻常的事、不寻
- 据记载,在义和团运动时期,外国人被称为“大毛子”,一律杀无赦。中国人如信奉天主教、基督教,通被称为“二毛子”;其他通洋学
- 三个大小相等互成120°角的力F1=F2=F3=F,它们合成后合力大小是( ) A.0
- 将H2、N2、O2三种气体分别放入三个不同的密闭容器中,当它们的温度、密度完全相同时,这三种气体的压强P的大小顺序是A.
- 俄罗斯科学家用铪和钨两种核素精确测定了地球和月球的年龄,得出月球至少比地球早700万年形成,它们是根据Hf(铪-182)



