离子反应发生的条件 知识点题库
在复杂体系中,确认化学反应先后顺序有利于解决问题。下列反应先后顺序判断正确的是( )
A . 在含等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加入盐酸:AlO2-、Al(OH)3、OH-、CO32-
B . 在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2:I-、Br-、Fe2+
C . 在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2:KOH、Ba(OH)2、BaCO3
D . 在含等物质的量的Fe2+、Ag+、Cu2+、H+的溶液中加入Zn:Ag+、Cu2+、H+、Fe2+
现有五种溶液,分别含下列离子:①Ag+②Mg2+③Fe2+④Al3+⑤Fe3+ .
(1)写出符合下列条件的离子符号:
滴加氯水有明显现象的离子是 ,加铁粉后溶液增重的是 ;
(2)向③的溶液中滴加NaOH溶液,现象是 ,反应过程中属于氧化还原反应的化学方程式 .
如图中能表示将Ba(OH)2溶液逐滴加入到硫酸铝溶液中,产生沉淀的质量(W)与加入Ba(OH)2溶液的体积(V)关系的是( )
A . 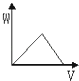 B .
B . 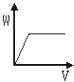 C .
C . 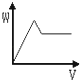 D .
D . 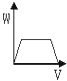
 B .
B .  C .
C .  D .
D . 
溶液X中含有右表离子中的某5种,且其浓度均为0.1mol/L(不考虑水的电离与离子水解).向X溶液加入足量稀盐酸,有无色气体生成,经分析反应前后阴离子种类没有变化.下列叙述不正确的是( )
阳离子 | 阴离子 |
Na+ Ca2+ Fe 2+ Al2+ Fe 3+ Mg3+ | OH﹣ HCO2﹣ CO32﹣ Cl﹣ NO3﹣ SO42﹣ |
A . X溶液中不可能含有HC03﹣或CO32﹣
B . 生成无色气体的离子方程式为:3Fe2++NO3﹣+4H+═3Fe3++NO+2H2O
C . 根据电荷守恒,原溶液中一定含Mg2+
D . X溶液中一定含3种阳离子、2种阴离子
已知电离平衡常数:K(H2CO3)>K(HClO)>K(HCO3﹣),氧化性:HClO>Cl2>Br2>Fe3+>I2 . 下列有关离子反应或离子方程式的叙述中正确的是( )
A . 向FeI2溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl﹣
B . 向溴水中加入足量氯化亚铁溶液能使溴水变成无色
C . 向NaClO溶液中通入少量二氧化碳的离子方程式:2ClO﹣+CO2+H2O=2HClO+CO32﹣
D . 能使pH试纸显深红色的溶液中,Fe3+、Cl﹣、Ba2+、Br﹣能大量共存
某无色溶液含有下列离子中的若干种:H+、NH4+、Fe3+、Ba2+、Al3+、Cl﹣、OH﹣、CO32﹣、NO3﹣ . 向该溶液中加入铝粉,只放出H2 , 则溶液中能大量存在的离子最多有( )
A . 3种
B . 4种
C . 5种
D . 6种
向 Ba(OH)2溶液中逐滴加入稀硫酸,请回答下列问题
-
(1) 写出反应的化学方程式
-
(2) 若缓慢加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似用图中曲线(填字母)表示
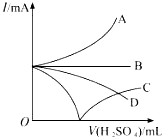
-
(3) 如果用盐酸代替稀硫酸,(填“能”或“不能”)观察到与(2)同样的实验现象,理由是
-
(4) 若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液的中央,如下图所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应.在此实验过程中,小球将(填字母)
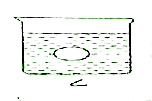
A.沉入水底 B 浮于水面 C 上下跳动.
在含有NH4+、Fe2+、Cu2+、SO32﹣的溶液中加入过量的过氧化钠,然后再加入过量的盐酸离子的物质的量不变的是( )
A . NH4+
B . Fe2+
C . Cu2+
D . SO32﹣
将单质Fe、Cu与含Fe3+、Fe2+、Cu2+的溶液一起放进某容器中,根据下列不同情况,填写金属或金属离子:
-
(1) 充分反应后,Fe有剩余,则容器内溶液中不可能有的离子;
-
(2) 充分反应后,如果容器内还有大量Fe3+ , 则容器中一定有的离子有,一定没有的金属有.
-
(3) 充分反应后,如果容器内有较多Cu2+和相当量的Cu,则容器内不可能有.
下列叙述正确的是( )
A . 将CO2通入BaCl2溶液中至饱和,无沉淀产生;再通入SO2 , 产生沉淀
B . 除去FeCl2中少量的FeBr2 , 加入适量氯水,再加四氯化碳萃取分液
C . 在稀硫酸中加入铜粉,铜粉不溶解;再加入KNO3固体,铜粉仍不溶解
D . 向AlCl3溶液中滴加1mol/L NaOH溶液10ml,产生白色沉淀;再加入1mol/L NaHSO4溶液10ml,沉淀恰好消失
氯化钡有剧毒,致死量为0.3g,万一不慎误服,应大量吞服鸡蛋清及适量解毒剂,此解毒剂是( )
A . AgNO3
B . CuSO4
C . MgSO4
D . Na2CO3
在某无色透明的酸性溶液中,能大量共存的离子组是( )
A . Na+ 、K+、SO42-、HCO3-
B . Cu2+、K+、SO42-、NO3-
C . Na+、 K+、Cl-、 NO3-
D . Fe3+、K+、SO42-、Cl-
下列物质①NaHSO4 ②HCl ③Cu ④CO2 ⑤Ba(OH)2 ⑥ NaOH ⑦ NaHCO3 ⑧CH3COOH
-
(1) 属于强电解质的是(填序号);
水溶液能导电的是(填序号)。
-
(2) 写出下列物质在水溶液中的电离方程式
①:
⑦:
⑧:
-
(3) 写出下列物质相互反应的离子方程式
少量的①与⑤:
⑥与⑧:
我国自主研制的C919大型客机的机身大量采用第三代铝锂合金减重并提高刚度。某铝锂合金成分(质量百分比)如下(Bal指剩余的百分含量):

| 成分 | Si | Fe | Cu | Mn | Mg | Zn | Ti | Li | Al |
| 含量 | 0.08 | 0.1 | 2.9~3.5 | 0.5 | 0.25~0.8 | 0.25 | 0.1 | 0.8~1.1 | Bal |
为了使合金具有高耐腐性能,通常先用酸腐蚀除去铝锂合金表面的氧化层,再进行氧化处理,并进行适当封闭,以提高合金表面耐腐蚀性能。仔细阅读上述信息,回答下列问题:
-
(1) 铝锂合金可用于制造飞机,铝锂合金材料的主要特点是。
-
(2) 铝元素原子核外有种不同运动状态的电子,最外层电子排布式为。
-
(3) 碱腐蚀工艺采用40~60g/L的NaOH溶液,在40~55℃下处理0.5~2min时间。写出碱腐蚀主要反应的化学方程式(写一个即可)。
-
(4) 镁与铝也是构成轻合金的两种常见金属,请从原子结构角度分析比较它们金属性的强弱
-
(5) 向镁铝合金滴入盐酸至恰好全部溶解,再逐渐滴入氢氧化钠溶液至过量,在滴氢氧化钠过程中观察到的现象有:;写出其现象中的一个离子方程式。
下列反应的离子方程式正确的是( )
A . 漂白粉溶液中通入过量的二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO
B . 铅蓄电池放电时的正极反应PbO2+2e-+4H+=Pb2++2H2O
C . 硫酸铝溶液中加入过量氨水3NH3·H2O+Al3+=Al(OH)3↓+3NH4+
D . 用过量FeBr2溶液吸收少量Cl2 Br-+Cl2=Br2+2Cl-
将浓度均为0.1 mol/L的三种溶液等体积混合,充分反应后没有沉淀的一组溶液是( )
A . BaCl2、NaOH、NaHCO3
B . Na2CO3、MgCl2、H2SO4
C . AlCl3、NH3·H2O、NaOH
D . Ba(OH)2、CaCl2、Na2SO4
-
(1) I、硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(2MgO·B2O3·H2O、SiO2及少量Fe3O4、CaCO3、Al2O3)为原料生产硼酸的工艺流程如下:
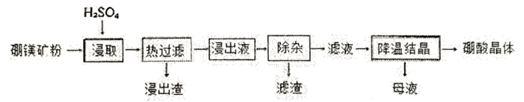
已知: H3BO3在20℃、40℃、60℃、100℃时溶解度依次为5.0g、8.7g、14.8g、40.2 g。
浸出渣除了CaSO4外,还有; (写化学式)
-
(2) “浸出液”显酸性,含H3BO3和Mg2+、SO
 , 还含有Fe3+、Fe2+、Ca2+、Al3+等杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO, 除去的杂质离子是; H2O2的作用是(用离子方程式表示)。
, 还含有Fe3+、Fe2+、Ca2+、Al3+等杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO, 除去的杂质离子是; H2O2的作用是(用离子方程式表示)。
-
(3) “浸取”后,采用“热过滤”的目的是
-
(4) 以硼酸为原料可制得硼氢化钠(NaBH4)它是有机合成中的重要还原剂,其电子式为
-
(5) II、为了分析矿石中铁元素的含量,先将浸出液处理,使铁元素还原成Fe2+ , 再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式:5Fe2+ + MnO
 + 8H+= 5Fe3+ + Mn2+ + 4H2O
+ 8H+= 5Fe3+ + Mn2+ + 4H2O 滴定前是否要滴加指示剂?(填“是”或“否");
-
(6) 达到滴定终点的标志是
-
(7) 某同学称取4.000g样品,经处理后在容量瓶中配制成100mL溶液,移取25.00mL试样溶液,用1.000×10-2mol/L KMnO4标准溶液滴定。达到滴定终点时消耗标准溶液20.00 mL, 则样品中铁元素的质量分数是
下列溶液混合后,不会发生离子反应的是( )
A . 硝酸钡溶液和硫酸钠溶液
B . 醋酸钠溶液和稀硫酸
C . 碳酸钾溶液和硫酸氢钠溶液
D . 硝酸钾溶液和氯化铜溶液
对于下列实验,不能正确表示其反应的离子方程式是( )
A . 向热KOH溶液中加入少量NH4HCO3粉末: 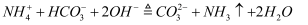 B . 向澄清石灰水中滴加Na2CO3溶液:Ca2++
B . 向澄清石灰水中滴加Na2CO3溶液:Ca2++  =CaCO3↓
C . 向FeCl3溶液中加入KI溶液:Fe3++2I-=Fe2++I2
D . 向NaClO溶液中滴加盐酸:ClO-+2H++Cl-=Cl2↑+H2O
=CaCO3↓
C . 向FeCl3溶液中加入KI溶液:Fe3++2I-=Fe2++I2
D . 向NaClO溶液中滴加盐酸:ClO-+2H++Cl-=Cl2↑+H2O
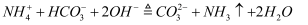 B . 向澄清石灰水中滴加Na2CO3溶液:Ca2++
B . 向澄清石灰水中滴加Na2CO3溶液:Ca2++  =CaCO3↓
C . 向FeCl3溶液中加入KI溶液:Fe3++2I-=Fe2++I2
D . 向NaClO溶液中滴加盐酸:ClO-+2H++Cl-=Cl2↑+H2O
=CaCO3↓
C . 向FeCl3溶液中加入KI溶液:Fe3++2I-=Fe2++I2
D . 向NaClO溶液中滴加盐酸:ClO-+2H++Cl-=Cl2↑+H2O
以下物质混合不能发生离子反应的是( )
A . CH3COONa 溶液与 HCl 溶液
B . MgCO3 沉淀与 NaOH 溶液
C . FeCl2 溶液与 KMnO4溶液
D . Na2CO3 溶液与 KOH 溶液
最近更新
- 已知圆锥外切于半径为1的球,求当圆锥体积最小时它的表面积.
- 假设2016年某国全社会商品零售价格总额为200 000亿元,货币流通次数为5次,每件M商品的价格为10元。2016年该
- For severalyears, we lived at the end of a long Texas countr
- 依次填入下面文字横线上的词语,最恰当的一项是 周国平说,我不认为读书可以成为时尚,并且对一切成为时尚的读书持
- 关于我国自然灾害的叙述,正确的是( ) ①我国发生地震灾害的频度不高,影响较小②江南丘陵降水丰沛,地下水水位高,土
- .下列加点词的意思和用法不同于其他三项的是( ) A.释之既朝毕,因前言便宜事 B.于是相如前进缶,因跪请秦王
- 如果一条直线与一个平面平行,那么,称此直线与平构成一个“平行线面线”.在一个平行六面体中,由两个顶点确定的直线与含有四个
- 阅读下面短文,回答16—19题。(12分) 学校请了一位名师给我们班上一节课。第二天早上8点整,名师准时出现在
- 高等生物细胞中的nuc—l基因编码的蛋白质能使DNA降解,进而导致细胞死亡。下列有关叙述正确的是 ( ) A.
- “获得感”名列《咬文嚼字》杂志社评选的2015年度十大热词榜首。“获得感&rdquo
- ---Did you go to the lecture delivered by Professor Li last
- 珠江三角洲地区盛产的经济作物是( ) A.天然橡胶 B.棉花 C.油棕 D.甘
- 30℃时Ca(OH)2在水中的溶解度为0.16g 。在此温度下,实验小组为制备饱和的澄清石灰水,称取5.6g生石灰,放
- 如图,已知一次函数的图象与反比例函数的图象在第一象限相交于点,与轴相交于点轴于点,的面积为1,则的长为 (
- Long bus rides are like television shows.They have a beginni
- 有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列各项的事实不能说明上述观点的是
- 如图所示,通有稳恒电流的长直螺线管竖直放置,铜环R沿螺线管的轴线加速下落.在下落过程中,环面始终保持水平.铜环先后经过轴
- 如果数据x1、x2、…、xn 的平均值为,方差为S2 ,则3x1+5、3x2+5、…、3xn+5 的平均值和方差分别为(
- It’s very coldoutside. Could you please _______the door? A.
- 如图,已知点A、B、C、D在一条直线上,EC∥FD,∠F=∠E, 求证:AE∥BF. 请在下列空格内填写结论和理



