化学平衡移动原理 知识点题库
光谱研究表明,易溶于水的SO2所形成的溶液中存在着下列平衡: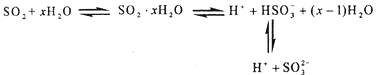
据此,下列判断中正确的是( )
K | Na | KCl | NaCl | |
熔点(℃) | 63.65 | 97.8 | 770 | 801 |
沸点(℃) | 774 | 882.9 | 1500(升华) | 1431 |
根据平衡移动原理,可推知,用Na与KCl反应制取K的适宜温度是( )
 2NH3(g)ΔH<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是( )
2NH3(g)ΔH<0。当改变某个条件并维持新条件直至新的平衡时,下表中关于新平衡与原平衡的比较正确的是( )
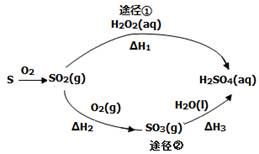
 CH3OCH3(g)+H2O(g) ΔH=-25 kJ/mol。某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
CH3OCH3(g)+H2O(g) ΔH=-25 kJ/mol。某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下: | 物质 | CH3OH | CH3OCH3 | H2O |
| c/(mol·L-1) | 0.8 | 1.24 | 1.24 |
下列说法正确的是( )
①平衡后升高温度,平衡常数>400
②平衡时,c(CH3OCH3)=1.6 mol/L
③平衡时,反应混合物的总能量减小20 kJ
④平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大
⑤此时刻反应达到平衡状态
⑥平衡时CH3OH的浓度为0.08 mol·L-1
-
(1) CO泄漏会导致人体中毒,用于检测CO的传感器的工作原理如图所示:写出电极I上发生的反应式:。

工作一段时间后溶液中H2SO4的浓度 (填“变大”、“变小”或“不变”)
-
(2) 用O2氧化HCl制取Cl2 , 可提高效益,减少污染。反应为:4HCl(g)+O2(g)
 2Cl2(g)+2H2O(g) ∆H , 通过控制条件,分两步循环进行,可使HCl转化率接近100%,其原理如图所示:
2Cl2(g)+2H2O(g) ∆H , 通过控制条件,分两步循环进行,可使HCl转化率接近100%,其原理如图所示: 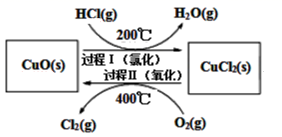
过程I的反应为:2HCl(g)+CuO(s)
 CuCl2(s)+H2O(g) ∆H1
CuCl2(s)+H2O(g) ∆H1过程II反应的热化学方程式(∆H2用含有∆H和∆H1的代数式表示)。
-
(3) 在温度T0℃,容积为1L的绝热容器中,充入0.2molNO2 , 发生反应:2NO2(g)
 N2O4(g) ∆H<0,容器中NO2的相关量随时间变化如图所示。
N2O4(g) ∆H<0,容器中NO2的相关量随时间变化如图所示。 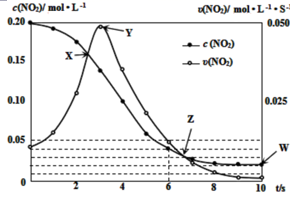
①反应到6s时,NO2的转化率是。
②根据图示,以下各点表示反应达到平衡状态的是。
a.X b.Y c.Z d.W
③0~3s内容器中NO2的反应速率增大,而3s后容器中NO2的反应速率减小了,原因是。
④此容器中反应达平衡时,温度若为T1℃,此温度下的平衡常数K═。
-
(4) 工业上可用Na2SO3溶液吸收法处理SO2 , 25℃时用1mol•L-1的Na2SO3溶液吸收SO2 , 当溶液pH═7时,溶液中各离子浓度的大小关系为:c(Na+)>c(HSO3-)>c(SO32-)>c(H+)═c(OH-)。(已知25℃时:H2SO3的电离常数Ka1═1.3×10-2 , Ka2═6.2×10-8)请结合所学理论通过计算说明c(HSO3-)>c(SO32-)的原因。
-
(1) 已知:N2(g)+O2(g)=2NO(g);ΔH1=+180.5 kJ·mol-1
C(s)+O2(g)=CO2(g);ΔH2=-393.5 kJ·mol-1
2C(s)+O2(g)=2CO(g);ΔH3=-221 kJ·mol-1
反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g)的ΔH= kJ·mol-1。
-
(2) 催化氧化法去除NO是在一定条件下,用NH3消除NO污染,其反应原理为4NH3+6NO
 5N2+6H2O。不同温度条件下,n(NH3)∶n(NO)的物质的量之比分别为4∶1、3∶1、1∶3时,得到NO脱除率曲线如图所示:
5N2+6H2O。不同温度条件下,n(NH3)∶n(NO)的物质的量之比分别为4∶1、3∶1、1∶3时,得到NO脱除率曲线如图所示: 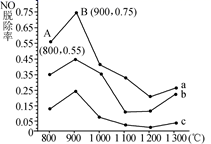
①n(NH3)∶n(NO)的物质的量之比为1∶3时,对应的是曲线(填“a”“b”或“c”)。
②由图可知,无论以何种比例反应,在温度超过900℃时NO脱除率都会骤然下降的原因可能是。
-
(3) NO氧化反应:2NO(g)+O2(g)⇌2NO2(g)分两步进行,其反应过程能量变化示意图如图:
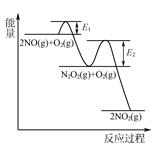
Ⅰ. 2NO(g)→N2O2(g);ΔH1
Ⅱ. N2O2(g)+O2(g)→2NO2(g);ΔH2
①化学反应速率有速率较慢的反应步骤决定。以上反应决定NO氧化反应速率的步骤是(填“Ⅰ”或“Ⅱ”)。
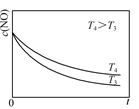
②在恒容的密闭容器中充入一定量的NO和O2气体,保持其他条件不变,控制反应温度分别为T3和T4(T4>T3),测得c(NO)随t(时间)的变化曲线如图。转化相同量的NO,在温度(填“T3”或“T4”)下消耗的时间较长,试结合反应过程能量图分析其原因:。
-
(4) NH3催化还原NO是重要的烟气脱硝技术,其反应过程与能量关系如图:
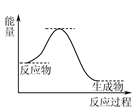
研究发现在以Fe2O3为主的催化剂上可能发生的反应过程如图,写出脱硝过程的总反应方程式:。
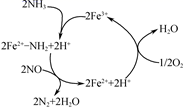
-
(1) Deacon发明的直接氧化法为:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)。下图为刚性容器中,进料浓度比c(HCl) ∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:
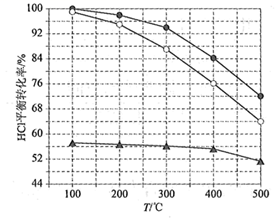
可知反应平衡常数K(300℃)K(400℃)(填“大于”或“小于”)。设HCl初始浓度为c0 , 根据进料浓度比c(HCl)∶c(O2)=1∶1的数据计算K(400℃)=(列出计算式)。按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O2)过低、过高的不利影响分别是。
-
(2) Deacon直接氧化法可按下列催化过程进行:
CuCl2(s)=CuCl(s)+
 Cl2(g) ΔH1=83 kJ·mol-1
Cl2(g) ΔH1=83 kJ·mol-1CuCl(s)+
 O2(g)=CuO(s)+
O2(g)=CuO(s)+  Cl2(g) ΔH2=-20 kJ·mol-1
Cl2(g) ΔH2=-20 kJ·mol-1CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=-121 kJ·mol-1
则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH= kJ·mol-1。
-
(3) 在一定温度的条件下,进一步提高HCl的转化率的方法是。(写出2种)
-
(4) 在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:
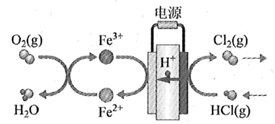
负极区发生的反应有(写反应方程式)。电路中转移1 mol电子,需消耗氧气L(标准状况)
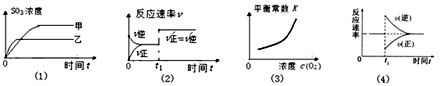
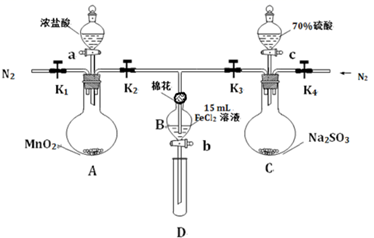
实验过程:
I.打开弹簧夹K1~K4 , 通入一段时间N2 , 再将T型导管插入B中,继续通入N2 , 然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
-
(1) 过程Ⅰ的目的是。
-
(2) 棉花中浸润的溶液为。
-
(3) A中发生反应的化学方程式为。
-
(4) 过程Ⅴ中,B溶液中发生反应的离子方程式是。
-
(5) 甲、乙、丙三位同学分别完成了上述实验,他们的检测结果一定能够证明氧化性:Cl2 > Fe3+ >SO2的是(填“甲”“乙”“丙”)。
过程Ⅳ B溶液中含有的离子
过程Ⅵ B溶液中含有的离子
甲
有Fe3+无Fe2+
有

乙
既有Fe3+又有Fe2+
有

丙
有Fe3+无Fe2+
有Fe2+
-
(6) 进行实验过程Ⅴ时,B中溶液颜色由黄色逐渐变为红棕色,停止通气,放置一段时间后溶液颜色变为浅绿色。查阅资料:Fe2+(aq) +
 (aq)
(aq)  FeSO3(s)(墨绿色)。
FeSO3(s)(墨绿色)。 提出假设:FeCl3与 SO2的反应经历了中间产物FeSO3 , 溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色。某同学设计如下实验,证实该假设成立:

①溶液E化学式为,溶液F化学式为。
②请用化学平衡原理解释步骤3中红棕色溶液颜色变为浅绿色的原因。
 2SO3(g),经过2min达到平衡状态,SO2的平衡转化率为90.0%。
2SO3(g),经过2min达到平衡状态,SO2的平衡转化率为90.0%。
-
(1) 0~2min内O2的平均反应速率v(O2)=。
-
(2) 该温度下此反应的化学平衡常数的值K=。
-
(3) 在相同温度下,某容器内c(SO2)=c(O2)=c(SO3)=1.0mol·L-1 , 则此时反应速率v正v逆(填“>”、“<”或“=”)。
-
(4) 在一定温度下,下列措施可以提高SO2转化率的是___ (填字母)。A . 增大SO2的浓度 B . 容积不变,充入氖气 C . 增大O2的浓度 D . 容积不变,再充入4.0molSO2与2.0molO2
-
(1) I.火法炼铅将铅精矿在空气中焙烧,生成PbO和SO2。
①用铅精矿火法炼铅的反应的化学方程式为。
②火法炼铅的废气中含低浓度SO2 , 可将废气通入过量氨水中进行处理,反应的离子方程式为。
-
(2) II.湿法炼铅在制备金属铅的同时,还可制得硫磺,相对于火法炼铅更为环保。湿法炼铅的工艺流程如图:
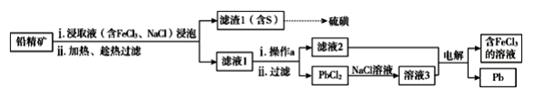
已知:①不同温度下PbCl2的溶解度如下表所示。
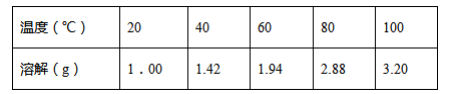
②PbCl2为能溶于水的弱电解质,在Cl-浓度较大的溶液中,存在平衡:PbCl2(aq)+2Cl-(aq)
 PbCl42-(aq)。
PbCl42-(aq)。铅精矿浸取后“趁热过滤”的原因是。
-
(3) 操作a为加适量水稀释并冷却,该操作有利于滤液1中PbCl2的析出。试分析“加适量水稀释”可能的原因是。
-
(4) 将溶液3和滤液2分别置于如图所示电解装置的两个极室中,可制取金属铅并使浸取液中的FeCl3再生。
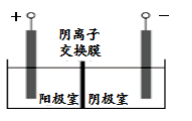
①溶液3应置于(填“阴极室”或“阳极室”)中。
②滤液2电解后可实现FeCl3的再生,该电极的电极反应式。
③若铅精矿的质量为ag,铅浸出率为b,当电解池中通过cmol电子时,金属铅全部析出,铅精矿中PbS的质量分数为(用a、b、c的代数式表示)。
-
(1) SO2的排放主要来自于煤的燃烧,工业上常用氨水吸收法处理尾气中的SO2。已知吸收过程中相关反应的热化学方程式如下:① SO2(g) + NH3•H2O(aq) =NH4HSO3(aq) △H1 = a kJ•mol-1;② NH3•H2O(aq) + NH4HSO3(aq) =(NH4)2SO3(aq) + H2O(l)△H2 = b kJ•mol-1;③ 2(NH4)2SO3(aq) + O2(g) =2(NH4)2SO4(aq) △H3= c kJ•mol-1 , 则反应 2SO2(g) + 4NH3•H2O(aq) + O2(g) =2(NH4)2SO4(aq) + 2H2O(l) △H = 。
-
(2) NOx的排放主要来自于汽车尾气,有人利用反应C (s) + 2NO(g)
 N2(g) + CO2(g) △H=-34.0 kJ•mol-1 , 用活性炭对NO进行吸附。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率 α(NO)随温度的变化如图所示:
N2(g) + CO2(g) △H=-34.0 kJ•mol-1 , 用活性炭对NO进行吸附。在恒压密闭容器中加入足量的活性炭和一定量的NO气体,测得NO的转化率 α(NO)随温度的变化如图所示: 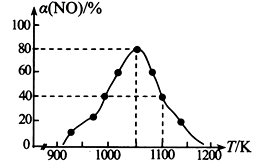
①由图可知,1050K前反应中NO的转化率随温度升高而增大,原因是; 在1100K 时,CO2的体积分数为。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1050K、1.1×106Pa 时,该反应的化学平衡常数Kp=(已知:气体分压=气体总压×体积分数)。
-
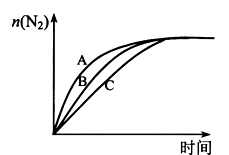
(3) 在高效催化剂的作用下用CH4还原NO2 , 也可消除氮氧化物的污染。在相同条件下,选用A,B,C三种不同催化剂进行反应,生成 N2的物质的量与时间变化关系如图所示,其中活化能最小的是(填字母标号)。
-
(4) 在汽车尾气的净化装置中 CO和NO发生反应:2NO(g) + 2CO(g)
 N2(g) + 2CO2(g) △H2 =-746.8 kJ•mol-1。实验测得,υ正=k正•c2(NO) •c2(CO) ,υ逆=k逆•c(N2) •c2(CO2) (k正、k逆为速率常数,只与温度有关)。
N2(g) + 2CO2(g) △H2 =-746.8 kJ•mol-1。实验测得,υ正=k正•c2(NO) •c2(CO) ,υ逆=k逆•c(N2) •c2(CO2) (k正、k逆为速率常数,只与温度有关)。 ①达到平衡后,仅升高温度,k正增大的倍数(填" >”、“< ”或“=”) k逆增大的倍数。
②若在1L 的密闭容器中充入1 mol CO和1 mol NO,在一定温度下达到平衡时,CO的转化率为40%,则
 =(保留2位有效数字)。
=(保留2位有效数字)。
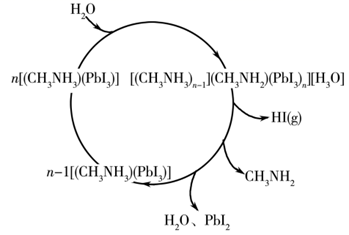
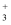 发生作用,生成H3O+和CH3NH2
C . 该反应的化学方程式为(CH3NH3)(PbI3)
发生作用,生成H3O+和CH3NH2
C . 该反应的化学方程式为(CH3NH3)(PbI3) 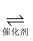 HI+CH3NH2+PbI2
D . 及时分离出HI有利于提高产率
HI+CH3NH2+PbI2
D . 及时分离出HI有利于提高产率
-
(1) 用CO2可以生产燃料甲醇。
已知:
 △H=-a kJ/mol
△H=-a kJ/mol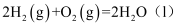 △H=-b kJ/mol
△H=-b kJ/mol 则表示
 燃烧的热化学方程式为。
燃烧的热化学方程式为。 -
(2) 某温度
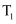 下,将6 mol CO2和8 molH2充入一容积为2 L的密闭容器中发生
下,将6 mol CO2和8 molH2充入一容积为2 L的密闭容器中发生 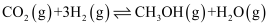 △H<0反应,测得H2的物质的量随时间变化如图中实线所示。
△H<0反应,测得H2的物质的量随时间变化如图中实线所示。 
请回答下列问题:
①前
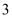 分钟内,H2的平均反应速率为
分钟内,H2的平均反应速率为 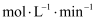 (保留两位小数)。
(保留两位小数)。②下列表述能表示该反应已达平衡的是(填序号)。
a.容器内压强不再改变 b.容器内气体的密度不再改变
c.容器内气体的平均摩尔质量不再改变 d.容器内各物质的物质的量相等
③在温度
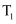 时,该反应的化学平衡常数为。
时,该反应的化学平衡常数为。④仅改变某一条件再进行实验,测得H2的物质的量随时间变化如图中虚线所示。与实线相比,改变条件的方式可能是。
-
(3) 二氧化硫一空气质子交换膜燃料电池将化学能转变成电能的同时,实现了制硫酸、发电、环保三位一体的结合,降低了成本提高了效益,其原理如图所示。
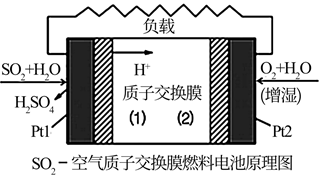
在该燃料电池中,负极的电极方程式为。
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②将混合气体中的氨液化有利于合成氨反应
③实验室常用排饱和食盐水的方法收集氯气
④红棕色NO2气体加压后颜色先变深后变浅
⑤加入催化剂有利于合成氨的反应
⑥由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深
⑦500 ℃时比室温更有利于合成氨的反应
 C(g)+ 2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是 ( )
C(g)+ 2D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是 ( )①增加A的量,平衡向逆反方向移动 ②升高温度,平衡向逆反应方向移动,v正减小 ③压强增大一倍,平衡不移动,v正、v逆不变 ④增大B的浓度v正>v逆 ⑤加入催化剂,B的转化率提高
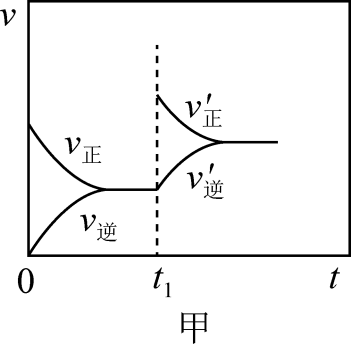
 2SO3(g) △H<0,t1时改变的条件是增大体系的压强
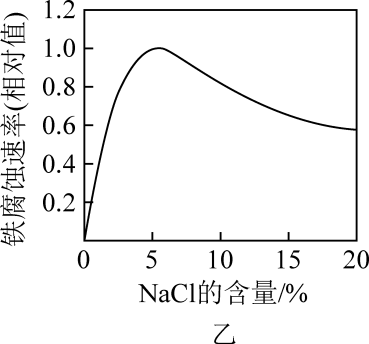
B . 图乙NaCl溶液浓度过高铁腐蚀速率降低,说明NaCl浓度越大溶液中O2的浓度越小
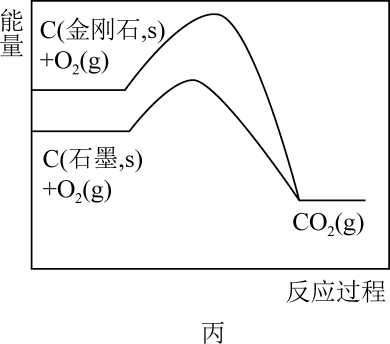
C . 图丙说明石墨转化为金刚石的反应的△H<0
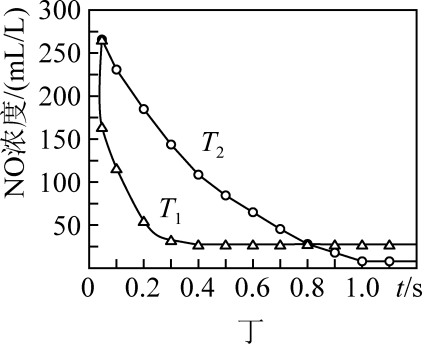
D . 图丁是一定条件下发生反应:4NH3(g)+4NO(g)+O2(g)
2SO3(g) △H<0,t1时改变的条件是增大体系的压强
B . 图乙NaCl溶液浓度过高铁腐蚀速率降低,说明NaCl浓度越大溶液中O2的浓度越小
C . 图丙说明石墨转化为金刚石的反应的△H<0
D . 图丁是一定条件下发生反应:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g)此过程△H<0
4N2(g)+6H2O(g)此过程△H<0
- 读漫画《投老张一票给十元!》,完成下列各题。这幅漫画主要告诉我们 A.我国目前的选举尚无法可依 B.我国要禁止一切竞选活
- 古诗文名句默写。(⑴—⑶题必做,第⑷⑸题任选一题作答即可)(6分) ⑴枯藤老树昏鸦, ▲ ,古道西风瘦马。
- (1)氢气是一种高效而无污染的理想能源,近20年来,对以氢气作为未来的动力燃料氢能源的研究获得了迅速发展。 ① 为了有效
- 设函数,其中,则导数的取值范围是 (A) (B) (C) (D)
- 家兔的一个初级卵母细胞中有22个四分体,则形成的卵细胞中染色体数为() A.11条 B.22条 C.33条
- 党的十八大报告提出全面建成小康社会的新要求,既与党的十六大、十七大提出的全面建设小康社会宏伟目标的要求相一致,又根据经济
- ---Lily,will you go to Jenny’s birthday party this Saturday?
- 某芳香烃A,分子式为C8H10;某烃类衍生物X,分子式为C15H14O3,能使FeCl3溶液显紫色;J分子内有两个互为对
- 小王参加一次比赛,比赛共设三关,第一、二关各有两个必答题,如果每关两个问题都答对,可进入下一关,第三关有三个问题,只要答
- 表面积为的正八面体的各个顶点都在同一个球面上,则此球的体积为 A. B. C.
- “君子之学必日进,日新者日进也。不日新者必日退,未有不进而不退者。”这说明( )A.人应该天天追求时尚、时髦B.人
- 某植株从环境中吸收前体物质经一系列代谢过程合成紫色素,此过程由A、a和B、b两对等位基因共同控制(如图所示)。其中具紫色
- 区别SO2和CO2气体可选用()A. 通入澄清石灰水中 B. 通入品红溶液中 C. 用带火星的木条检验 D. 通入石蕊试
- 下列各组词语中书写完全正确的一组是 A.斑澜 宁谧 贻然自得 咄咄逼人 B.搭讪 渊源 矫枉过
- 第二节 情景对话(共5小题;每小题1分,满分5分) 根据对话情景和内容,从对话后所给的选项中选出能填入空白处的最佳选项
- It displeases my parents when Richard and I stay out late at
- 从2015年9月起,北京市部分小学一年级《语文》教材中,古典诗词将由现在的6至8篇增加到22篇,整个小学阶段不少于100
- 某台湾旅行团要去拜访中华民族的人文始祖,他们应去的地方 A.黄帝陵 B.大禹陵
- She couldn’t rememberwhere it was _______ she first met me.
- 某校学生用化学知识解决生活中的问题,下列家庭小实验不合理的是 ( ) (A)用食醋除去暖



