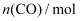化学平衡移动原理 知识点题库
 N2O4(g) △H<0。将烧瓶置于100℃的水中,则下列物理量中不会改变的是( )
N2O4(g) △H<0。将烧瓶置于100℃的水中,则下列物理量中不会改变的是( ) cC(g)+dD(g),压缩容积到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
cC(g)+dD(g),压缩容积到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是( )
 CO(g) +H2(g) △H=+131.3 kJ·mol-1
CO(g) +H2(g) △H=+131.3 kJ·mol-1
-
(1) 该反应的平衡常数K随温度的升高而(选填“增大”“ 减小”或“不变”)
-
(2) 上述反应达到平衡后,将体系中的C(s)部分移走,平衡(选填“向左移”“向右移”或“不移动”)。
-
(3) 下列事实能说明该反应在一定条件下已达到平衡状态的有___________(填序号)。A . 单位体积内每消耗1 mol CO的同时生成1molH2 B . 混合气体总物质的量保持不变 C . 生成H2O(g)的速率与消耗CO的速率相等 D . H2O(g)、CO、H2的浓度相等
-
(4) 某温度下,将4.0 mol H2O(g)和足量的炭充入2 L的密闭容器中,发生如下反应,C(s)+ H2O(g)
 CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为。
-
(5) 已知:① C(s)+H2O(l)
 CO(g)+H2(g) △H1
CO(g)+H2(g) △H1 ② 2CO(g)+O2(g)=2CO2 (g) △H2
③ H2O (l)=H2 (g)+1/2 O2 (g) △H3
则C(s)+O2 (g)=CO2 (g)的△H=。
-
(1) 脱硫总反应:SO2(g)+CO(NH2)2(aq)+2H2O(l)+1/2O2(g)=(NH2)SO4(aq)+CO2(g),已知该反应能自发进行,则条件是(填“高温”、“低温”或“任何温度”)。
-
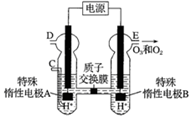
(2) 电解稀硫酸制备O3(原理如图),则产生O3的电极反应式为。
-
(3) 室温下,往恒容的反应器中加入固定物质的量的SO2和NO,通入O3充分混合。反应相同时间后,各组分的物质的量随n(O3)∶n(NO)的变化如图。
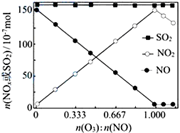
① n(NO2)随n(O3)∶n(NO)的变化先增加后减少,原因是。
② 臭氧量对反应SO2(g)+O3(g)=SO3(g)+O2(g)的影响不大,试用过渡态理论解释可能原因。
-
(4) 通过控制变量法研究脱除效率的影响因素得到数据如下图所示,下列说法正确的是____。
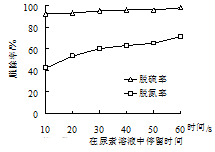
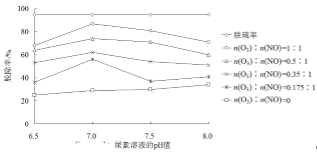 A . 烟气在尿素溶液中的反应:v(脱硫)<v(脱硝) B . 尿素溶液pH的变化对脱硝效率的影响大于对脱硫效率的影响 C . 强酸性条件下不利于尿素对氮氧化物的脱除 D . pH=7的尿素溶液脱硫效果最佳
A . 烟气在尿素溶液中的反应:v(脱硫)<v(脱硝) B . 尿素溶液pH的变化对脱硝效率的影响大于对脱硫效率的影响 C . 强酸性条件下不利于尿素对氮氧化物的脱除 D . pH=7的尿素溶液脱硫效果最佳 -
(5) 尿素的制备:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ΔH<0。一定条件下,往10 L恒容密闭容器中充入2 mol NH3和1 mol CO2。
CO(NH2)2(s)+H2O(g) ΔH<0。一定条件下,往10 L恒容密闭容器中充入2 mol NH3和1 mol CO2。 ① 该反应10 min 后达到平衡,测得容器中气体密度为4.8 g·L-1 , 平衡常数K=。
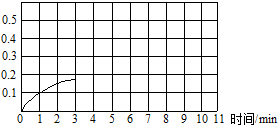
② 上图是该条件下,系统中尿素的物质的量随反应时间的变化趋势,当反应时间达到3min 时,迅速将体系升温,请在图中画出3~10 min 内容器中尿素的物质的量的变化趋势曲线。
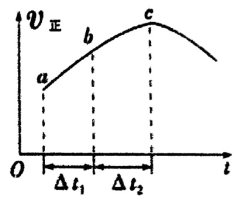
 CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示,由图可得出的结论正确的是( )
CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示,由图可得出的结论正确的是( )
 2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡及指定物质的浓度如何变化?
2CO(g) ΔH>0,达到平衡后,若改变下列条件,则平衡及指定物质的浓度如何变化?
-
(1) 增加C(s),平衡。
-
(2) 减小密闭容器容积,保持温度不变,则平衡。
-
(3) 通入N2,保持密闭容器容积和温度不变,则平衡。
-
(4) 保持密闭容器容积不变,升高温度,则平衡。
2NH3(g)+NO(g)+NO2(g) 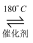 2N2(g)+3H2O
2N2(g)+3H2O 
在恒容的密闭容器中,下列有关说法正确的是( )
 CH3CH2OH(g)+3H2O(g) △H<0,在5MPa 下测得不同温度下平衡体系中各种物质的体积分数 ( V% ) 如图所示,下列说法中正确的是( )
CH3CH2OH(g)+3H2O(g) △H<0,在5MPa 下测得不同温度下平衡体系中各种物质的体积分数 ( V% ) 如图所示,下列说法中正确的是( ) 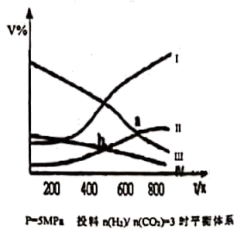
 依据图可判断正反应为放热反应
B .
依据图可判断正反应为放热反应
B .  虚线可表示使用了催化剂时的变化情况
C .
虚线可表示使用了催化剂时的变化情况
C .  若ΔH<0,图可表示升高温度使平衡向逆反应方向移动
D .
若ΔH<0,图可表示升高温度使平衡向逆反应方向移动
D . 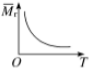 由图中混合气体的平均相对分子质量随温度的变化情况,可推知正反应吸热
由图中混合气体的平均相对分子质量随温度的变化情况,可推知正反应吸热
 CH4(g)+2H2O(g)△H<0。一定温度下,在一容积恒定的密闭容器中充入1mol CO2(g)和4molH2(g)发生上述反应,反应达到平衡后,若要同时增大正反应速率和H2平衡转化率,下列措施合理的是( )
CH4(g)+2H2O(g)△H<0。一定温度下,在一容积恒定的密闭容器中充入1mol CO2(g)和4molH2(g)发生上述反应,反应达到平衡后,若要同时增大正反应速率和H2平衡转化率,下列措施合理的是( )
热化学转化法:原理为CO2(g)+4H2(g)  CH4(g)+2H2O(g)△H
CH4(g)+2H2O(g)△H
-
(1) 每生成0.4mol CH4(g),放出66kJ的热量。则△H=;
-
(2) 其他条件不变,压强对CO2的转化率及CH4的选择性的影响如图所示。CH4的选择性=
 ×100%,CO2甲烷化反应选择0.1MPa (1个大气压)而不选择更高压强的原因是。
×100%,CO2甲烷化反应选择0.1MPa (1个大气压)而不选择更高压强的原因是。 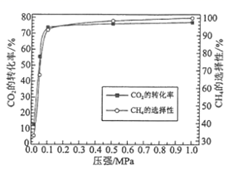
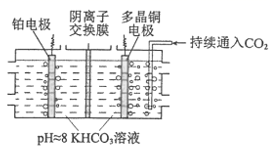
电化学转化法:在多晶Cu催化下,电解CO2制备CH4的原理如图所示。
-
(3) 铂电极上产生的气体为(填化学式);
-
(4) 电解结束时阴、阳极室的KHCO3溶液的浓度基本保持不变。在电解过程中,
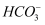 移向 (填“阴”或“阳” )极室。写出阴极的电极反应式;
移向 (填“阴”或“阳” )极室。写出阴极的电极反应式;
-
(5) 电解过程中应持续通入CO2 , 同时温度应控制在10℃左右,使CO2优先于H+在电极上发生反应。该电解过程不在室温下进行的原因是。
-
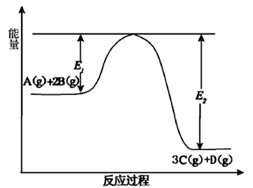
(1) 苯硫酚(C6H5SH)是一种重要的有机合成中间体,工业上常用氯苯(C6H5Cl)和硫化氢(H2S)来制备苯硫酚。已知下列两个反应的能量关系如图所示,则C6H5Cl与H2S反应生成C6H5SH的热化学方程式为。
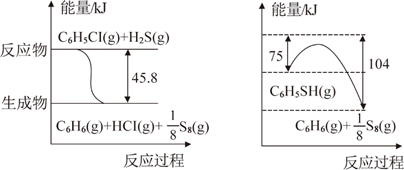
-
(2) H2S与CO2在高温下反应制得的羰基硫(COS)可用于合成除草剂。在610K时,将0.40molH2S与0.10molCO2充入2.5L的空钢瓶中,发生反应:H2S(g)+CO2(g)
 COS(g)+H2O(g);△H=+35kJ/mol,反应达平衡后水蒸气的物质的量分数为0.02。
COS(g)+H2O(g);△H=+35kJ/mol,反应达平衡后水蒸气的物质的量分数为0.02。 ①在610K时,反应经2min达到平衡,则0~2min的反应速率v(H2S)=。
②实验测得上述反应的速率方程为:v正=k正·c(H2S)·c(CO2),v逆=k逆·c(COS)·c(H2O),k正、k逆分别为正、逆反应速率常数,速率常数k随温度升高而增大。则达到平衡后,仅升高温度,k正增大的倍数 (填“>”“<”或“=”)k逆增大的倍数。
③该条件下,容器中反应达到化学平衡状态的依据是(填字母序号)。
A.容器内混合气体密度不再变化
B.v正(H2S)=v逆(COS)
C.容器内的压强不再变化
D.H2S与CO2的质量之比不变
-
(3) 工业上可以通过硫化氢分解制得H2和硫蒸气。在密闭容器中充入一定量H2S气体,反应原理:2H2S(g)
 2H2(g)+S2(g),H2S气体的平衡转化率与温度、压强的关系如图所示。
2H2(g)+S2(g),H2S气体的平衡转化率与温度、压强的关系如图所示。 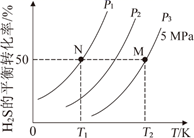
①图中压强(P1、P2、P3)的大小顺序为,理由是。
②如果要进一步提高H2S的平衡转化率,除改变温度、压强外,还可以采取的措施有。
③在温度T2、P3=5MPa条件下,该反应的平衡常数Kp=MPa(已知:用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
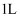 的恒容密闭容器中充入一定量的CO和
的恒容密闭容器中充入一定量的CO和  ,发生如下反应:
,发生如下反应: 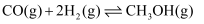 ,反应过程中测定的部分数据见表:
,反应过程中测定的部分数据见表: | 反应时间/min | | |
| 0 | 0.30 | 0.60 |
| 20 | 0.10 | |
| 30 | 0.20 |
下列说法正确的是( )
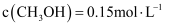 ,则反应的
,则反应的 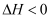 B . 反应在
B . 反应在 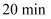 内的平均速率为
内的平均速率为 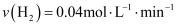 C . 保持其他条件不变,再向平衡体系中同时通入
C . 保持其他条件不变,再向平衡体系中同时通入  ,达到新平衡前v(正)<v(逆)
D . 相同温度下,若起始时向容器中充入
,达到新平衡前v(正)<v(逆)
D . 相同温度下,若起始时向容器中充入 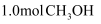 ,达到平衡时
,达到平衡时  转化率大于
转化率大于 
-
(1) 硝酸厂常用催化还原法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:I.CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH1=-890.3kJ·mol-1;
II.N2(g)+2O2(g)=2NO2(g)ΔH2=+67.7kJ·mol-1
则CH4(g)+2NO2(g)=CO2(g)+N2(g)+2H2O(l)ΔH=。
-
(2) 工业上利用NH3生产氢氰酸(HCN)的反应为CH4(g)+NH3(g)⇌HCN(g)+3H2(g) ΔH>0。
①该反应在(填“较高”或“较低”)温度下能自发进行。
②一定温度下,向2L恒容密闭容器中充入2molCH4(g)和2molNH3(g),发生上述反应,10min末达到平衡状态,测得NH3的体积分数为30%。则0~10min内,用HCN的浓度变化表示的平均反应速率为;CH4的平衡转化率为;该温度下,该反应的平衡常数K=(mol/L)2
-
(3) 在催化剂作用下,CO还原NO2进行汽车尾气处理:2NO2(g)+4CO(g)⇌4CO2(g)+N2(g)ΔH<0。
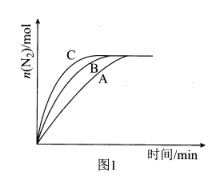
①相同条件下,选用A、B、C三种催化剂进行反应,生成N2的物质的量随时间的变化如图1所示。活化能最小的是[填“E(A)”“E(B)”或“E(C)”]。
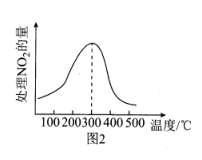
②在催化剂B作用下,测得相同时间内,处理NO2的量与温度的关系如图2所示。温度高于300℃,处理NO2的量随温度升高而减小的原因为(假设该温度范围内催化效率相同)。
-
(4) 煤燃烧产生的SO2可用足量NaOH溶液吸收生成Na2SO3 , Na2SO3溶液中各离子浓度由大到小的顺序为。
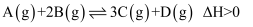 B . 其它条件不变,升高温度,A的转化率增大
C . 其它条件不变,加催化剂,反应速率增大,
B . 其它条件不变,升高温度,A的转化率增大
C . 其它条件不变,加催化剂,反应速率增大, 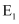 和
和  均减小,ΔH不变
D . 其它条件不变,增大压强,平衡向逆向移动,平衡常数K减小
均减小,ΔH不变
D . 其它条件不变,增大压强,平衡向逆向移动,平衡常数K减小
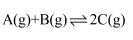
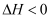 。
。 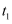 时刻达到平衡后,在
时刻达到平衡后,在  时刻改变某一条件,其反应过程如图所示。下列说法正确的是( )
时刻改变某一条件,其反应过程如图所示。下列说法正确的是( ) 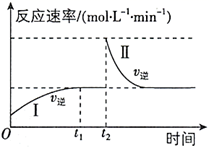
 时,
时, 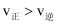 B . Ⅰ、Ⅱ两过程达到平衡时,
B . Ⅰ、Ⅱ两过程达到平衡时, 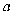 的体积分数:
的体积分数: 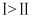 C .
C .  时刻改变的条件可以是向密闭容器中加入
时刻改变的条件可以是向密闭容器中加入 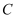 D . Ⅰ、Ⅱ两过程达到平衡时,平衡常数:
D . Ⅰ、Ⅱ两过程达到平衡时,平衡常数: 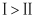
-
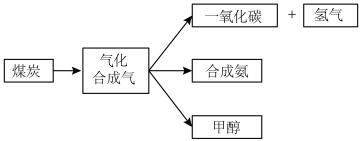
(1) 煤的气化发生的主要反应是:
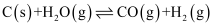 。
。已知:
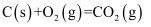
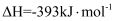

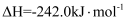

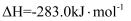
煤气化时发生主要反应的热化学方程式是。
-
(2) 用煤气化后得到的
 合成氨:
合成氨: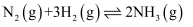
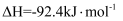 。在容积为2L的密闭容器中投入
。在容积为2L的密闭容器中投入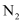 和
和 充分反应,在不同时间改变反应条件,正反应速率的变化如图所示。下列说法正确的是(填字母)。
充分反应,在不同时间改变反应条件,正反应速率的变化如图所示。下列说法正确的是(填字母)。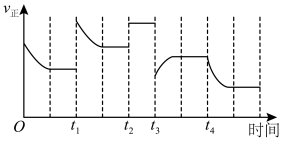
a.t1时可能增大了
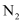 的浓度 b.t2时可能充入了氦气
的浓度 b.t2时可能充入了氦气c.t3时可能降低了温度 d.t4时可能分离出氨气
-
(3) 如图是合成氨反应平衡混合气中
 的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是(填“温度”或“压强”);判断L1L2 (填“>”或“<”),理由是。
的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是(填“温度”或“压强”);判断L1L2 (填“>”或“<”),理由是。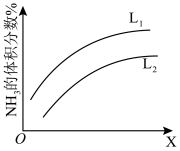
-
(4) 某温度时合成甲醇的反应
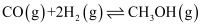
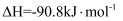 , 在容积固定的密闭容器中,各物质的浓度如下表所示:
, 在容积固定的密闭容器中,各物质的浓度如下表所示:浓度
时间
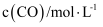
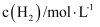
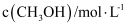
0
1.0
1.8
0
2min
0.5
0.5
4min
0.4
0.6
0.6
6min
0.4
0.6
0.6
①前2min的反应速率
 。
。②该温度下的平衡常数。(可用分数表示)
-
(1) 载人航天器中,可通过如下反应将航天员呼出的
 转化为
转化为 , 再通过电解
, 再通过电解 获得
获得 。
。已知:①
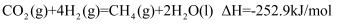
②
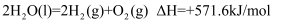
则
 和
和 反应生成
反应生成 和
和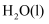 的热化学方程式为。
的热化学方程式为。 -
(2) 已知
 和
和 可以相互转化:
可以相互转化: 。现将一定量
。现将一定量 和
和 的混合气体通入体积为2L的恒温密闭容器中,物质浓度随时间的变化关系如图1所示。
的混合气体通入体积为2L的恒温密闭容器中,物质浓度随时间的变化关系如图1所示。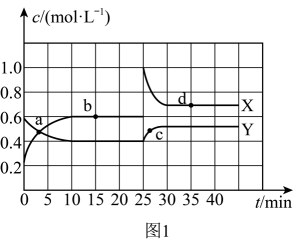
①图中曲线(填“X”或“Y”)表示
 随时间的变化。
随时间的变化。②a、b、c、d四个点中,表示化学反应处于平衡状态的是(填字母)。d点的平衡常数K=(计算结果精确到0.1)。
③
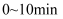 内,
内,
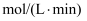 。
。 -
(3)
 催化氧化生成
催化氧化生成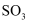 :
: , 混合体系中
, 混合体系中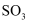 的百分含量与温度(T)的关系如图2所示(曲线上任何一点都表示平衡状态)。
的百分含量与温度(T)的关系如图2所示(曲线上任何一点都表示平衡状态)。 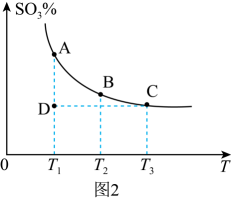
①若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡(填“向左”、“向右”或“不”)移动。
②若反应进行到状态D时,
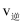 (填“>”、“<”或“=”,下同)
(填“>”、“<”或“=”,下同)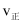 。
。③平衡常数K(A)K(C)。
- 每处错误仅涉及一个单词的增加,删除或修改。 增加: 在缺词处加一个漏字符号(∧), 并在其下面写出该加的词。删除: 把多
- ,绿杨阴里白沙堤。 (白居易《钱塘湖春行》)
- 图中为不同大陆上纬度相近的三个气象站测得的气温、降水量和日照时数资料。读图完成下列各题。12.①地年降水的季节分配主要受
- 被誉为“光纤之父”的华人科学家高锟荣获2009年诺贝尔化学奖。下列叙述错误的是( ) A.SiO2是
- 化学与生产、生活密切相关。下列叙述正确的是( ) A.煤的干馏和石油的分馏均属化学变化 B.明矾可用于水的消毒、杀
- 如图,已知抛物线y=﹣ax2+2ax+3a(a≠0)与x轴交于A、B两点,与y轴交于点C. (1)请直接写出A、B两点的
- About ________ of the workers in the factory were born in t
- “(楚庄王十六年)伐陈,杀夏征舒。……已破陈,即县之。”“(韩桓惠王十年)我上党郡守以上党郡降赵。”这说明春秋战国时期
- 把下列各组中的气体通入溶液中,溶液导电能力显著增强的是A.CO通入Ba(OH)溶液B.NH通入醋酸溶液中C.CO通入Na
- 对公众而言,只有理性参与公共事务,才能培养“无穷的远方、无数的人们,都与我有关”的公共精神,这本身就是最好的民主演练;对
- 近代欧洲资产阶级宣扬民主思想的根本目的是 A.反对封建专制统治 B.反对宗教神学的束
- 已知直线(a+2)x+(a2-2a-3)y-2a=0在x轴上的截距为3,求直线在y轴上的截距.
- 具有两对相对性状的亲本甲与乙杂交得到F1,F1自交得到F2,F2中各种表现型比例为9:3:3:1,其中甲与乙表现型相同的
- 孙中山领导的辛亥革命实现了20世纪中国第一次历史性巨变,因为这次革命()A、结束了帝国主义在中国的殖民统治 B、
- 马克思在《<黑格尔法哲学批判>导言》中写道:“路德战胜了信神的奴役制,只是因为他用信仰的奴役制代替了它。”“
- —Whydo you want to work for our company? —Thisis the job tha
- He can’t help __ housework, for he is busy __ for the examin
- 几种短周期元素的原子半径及主要化合价如下表: 元素代号 X Y Z W 原子半径/pm 160 143 70 66 主要
- To the great ______ of the youngwriter, his first book sell
- 以下学校某选修课学习小组对艺术楼附近湖泊进行的测定。 步骤1:取两个相同的透明玻璃瓶,分别编号为1号、2号。 步骤2:用