化学平衡中反应条件的控制 知识点题库
A | B | C | |
甲 | 1 | 3 | 0 |
乙 | 0 | 0 | 2 |
丙 | 1.5 | 4.5 | 1 |
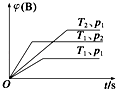
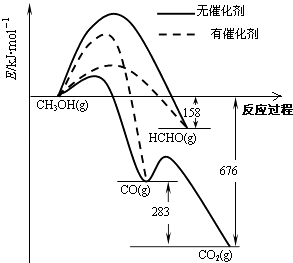
人们常用催化剂来选择反应进行的方向.如图所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].
-
(1) ①在有催化剂作用下,CH3OH与O2反应主要生成(填“CO、CO2”或“HCHO”).2HCHO(g)+O2(g)═2CO(g)+2H2O(g)△H=.
②甲醇制取甲醛可用Ag作催化剂,含有AgCl会影响Ag催化剂的活性.用氨水可以溶解除去其中的AgCl,写出该反应的离子方程式:.
-
(2) 已知:CO(g)+2H2(g)⇌CH3OH(g)△H=﹣a kJ•mol﹣1 .
①经测定不同温度下该反应的平衡常数如下:
温度(℃)
250
300
350
K
2.041
0.270
0.012
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)=0.4mol•L﹣1、c(H2)=0.4mol•L﹣1、c(CH3OH)=0.8mol•L﹣1 , 则此时v正v逆(填“>”、“<”或“=”).
②某温度下,在体积固定的2L的密闭容器中将1mol CO和2mol H2混合,测得不同时刻的反应前后压强关系如下:
时间(min)
5
10
15
20
25
30
压强比(P后/P前)
0.98
0.90
0.80
0.70
0.70
0.70
则0~15min,用H2表示的平均反应速率为,达到平衡时CO的转化率为.
-
(3) 利用钠碱循环法可除去SO2 , 消除SO2对环境的污染.吸收液吸收SO2的过程中,pH随n(SO32﹣):n(HSO3﹣)变化关系如下表:
n(SO32﹣):n(HSO3﹣)
91:9
1:1
1:91
pH
8.2
7.2
6.2
①根据上表判断NaHSO3溶液显性.
②在NaHSO3溶液中离子浓度关系正确的是 (填字母).
a.c(Na+)=2c(SO32﹣)+c(HSO3﹣)
b.c(Na+)>c(HSO3﹣)>c(H+)>c(SO32﹣)>c(OH﹣)
c.c(H2SO3)+c(H+)=c(SO32﹣)+(OH﹣)
d.c(Na+)+c(H+)=c(SO32﹣)+c(HSO3﹣)+c(OH﹣)
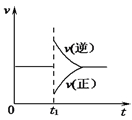
-
(1) x值等于;
-
(2) A的转化率为;
-
(3) 如果增大反应体系的压强,则平衡体系中C的质量分数(增大、减小、不变)
-
(4) 如果上述反应在相同条件下从逆反应开始进行,开始加入C和D各4 /3mol,要使平衡时各物质的质量分数与原平衡时完全相等,则还应加入B物质 mol。
 C(g),经过10s后,A的浓度为2mol.L-1,在此同时,B的浓度降低了0.06 mol.L-1..
C(g),经过10s后,A的浓度为2mol.L-1,在此同时,B的浓度降低了0.06 mol.L-1..
-
(1) A的起始浓度为多少?
-
(2) 10 s内用A的物质浓度变化表示的反应速率是多少?
 N2(g)+2H2O(g) ΔH,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n为常数),测得有关实验数据如下:
N2(g)+2H2O(g) ΔH,该反应的速率表达式为v=k·cm(NO)·cn(H2)(k、m、n为常数),测得有关实验数据如下: 容器编号 | 物质的起始浓度 (mol/L) | 速率 (mol·L-1·s-1) | 物质的平衡浓度 (mol/L) | |
c(NO) | c(H2) | c(N2) | ||
Ⅰ | 6×10-3 | 1×10-3 | a×10-3 | 2×10-4 |
Ⅱ | 6×10-3 | 2×10-3 | 2a×10-3 | |
Ⅲ | 1×10-3 | 6×10-3 | b×10-3 | |
Ⅳ | 2×10-3 | 6×10-3 | 4b×10-3 | |
下列说法正确的是( )
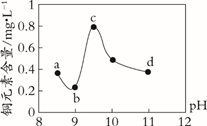
查阅资料,平衡I:Cu(OH)2 + 4NH3  [Cu(NH3)4]2+ + 2OH-;
[Cu(NH3)4]2+ + 2OH-;
平衡II:Cu(OH)2 + 2OH-  [Cu(OH)4]2-
[Cu(OH)4]2-
|
项目 |
废水水质 |
排放标准 |
|
pH |
1.0 |
6~9 |
|
Cu2+/ mg·L-1 |
72 |
≤0.5 |
|
NH4+/ mg·L-1 |
2632 |
≤15 |
下列说法错误的是( )
 2Fe2+(aq)+I2(aq),达到平衡,下列说法中错误的是( )
2Fe2+(aq)+I2(aq),达到平衡,下列说法中错误的是( )
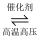 2NH3的微观历程如图所示。下列说法正确的是( )
2NH3的微观历程如图所示。下列说法正确的是( ) 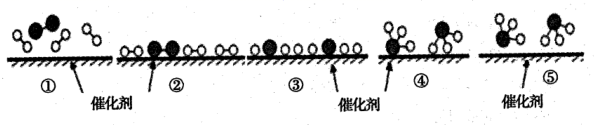
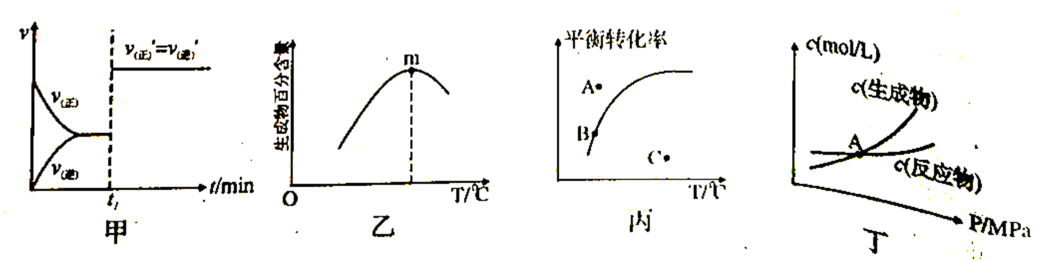
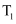 时刻可能改变了压强或使用了催化剂
B . 由乙图可知,反应在m点可能达到了平衡状态
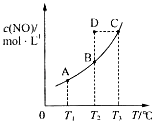
C . 由丙图可知,反应过程中
时刻可能改变了压强或使用了催化剂
B . 由乙图可知,反应在m点可能达到了平衡状态
C . 由丙图可知,反应过程中 的点是C点
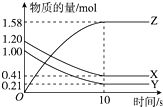
D . 由丁图可知,交点A表示反应一定处于平衡状态,此时
的点是C点
D . 由丁图可知,交点A表示反应一定处于平衡状态,此时
 可通过水煤气变换反应
可通过水煤气变换反应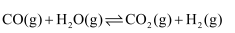 除去。某合成氨原料气中
除去。某合成氨原料气中 、
、 、
、 、
、 的体积分数分别为20%、50%、25%、5%。一定温度下按不同投料比
的体积分数分别为20%、50%、25%、5%。一定温度下按不同投料比 通入水蒸气,平衡后混合气体中
通入水蒸气,平衡后混合气体中 的体积分数如下表。
的体积分数如下表。投料比
温度/℃ |
|
|
|
200 | 1.70 | 0.21 | 0.02 |
250 | 2.73 | 0.30 | 0.06 |
300 | 6.00 | 0.84 | 0.43 |
350 | 7.85 | 1.52 | 0.80 |
下列说法不正确的是( )
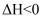 B . 温度相同时,投料比
B . 温度相同时,投料比 大,
大, 的转化率高
C . 按
的转化率高
C . 按 =1通入水蒸气后,反应前
=1通入水蒸气后,反应前 在混合气体中的体积分数为20%
D . 根据
在混合气体中的体积分数为20%
D . 根据 =1时数据推算,300℃时水煤气变换反应的平衡常数K为46
=1时数据推算,300℃时水煤气变换反应的平衡常数K为46
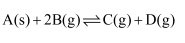 , 下列能作为化学平衡状态标志的是( )
, 下列能作为化学平衡状态标志的是( )①容器内气体的压强不变
②混合气体的密度不变
③混合气体的平均摩尔质量不变
④混合气体总物质的量不变
-
(1) 烟气中的NO可在催化剂作用下用NH3还原。氮的固定反应的相对能量变化如图所示:
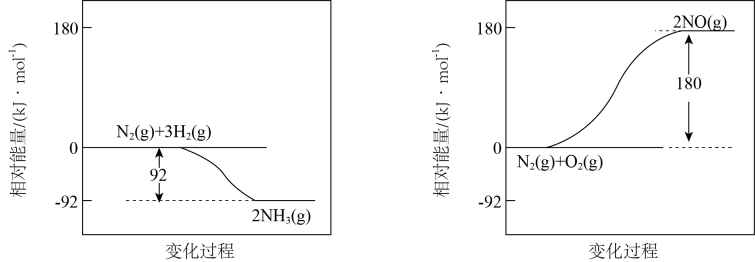
①图中两个反应的起始反应物的总能量大小(填“相等”“不相等”或“无法判断”)。已知
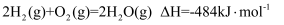 , 则
, 则
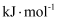 。
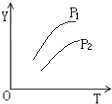
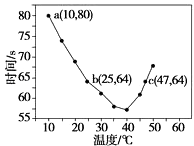
。②其他条件相同,分别在X、Y两种催化剂作用下在1L的密闭容器中通入
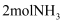 ,
, 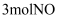 发生反应
发生反应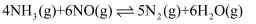 , 测得反应相同时间时NO的去除率与温度的关系如图所示。
, 测得反应相同时间时NO的去除率与温度的关系如图所示。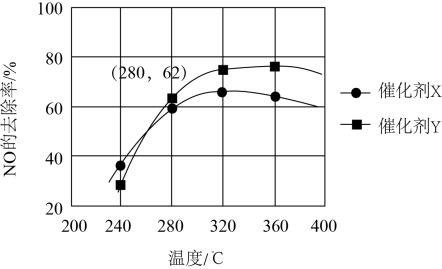
使用催化剂X,当温度高于320℃时,NO的去除率逐渐下降,其原因是。根据图像,(填“能”或“不能”)计算280℃时该反应的平衡常数,其理由是。
-
(2)
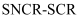 是一种新型的烟气脱硝技术,存在反应
是一种新型的烟气脱硝技术,存在反应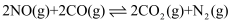 。将
。将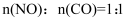 混合后置于一容积固定的密闭容器中,起始时气体压强为
混合后置于一容积固定的密闭容器中,起始时气体压强为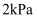 , 在500℃时上述反应达到平衡,气体压强为
, 在500℃时上述反应达到平衡,气体压强为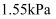 。
。①达到平衡时该反应的正反应速率(填“大于”或“等于”)0。
②此条件下反应的平衡常数

 (
( 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
- 田间喷洒农药,但农药大部分不能进入到植物细胞内,在此过程中起重要作用的是( ) A.细胞壁 B.细胞膜 C.细胞质
- 若函数的图象相邻两条对称轴之间的距离为,则为( ) A. B.1
- 实验室欲配制84g质量分数为10%的碳酸氢钠溶液用于实验,请计算: (1)需要碳酸氢钠的质量为g. (2)已知碳酸氢钠与
- 如图所示,电阻忽略不计的、两根两平行的光滑金属导轨竖直放置,其上端接一阻值为3Ω的定值电阻R。在水平虚线L1、L2间有一
- 如图,△ABC中,AC=BC=AB,ABED是边长为1的正方形,平面ABED⊥底面ABC,若G,F分别是EC,BD的中点
- 向含Fe3+、Fe2+、Mg2+、的水溶液中,加入足量的Na2O2固体,充分反应后再加入过量的稀盐酸,上述离子数目没有变
- 对下列培养基的叙述正确的是() A.制作固体培养基必须加入琼脂 B.加入青霉素可以得到放线菌 C.培养自生固氮菌不需额外
- 15.名句默写。(6分) 携来百侣曾游, 。 (2)
- 如下图,一束单色光射入一玻璃球体,入射角为60。已知光线在玻璃球内经一次反射后,再次折射回到空气中时与入射光线平行。此玻
- 下列图解能够正确表示神经细胞受到刺激时,膜电位与环境溶液中Na+浓度关系的是
- 20070412 是平面上的两个向量,且互为垂直. (1)求的值; (2)若的值.
- 10.儒家经典著作之一《尚书》中最早提到“民主“一词,认为:“天惟时求民主,乃大降显于成汤。”含义是说暴君夏桀残民以逞;
- .
- 假定2010年某国一单位M商品,其价值用该国货币表示为21元。如果2011年生产M商品的社会劳动生产率提高40%,且该国
- 本世纪,人类社会将逐渐步入氢经济时代。目前大规模产氢方式仍是化学制氢。 I、催化重整制氢 以甲醇为例,反应制氢气的一般途
- 仿照例句的句式,在下面两个横线上补写相应的内容。(4分) 例:假如我是一个画家,我就要用缤纷的色彩,来描绘世界的五彩斑斓
- 已知全集U={0,1,2,3,4},M={0,1,2},N={2,3},则(CuM)∩N=( )A. B
- 将饱和FeCl3溶液分别滴入下述液体中,能形成胶体的是 A.冷水 B.沸水
- 下列有关提高农产品商品率的措施的叙述中,错误的是() A.发展科技,提高产量 B.实现机械化,提高
- 求离心率为,且与椭圆9x2+4y2=36有共同焦点的椭圆方程.






