铁盐和亚铁盐的相互转变 知识点题库
-
(1) 实验室用锌粒与稀硫酸反应制取H2 , 要加快产生H2的速率,可采用的方法是(任写一种)。
-
(2) FeCl2溶液滴入KSCN溶液,出现红色,向变色的溶液中加入铁粉,溶液颜色变浅,直至褪色。原因是Fe3+被铁粉还原生成了Fe2+ , 写出该反应的离子方程式: 。
-
(3) 洁厕灵(主要成分是盐酸)与84消毒液(主要成分是次氯酸钠)是家庭生活中常备的两种清洁剂,但两种液体不能混合使用,两者混合会产生有毒气体Cl2 , 其发生的化学反应方程式为2HCl+NaClO=NaCl+Cl2↑+H2O。当有1mol的HCl参加反应时生成的氯气在标准状况下的体积为L。
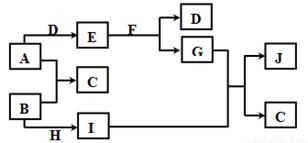
-
(1) 写出下列物质的化学式:H;D。
-
(2) 写出下列转化的化学方程式或离子方程式:
①E+F→D+G的化学方程式:;
②G+I→C+J的离子方程式:。
-
(3) 若要检验I物质的阳离子所加入的试剂是。实验现象为:
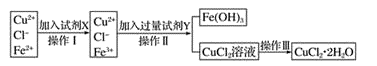
请参照下表给出的数据填空。

-
(1) 操作I加入X的目的是 。
-
(2) 下列物质都可以作为X,适合本实验的X物质可以是(填字母)。
A KMnO4 B NaClO C H2O2 D Cl2
-
(3) 操作II的Y试剂为(填化学式),并调节溶液的pH在范围。
-
(4) 实验室在配制CuCl2溶液时需加入少许(填物质名称),理由是(文字叙述并用有关离子方程式表示)。
-
(5) 若将CuCl2溶液蒸干灼烧,得到的固体是(填化学式);若要得无水CuCl2 , 请简述操作方法。
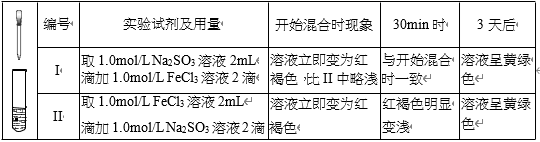
-
(1) 配制 FeCl3 溶液时,先将 FeCl3 溶于浓盐酸,再稀释至指定浓度。结合化学用语说 明浓盐酸的作用:。
-
(2) 甲同学认为,上述实验在开始混合时观察到的现象不涉及氧化还原反应,实验 I中红褐色比 II 中略浅的原因是。
-
(3) 乙同学认为实验 II 可能发生了氧化还原反应,为了探究反应的产物做了实验 III和生成物检验。
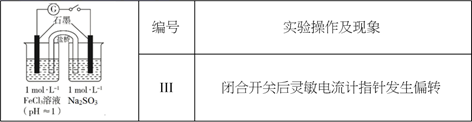
①取少量 Na2SO3 溶液电极附近的混合液,加入,产生白色沉淀,证明产生了 SO42-。
②该同学又设计实验探究另一电极的产物,取少量FeCl3溶液电极附近的混合液,加入铁氰化钾溶液,产生,证明产生了Fe2+。
-
(4) 实验 III 发生反应的方程式是。
-
(5) 实验小组查阅资料:溶液中 Fe3+、 SO32- 、OH-三种微粒会形成红色配合物并存在如下转化:

从反应速率和化学平衡两个角度解释实验 I、II 现象背后的原因可能是:。
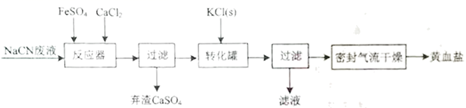
-
(1) 实验室用绿矾固体配制FeSO4溶液时,应先,再用蒸馏水稀释。
-
(2) “转化罐”中生成黄血盐晶体的反应类型为。
-
(3) 采用密封气流干燥取代在通风橱内干燥的原因是。
-
(4) 黄血盐的化学式可通过下列实验测定:
①准确称取4.220g样品加入水中充分溶解,将所得溶液转移至容量瓶配制成100.00mL溶液A。
②量取25.00mL溶液A,用2.000mol•L-1KMnO4溶液滴定,达到滴定终点时,共消耗KMnO4溶液15.25mL。反应如下(未配平):
 ③向②所得溶液加入Mn2+离子交换树脂,将Mn2+完全吸附后再滴加足量NaOH溶液,过滤、洗涤、灼烧,最终得固体0.2g。
③向②所得溶液加入Mn2+离子交换树脂,将Mn2+完全吸附后再滴加足量NaOH溶液,过滤、洗涤、灼烧,最终得固体0.2g。通过计算确定样品的化学式(写出计算过程)。
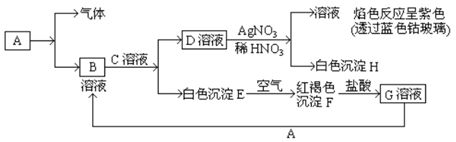
请回答下列问题:
-
(1) 写出B的化学式,D的化学式为;
-
(2) 写出由E转变成F的化学方程式。
-
(3) 写出D转化成H的离子方程式。
-
(4) 除去溶液B中混有的少量G溶液的最适宜方法是。
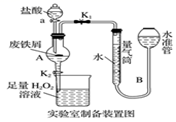
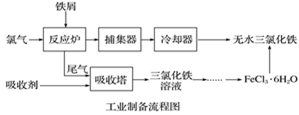
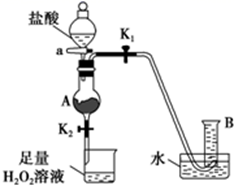
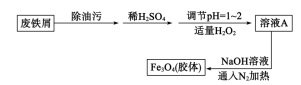
已知:①无水FeCl3的熔点为555K、沸点为588K。
②废铁屑中的杂质不与盐酸反应。
③不同温度下六水合氯化铁在水中的溶解度如下:
| 温度/℃ | 0 | 20 | 80 | 100 |
| 溶解度(g/100gH2O) | 74.4 | 91.8 | 525.8 | 535.7 |
实验室制备操作步骤如下:
I.打开弹簧夹K1 , 关闭活塞K2 , 并打开活塞a,缓慢滴加盐酸;
II.当装置A中不产生气泡时,关闭弹簧夹K1 , 打开活塞K2 , 当A中溶液完全进入烧杯后关闭活塞a;
III.将烧杯中溶液经过一系列操作后得到FeCl3·6H2O晶体。
请回答:
-
(1) 烧杯中足量的H2O2溶液的作用是。
-
(2) 从FeCl3溶液制得FeCl3·6H2O晶体的操作步骤是加入后、过滤、洗涤、干燥。
-
(3) 试写出吸收塔中反应的离子方程式:。
-
(4) 捕集器温度超过673K时,存在相对分子质量为325的铁的氯化物,该物质的分子式(相对原子质量:Cl-35.5、Fe-56)为。
-
(5) FeCl3的质量分数通常可用碘量法测定:称取mg无水氯化铁样品,溶于稀盐酸,配制成100mL溶液;取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入几滴淀粉溶液,并用cmol·L-1Na2S2O3溶液滴定,消耗VmL(已知:I2+2
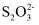 =2I-+
=2I-+ 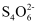 )。
)。 ①滴定终点的现象是;
②样品中氯化铁的质量分数为。
 转化为
转化为  下列物质中合适的是( )
下列物质中合适的是( )
 溶液
B .
溶液
B .  溶液
C . 氯水
D .
溶液
C . 氯水
D . 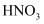 溶液
溶液
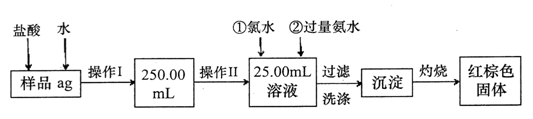
请根据流程,回答以下问题:
-
(1) 检验沉淀是否已经洗涤干净的操作是。
-
(2) 若坩埚质量是W1g,坩埚与加热后固体总质量是W2g,则样品中铁元素的质量分数;若称量准确,最终测得铁元素的质量分数偏大,则造成误差的原因可能是(写出一种原因即可)。
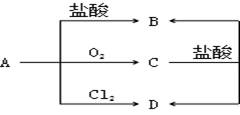
-
(1) 写出以下物质的化学式A、C、D。
-
(2) C+盐酸→B+D的离子方程式为,D的溶液可作为印刷电路板“腐蚀液”,写出该反应的化学方程式。
-
(3) 实验室保存B的溶液时常加入少量A,原因是(用离子方程式表示)
-
(4) 向B溶液中滴加NaOH溶液,产生的现象是,过程中所发生的氧化还原反应的化学方程式是。
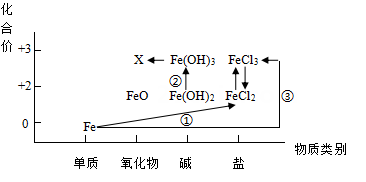
-
(1) X的化学式为,图中只具有还原性的物质是 (写化学式)。
-
(2) 实验室制备Fe(OH)2时,常伴随着反应②发生,此时的实验现象是。
-
(3) 写出反应③的化学方程式。
-
(4) 为探究Fe(NO3)2晶体的热分解产物。某化学兴趣小组按图进行了如图实验,回答下列问题:
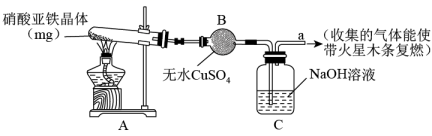
①实验时观察到A处试管中有红棕色气体生成,说明硝酸亚铁晶体分解产物含有,B中无水硫酸铜变蓝,说明分解产物中含有。
②检验热分解后的固体为氧化铁的方案为
实验步骤
现象
(i)取反应后少量红棕色固体于试管中,加入稀硫酸溶解
溶解后得色溶液
(i)向少许(i)溶液中滴入少量
溶液变成红色
由以上实验结果写出Fe(NO3)2·xH2O分解的化学方程式。
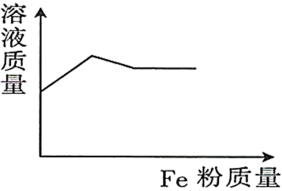
 和
和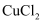 的混合溶液中逐渐加入
的混合溶液中逐渐加入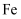 粉至过量,该溶液的质量随加入铁粉的质量的变化关系图为( )
粉至过量,该溶液的质量随加入铁粉的质量的变化关系图为( )
 B .
B . 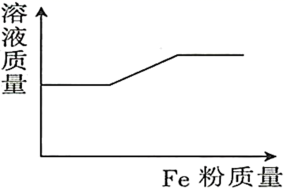 C .
C . 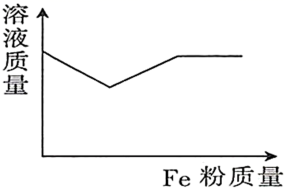 D .
D . 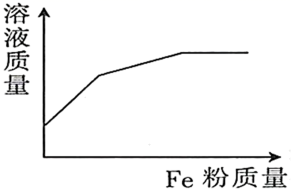
 的目的是将部分
的目的是将部分 氧化为
氧化为 C . 溶液A中
C . 溶液A中 和
和 的浓度最佳比为
的浓度最佳比为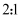 D . 提纯
D . 提纯 胶体的方法是过滤
胶体的方法是过滤
- —______ will you comeback, Mum? —In ten minutes. A. How long
- 在△ABC中,bsinA<a<b,则此三角形有( ) A.一解 B.两解 C.无解
- 下列哪个物体的质量最接近50g A.一枚大头针 B.一只鸡 C.一个鸡蛋 D.一
- Li Ming won the first prize in the English speech contest an
- 自“光荣革命”确立英国君主立宪政体后,英王室逐渐走下权力的最高殿堂。虽然王室奉行不干政原则,但又非常注意利用王室成员的影
- 如图所示,在正方体ABCD—A1B1C1D1中,E,F分别是BB1,CD的中点.(1)求证:AD⊥D1F;(2)求AE与
- 已知如图:二次函数y=ax2+bx+c的图象与x轴交于A、B两点,与y轴交于点C,若AC=20,BC=15,∠ACB=9
- 氟、氯、溴、碘四种元素,它们的下列性质的递变规律不正确的是( ) A.单质密度依次增大
- 下列关于真核细胞的结构和功能的叙述,正确的是() A. 细胞膜可提高细胞内化学反应的速率 B. 细胞核中可完成基因的复制
- 实验室配制氯化钠溶液的操作中,正确的是() A. 取氯化钠 B. 称氯化钠 C. 量取水 D. 溶解
- 用玻璃制造的封闭的电话亭隔音效果好,这主要是因为玻璃:A.能较好地吸收声音; B.能较
- 直升机悬停在空中向地面投放装有救灾物资的箱子,如图所示。设投放初速度为零.箱子所受的空气阻力与箱子下落速度的平方成正比,
- children there are in a family, their life will
- 下列句子中,没有语病的一句是 A.据我的愚见,斜线号是近些年才发展起来,逐渐被采用,但还没有被国家语言文字工作委员会认定
- 图为“探究求合力的方法”的实验装置.1.下列说法中正确的是 A.在测量同一组数据F1、F2和合力F的过程中,
- 如图所示,在□ABCD中,对角线AC与BD相交于点O,过点O任作一条直线分别交AB,CD于点E,F.(1)求证:OE=
- 从2007年下半年开始,山东省县乡两级人大换届选举陆续进行,这是社会主义民主一次最广泛、最深刻的实践。在县、乡和不设区的
- 下列各句中,没有语病的一句是 A.要造就一批大师,政治家能做的最有价值的贡献,是创造海纳百川的人文环境,确立鼓励追求真
- 如图4-3-4所示,在水平桌面上放一个重为GA=20 N的木块,木块与桌面间的动摩擦因数μA=0.4,使这个木块沿桌面做
- (2010北京文数)⑴ 集合,则= (A) {1,2} (B) {0,1,2} (C){1,2,3}



