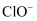硫酸根离子的检验 知识点
硫酸根离子的检验 知识点题库
实验室检验某溶液中是否含有Cl﹣的操作方法是:.
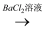 白色沉淀
白色沉淀 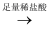 沉淀不溶解
B . 方案乙:试液
沉淀不溶解
B . 方案乙:试液 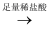 无沉淀(也无气泡)
无沉淀(也无气泡)  白色沉淀
C . 方案丙:试液
白色沉淀
C . 方案丙:试液  无沉淀
无沉淀  白色沉淀
D . 方案丁:试液
白色沉淀
D . 方案丁:试液  白色沉淀(过滤)
白色沉淀(过滤)  沉淀不溶解
沉淀不溶解
-
(1) 写由A与D的化学式:AD。
-
(2) A与E溶液反应的离子方程式。
-
(3) 已知:H+(aq)+OH-(aq)=H2O(l)△H=-akJ/mol,请写出相同条件下B与C的稀溶液反应的中和热的热化学方程式。
-
(4) 检验E溶液中阴离子的方法为。
-
(5) 请写出向E溶液中加过量B溶液的化学方程式。
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向盛有稀 | 试管口出现红棕色气体 | 溶液中的 |
| B | 向某钠盐X溶液中加入盐酸,将产生的气体通入 | 有白色沉淀产生 | 反应生成的气体可能为 |
| C | 向滴加酚酞的氨水中加蒸馏水稀释 | 溶液红色变浅 | 溶液中所有离子的浓度均减小 |
| D | 用铂丝蘸取某溶液在酒精灯火焰上灼烧 | 直接观察,火焰呈黄色 | 溶液中的金属阳离子只有 |
| 实验操作及现象 | 实验结论 | |
| A | 将一块表面打磨过的铝箔在酒精灯上加热至熔化,液态铝不会滴落 | Al2O3的熔点高于Al |
| B | 向无色溶液中滴入BaCl2溶液,出现白色沉淀 | 该溶液一定含SO |
| C | 某气体能使湿润的淀粉KI试纸变蓝 | 该气体一定是Cl2 |
| D | 蘸有浓氨水的玻璃棒放在某溶液上方,产生白烟 | 该溶液一定为浓盐酸 |
 , 并探究
, 并探究 与
与 溶液的反应。
溶液的反应。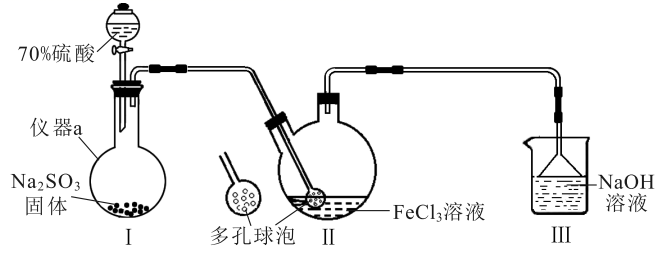
回答下列问题:
-
(1) 仪器
 的名称是,装置Ⅰ中反应的化学方程式为。
的名称是,装置Ⅰ中反应的化学方程式为。
-
(2) 多孔球泡的作用有、。
-
(3) 实验开始后,装置Ⅱ中溶液很快由黄色变为红棕色;停止通入
 , 放置一段时间后,Ⅱ中溶液又逐渐变为浅绿色。有同学认为此时该溶液中含有
, 放置一段时间后,Ⅱ中溶液又逐渐变为浅绿色。有同学认为此时该溶液中含有 , 并进行以下实验验证:
, 并进行以下实验验证:操作
现象
结论
取少量装置Ⅱ中溶液于试管中,先滴加溶液,再滴加适量
 溶液,振荡
溶液,振荡先无明显现象,加入
 溶液后,现象是
溶液后,现象是溶液中含有

-
(4) 为探究装置Ⅱ中溶液颜色变化的原因,查阅资料后提出假设:该装置中可能存在以下两种化学反应。将反应ii补充完整。
i.
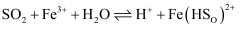 (红棕色);
(红棕色);ii.
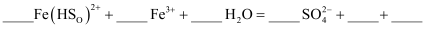
-
(5) 为检验反应ii中生成的
 , 可选用的化学试剂是。
, 可选用的化学试剂是。
-
(1) 取少量黄色溶液,(填操作和现象),证明黄色溶液中含有Fe3+。
-
(2) 取黄色溶液,加入铁粉振荡,溶液由黄色变为浅绿色,反应的离子方程式为。
-
(3) 探究溶液变黄的原因。
①实验证实,溶液变黄是因为空气中的O2将Fe2+氧化,反应的离子方程式为。
②用FeSO4和稀硫酸配制不同溶液,进一步探究影响溶液变黄的其他因素,实验如下。
实验编号
Ⅰ
Ⅱ
Ⅲ
Ⅳ
c(FeSO4)/(mol·L−1)
0.5
0.25
0.5
0.25
溶液pH
3.3
3.5
2.9
2.9
初始颜色
浅绿色
浅绿色,比Ⅰ浅
浅绿色,同Ⅰ
浅绿色,同Ⅱ
0.5h颜色
浅绿色
黄绿色
浅绿色
浅绿色
5h颜色
黄色
黄色
浅黄色
浅黄色(比Ⅲ浅)
a.实验Ⅲ和Ⅳ说明对溶液变黄快慢有影响。
b.实验Ⅱ比Ⅰ更快变黄的原因是。
-
(4) 检验黄褐色沉淀的成分。
①通过下列实验证实,黄褐色沉淀中含有SO42-。
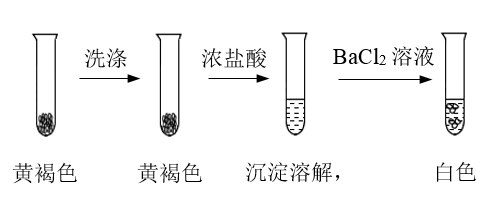
a.证实黄褐色沉淀中含有SO42-的证据是。
b.洗涤黄褐色沉淀的目的是。
②进一步实验证实黄褐色沉淀为Fe(OH)SO4.将反应的离子方程式补充完整:Fe3+++=Fe(OH)SO4↓+。
-
(5) 根据以上实验,配制FeSO4溶液时,为使溶液较长时间保持浅绿色,还需加入铁粉和稀硫酸,其中稀硫酸的作用是(答出两点)。
现象 | 解释(或结论) | |
A | 浓硝酸在光照下颜色变黄 | 浓硝酸不稳定 |
B | 浓硫酸能使小木条变黑 | 浓硫酸具有吸水性 |
C | 向某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 该溶液中含有SO |
D | Cl2和SO2均可使含有酚酞的NaOH溶液褪色 | Cl2和SO2均具有漂白性 |
 C . 滴加KSCN溶液变血红色,一定含有Fe3+
D . 滴加硝酸酸化的AgNO3溶液有白色沉淀生成,一定含有Cl-
C . 滴加KSCN溶液变血红色,一定含有Fe3+
D . 滴加硝酸酸化的AgNO3溶液有白色沉淀生成,一定含有Cl-
选项 | 实验操作及现象 | 解释或结论 |
A | 将氯水滴入KI-淀粉溶液中,溶液变成蓝色 | Cl2的氧化性强于I2 |
B | 将蘸有浓盐酸的玻璃棒与蘸有浓氨水的玻璃棒靠近,产生大量白烟 | NH3遇到HCl时反应生成NH4Cl晶体 |
C | 向某溶液中加入稀硝酸无明显现象,再加入BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有SO |
D | 向某溶液中逐滴加入NaOH溶液,立即产生白色沉淀,迅速变成灰绿,最终变成红褐色 | 此溶液中一定含有Fe2+ |
 B . 向溶液中加入稀硝酸后,再加入
B . 向溶液中加入稀硝酸后,再加入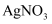 溶液有白色沉淀生成,则溶液中一定含有
溶液有白色沉淀生成,则溶液中一定含有 C . 加入
C . 加入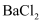 溶液有白色沉淀产生,再加盐酸,沉淀不溶解,原溶液中一定含有
溶液有白色沉淀产生,再加盐酸,沉淀不溶解,原溶液中一定含有 D . 向溶液中加入
D . 向溶液中加入 溶液,加热后产生使湿润的红色石蕊试纸变蓝的气体,则可推该溶液中一定含有
溶液,加热后产生使湿润的红色石蕊试纸变蓝的气体,则可推该溶液中一定含有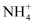

 溶液,用湿润的红色石蕊试纸放试管口未变蓝,则原溶液中无
溶液,用湿润的红色石蕊试纸放试管口未变蓝,则原溶液中无 B . 向无色溶液中加入
B . 向无色溶液中加入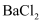 溶液有白色沉淀出现,则溶液中一定含有
溶液有白色沉淀出现,则溶液中一定含有 C . 用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中一定是钠盐
D . 向某溶液中加入稀盐酸产生使澄清石灰水变浑浊的气体,则溶液中可能含有
C . 用洁净的铂丝蘸取溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中一定是钠盐
D . 向某溶液中加入稀盐酸产生使澄清石灰水变浑浊的气体,则溶液中可能含有
选项 | 实验内容 | 结论 |
A | 向某溶液中滴加硝酸和硝酸银溶液,产生白色沉淀 | 该溶液中一定含 |
B | 向某溶液中滴加盐酸酸化 | 该溶液一定含: |
C | 向品红溶液中加入某固体粉末,溶液褪色 | 该固体中一定含有 |
D | 向某溶液中滴加澄清石灰水,产生白色沉淀 | 该溶液中一定含 |
- 下列物质中,只含有共价键的是 A.Na2O B.NaCl C.HCl
- 结核杆菌感染人体并侵入细胞后会引起结核病,体内接触该靶细胞并导致其裂解的免疫细胞是() A.浆细胞
- 分解因式2-2x+=______________
- It’s said that there are plenty of hotels in Shanghai. There
- 阅读下面这首宋词,回答问题。(8分) 木兰花令·次欧公西湖韵① 苏轼 霜余已失长淮阔,空听潺潺清颍②咽。 佳人犹
- 已知数列{an}的前n项和为Sn,对任意n∈N*都有Sn=an-,若1<Sk<9(k∈N*),则k的值为________
- 阅读下面的材料,根据要求作文。 (60分) 有人发现这样一个现象:在飞机上,同样是30岁到40岁年纪的旅客,头等舱的旅客
- 1. 下列说法中正确的是 A.一段电路中的电流增大了,一定是因为电路中的电阻减小了
- 将地球上一只标准的摆钟搬到月球,则该摆钟是走快了还是走慢了?在12 h内摆钟和标准的摆钟相差多少时间?(g月=g地/6)
- ......
- 双曲线的两个焦点为F1、F2,以F1F2为边作等边三角形,若双曲线恰好平分三角形的另两边,则双曲线的离心率为( )
- 一物体自t=0时开始做直线运动,其速度图线如图所示.下列选项正确的是()A.在0~6s内,物体离出发点最远为30m B.
- 下列化学方程式书写正确且属于分解反应的是 A.C6H12O6 +
- Silence is unnatural to man.He begins life with a cry and en
- 2009年第十一届全运会于10月11日在山东济南召开,全运会以《共同精彩》拉开大幕。《共同精彩》以民族乐与流行乐、地方乐
- 在将动物组织块分散成单个细胞时,可以使用胰蛋白酶。下列叙述错误的是( )A.动物细胞之间可能依靠蛋白质相互联系 B
- 新疆绿洲农业特色产品有棉花、甜菜和哈密瓜等。
- What does she looklike? She is tall and thin _________ long
- ______2013 Guangzhou Reading Month was started on Mar. 30th
- 在复杂的体系中,确认化学反应先后顺序有利于解决问题。下列化学反应先后顺序判断正确的是( ) A. 在含有等物质的量
 溶液的试管中加入
溶液的试管中加入 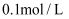 的
的  溶液
溶液 被
被  还原为
还原为 
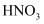 酸化的
酸化的  溶液中
溶液中