硫酸根离子的检验 知识点题库
把SO2通入Fe(NO3)3溶液中,溶液由黄色变为浅绿色,但立即又变为黄色,此时若滴入BaCl2溶液,则会产生白色沉淀。在上述一系列变化过程中,最终被还原的是( )
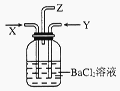
(2)加入HCl酸化的BaCl2溶液→白色沉淀→判断一定有SO42﹣ , 是否正确 理由
(3)加入Ba(NO3)2溶液→白色沉淀→再加HCl→沉淀不溶解→判断一定有SO42﹣ , 是否正确 理由 .
若以上操作都不正确,则正确的操作是:先加入 →现象 →再加入 →现象 →判断一定有SO42﹣ .
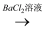 白色沉淀
白色沉淀 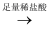 沉淀不溶解
B . 方案乙:试液
沉淀不溶解
B . 方案乙:试液 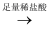 无沉淀(也无气泡)
无沉淀(也无气泡) 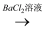 白色沉淀
C . 方案丙:试液
白色沉淀
C . 方案丙:试液 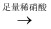 无沉淀
无沉淀  白色沉淀
D . 方案丁:试液
白色沉淀
D . 方案丁:试液  白色沉淀(过滤)
白色沉淀(过滤)  沉淀不溶解
沉淀不溶解
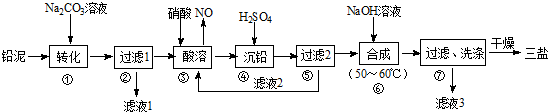
请回答下列问题:
-
(1) 铅蓄电池在生活中有广泛应用,其工作原理是Pb+PbO2+2H2SO4
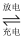 2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为。
2PbSO4+2H2O。若铅蓄电池放电前正、负极质量相等,放电时转移了1 mol电子,则理论上两极质量之差为。
-
(2) 将滤液1、滤液3合并,经蒸发浓缩、降温结晶、过滤等操作,可得到一种结晶水合物(Mr=322),其化学式为。
-
(3) 步骤③酸溶时铅与硝酸反应生成Pb(NO3)2及NO。滤液2中溶质的主要成分为(填化学式)。
-
(4) 步骤⑥合成三盐的化学方程式为。
-
(5) 步骤⑦的洗涤操作中,检验沉淀是否洗涤完全的操作方法是。
| | | | |
| A.在某溶液中加入盐酸后无现象,再加BaCl2产生白色沉淀证明有SO42- | B.样品中加NaOH溶液加热,蓝色石蕊试纸变红,证明检验样品中有NH4+的存在 | C.将混有少量氯化钾的硝酸钾饱和溶液在冰水中冷却,KNO3晶体先析出 | D.将灼热的铜丝伸入盛有氯气的集气瓶中,铜丝剧烈燃烧,产生棕黄色的烟 |
| 选项 | 实验操作及现象 | 推理或结论 |
| A | 向KI淀粉溶液中滴入氯水,溶液变成蓝色 | I-的还原性强于Cl- |
| B | 向某溶液中加入BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
| C | 取少量Na2O2粉末放在脱脂棉上,再将1滴水滴到Na2O2上,脱脂棉燃烧 | Na2O2与水反应放热 |
| D | 向某溶液中加入NaOH溶液,生成的白色絮状沉淀迅速变成灰绿色,最后变成红褐色 | 该溶液中一定含有Fe2+ |
-
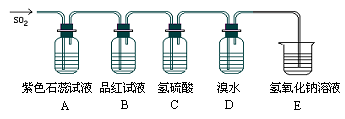
(1) 写出实验室制SO2的化学方程式:。
-
(2) 二氧化硫具有:①漂白性 ②酸性氧化物的性质 ③还原性 ④氧化性,在上图几个装置中对应表现出的性质是(填序号):
A中B中C中D中
-
(3) 有四位同学设计下列四个方案检验E溶液中是否含有SO42- , 你认为合理的是(_____)A . 试液
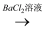 白色沉淀
白色沉淀 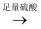 沉淀不溶解
B . 试液
沉淀不溶解
B . 试液 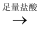 无沉淀
无沉淀  白色沉淀
C . 试液
白色沉淀
C . 试液  无沉淀
无沉淀  白色沉淀
D . 试液
白色沉淀
D . 试液  无沉淀
无沉淀  白色沉淀
白色沉淀
-
(4) 实验完毕后,将B中溶液取少量于试管中加热,现象是,原因是。
| 选项 | 实验操作 | 实验目的 |
| A | 将炽热的木炭与浓硝酸混合所得气体通入澄清石灰水中 | 验证碳的氧化产物为CO2 |
| B | 向饱和碳酸钠溶液中通入二氧化碳 | 探究Na2CO3和NaHCO3溶解度相对大小 |
| C | 向某溶液中滴加BaCl2溶液和稀硝酸 | 检验原溶液中是否含SO |
| D | 向淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜悬浊液并加热 | 验证淀粉已水解 |
| 目的 | 操作 | |
| A | Cu与浓硫酸反应后未见溶液变蓝色,为了观察生成了CuSO4 | 向反应后的溶液中加入适量蒸馏水 |
| B | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
| C | 检验某溶液中是否有SO42﹣ | 取少量溶液于试管中,向该溶液中加入已用盐酸酸化的BaCl2溶液 |
| D | 制备Fe(OH)3胶体 | 将NaOH溶液滴加到饱和FeCl3溶液中 |
|
选项 |
实验操作和现象 |
结论 |
|
A |
向纤维素中加入适量硫酸溶液,微热一段时间后,滴加新制的氢氧化铜悬浊液,加热煮沸,未发现砖红色沉淀生成 |
纤维素没有水解或者已经水解但水解后的产物中没有葡萄糖 |
|
B |
1-溴丙烷与NaOH的乙醇溶液共热,有气体生成,该气体可使酸性高锰酸钾溶液褪色 |
该气体是丙烯 |
|
C |
粗盐提纯时,将2mol·L-1NaOH、饱和BaCl2和0.5mol·L-1Na2CO3溶液依次加入后,一次过滤,滤液用HCl调至pH<3,取少许该溶液滴加饱和BaCl2溶液,发现有明显的白色沉淀生成 |
说明“一次过滤”后没有完全除尽 |
|
D |
向苯酚钠溶液中通入CO2 , 溶液变浑浊 |
碳酸溶液的pH比苯酚小 |
 C . 向浸取液中加入KSCN溶液,无明显现象,滴入新制氯水后,溶液变为红色,说明雾霾中Fe2+
D . 向浸取液中加入浓NaOH溶液微热,试管口附近湿润的红色石蕊试纸变蓝,说明雾霾中一定含有
C . 向浸取液中加入KSCN溶液,无明显现象,滴入新制氯水后,溶液变为红色,说明雾霾中Fe2+
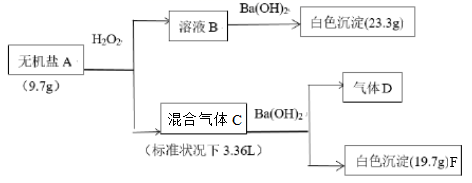
D . 向浸取液中加入浓NaOH溶液微热,试管口附近湿润的红色石蕊试纸变蓝,说明雾霾中一定含有 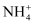
已知:D为单质,在标准状况下的密度为1.25 g/L;溶液B显酸性。
-
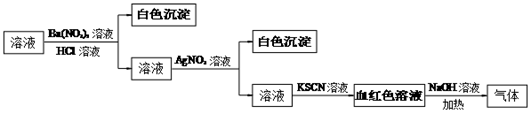
(1) 混合气体C含两种气体,其中气体D的结构式为,另一种气体的电子式为。
-
(2) 白色沉淀F可溶于盐酸,反应的离子方程式为。
-
(3) 加入足量H2O2反应后,检验溶液B中主要阴离子的实验操作是。
-
(4) 写出无机盐A所含的金属元素在周期表中的位置。
-
(5) 写出A与H2O2反应的离子方程式。
 C . 加入氯化钡溶液有白色沉淀生成,再加盐酸,沉淀不消失,一定有SO
C . 加入氯化钡溶液有白色沉淀生成,再加盐酸,沉淀不消失,一定有SO D . 焰色反应黄色火焰,一定有Na+ , 没有K+
D . 焰色反应黄色火焰,一定有Na+ , 没有K+
- (4分)小明想找到一种让物体快速冷却的方法.为此小明进行了如下的探究:小明注意到妈妈是把饭菜放在空气中冷却的,而厨房中适
- ______ I have will be yours sooner or later. A. Whatever
- 在研究同种哺乳动物的3个个体的2对相对性状时,发现其基因组成:甲为DBb;乙为DdBB;丙为dBb。下列推断错误的是 A
- 当人用手指将双耳堵住后,可出现的情况是:A.完全失去听觉; B.对听觉
- 诗人左思在其《咏史》中沉郁悲歌:“世胄蹑高位,英俊沉下僚。地势使之然,由来非一朝。”造成这一社会状况的制度原因是 A.征
- 某一动物死后,它所有的生理机能都停止了活动,当把它焚烧后,这一动物就不存在了。这说明 A. 物质的运动停止了
- “一山难容二虎”这一谚语,用生物学观点可以理解为( ) A.虎性情孤独,不群居 B.虎所需的生活空间很大 C.身
- A year after graduation, I was offered aposition teaching a
- 阅读下面的文字,完成题。 春天的梦 苏叔阳 黎明,窗外飘着雪花,静静地,静静地……啊,多像梦的使者。蓦地,几行诗句涌上心
- 读沿北回归线的东西向某剖面图,完成下列问题。 图15
- 随机抽取某中学甲乙两班各10名同学,测量他们的身高(单位:cm),获得身高数据的茎叶图如图7. (1)根据茎叶图判断哪个
- 一定量的石灰石与50g稀盐酸恰好完全反应,生成CO2 2.2g,求:(1)参加反应的CaCO3的质量;(2)盐酸的溶质质
- 花生油主要是从花生种子的( )中榨出来的。 A、胚根 B、胚芽 C、胚轴 D
- 国务院国资委10月22日公布的数据显示,今年上半年中央企业累计实现营业收入96874.6亿元,应交税费总额8514.2亿
- 3.填入下面一段文字横线处的语句,最恰当的一句是( ) 大数据的发展要遵循实践应用与理论升华相结合的科学路径
- 叶芽能发育成枝条,下列对叶芽发育的说法不正确的是 A.幼叶发育成叶 B.芽轴发育成茎 C.叶原基发育成幼叶
- When I was young, I liked totravel to places ______ could m
- 下图是某地区地形图,完成各题。与太湖平原、珠江三角洲等相比,图示地区成为商品粮基地的优势是
- 下列关于亚洲及欧洲人口的叙述,正确的是( ) A.在各大洲中,亚洲人口最多,欧洲人口密度最小 B.目前欧洲是世界上
- If a shop has chairs _______ women can park their men,women
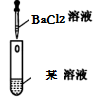
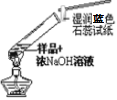

 ,该白色沉淀是BaSO4
,该白色沉淀是BaSO4


