硫酸根离子的检验 知识点题库
选项 | 实验 | 解释或结论 |
A | 用激光笔照射水玻璃溶液,有丁达尔现象 | SiO32﹣水解生成硅酸胶体 |
B | 在新制的氯水中加入碳酸钙粉末,充分搅拌 | 氯水中HClO的物质的量增加 |
C | 向包有Na2O2的脱脂棉滴少量水,脱脂棉燃烧 | Na2O2与H2O反应放热并有O2生成 |
D | 向某溶液中加入稀盐酸,再加入硝酸钡溶液生 成白色沉淀 | 原溶液中一定存在SO42﹣ |
-
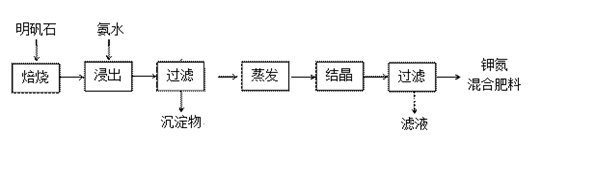
(1) 氨水浸出后得固体混合体系,过滤,滤液中除含K+、NH4+外,还含有大量的SO42-。检验SO42-的方法是
-
(2) 为测定混合肥料K2SO4、(NH4)2SO4中钾的含量,请完善下列步骤:
①称取钾氮肥试样并溶于水,加入足量溶液,产生白色沉淀。
②过滤、洗涤、。其中洗涤沉淀的方法为
③冷却、称重。
④若试样为m g,沉淀的物质的量为n mol,则试样中K2SO4的物质的量为:mol(用含有m、n的代数式表示)。
| 序号 | 实验事实 | 结论 |
| A | CO2的水溶液可以导电 | CO2是电解质 |
| B | Ca(ClO)2溶液中通入CO2产生白色沉淀 | 酸性:H2CO3>HClO |
| C | 向无色溶液中加入氯化钡溶液有白色沉淀生成,再加盐酸,沉淀不消失 | 原溶液中一定含有SO42- |
| D | 用铂丝蘸取某溶液在酒精灯火焰上灼烧直接观察火焰颜色,未见紫色 | 原溶液中不含K+ |
| 选项 | 实验目的 | 实验操作 |
| A | 配制0.4000mol·L−1的NaOH溶液 | 称取4.0g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至250mL容量瓶中定容 |
| B | 除去Mg粉中混有的Al粉 | 加入足量的NaOH溶液,过滤、洗涤、干燥 |
| C | 比较Fe3+和I2的氧化性强弱 | 向淀粉碘化钾溶液中滴入氯化铁溶液,溶液变蓝色 |
| D | 检验溶液中存在SO42‾ | 向未知溶液中先加入足量盐酸酸化,再加入BaCl2溶液 |

| 选项 | 操作 | 现象 | 结论 |
| A | 将铜粉加入 | 溶液变蓝 | 金属铜比铁活泼 |
| B | 向蔗糖中加入浓硫酸 | 蔗糖变成疏松多孔的海绵状的炭 | 浓硫酸具有脱水性和强氧化性 |
| C | 向含酚酞的NaOH溶液中通入 | 溶液红色褪去 | |
| D | 某溶液中滴加足量盐酸酸化的 | 生成白色沉淀 | 原溶液中一定有 |
-
(1) I.化合物A由三种元素组成,气体B是含氢量最高的烃。固体E既能溶于盐酸,又能溶于氢氧化钠溶液。按如下流程进行实验:
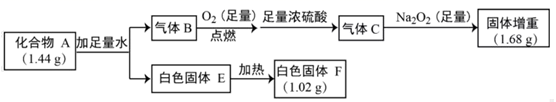
E的化学式为:,气体C与Na2O2反应的化学方程式为:
-
(2) A的化学式为:,A与足量盐酸反应的化学方程式为:
-
(3) Ⅱ.将ClO2通入NaOH和H2O2的混合溶液中,可制得一种高效漂白剂亚氯酸钠(NaClO2),实验装置如图所示:
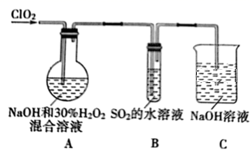
请回答:
写出A装置中发生反应的离子方程式
-
(4) 请设计实验方案探究通入足量的ClO2后,B装置溶液中存在的含有硫元素的微粒
| 实验 | 实验现象 |
| | ①品红溶液红色褪去,经检验溶液中含有SO42- ②加热褪色后的溶液至沸腾,未见颜色恢复,有气体溢出,可使蓝色石蕊试纸变红,遇淀粉碘化钾试纸,无明显变化。 |
| 选项 | 实验操作和现象 | 实验结论 |
| A | 取某溶液做焰色反应实验,观察到火焰为黄色 | 溶液中含有Na+ , 不含有K+ |
| B | 向久置的Na2SO3溶液中加入足量BaCl2溶液,出现白色沉淀;再加入足量稀盐酸,部分沉淀溶解 | 部分Na2SO3被氧化 |
| C | 向20%的蔗糖溶液中加入少量的稀硫酸,加热,再加入少量银氨溶液,未出现银镜现象 | 蔗糖未水解 |
| D | 向某溶液中加入KSCN溶液,溶液呈血红色 | 溶液中含Fe3+ , 不含Fe2+ |
-
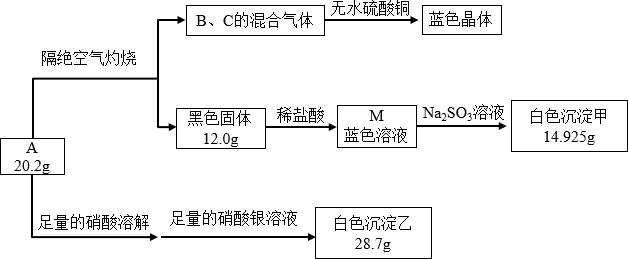
(1) 已知A在隔绝空气灼烧时发生的是非氧化还原反应,黑色固体是(写化学式)。
-
(2) 白色沉淀乙证明A中含元素。(写元素符号)
-
(3) 白色沉淀甲是一种氯化物,M溶液与Na2SO3溶液属于氧化还原反应,那么白色沉淀(写名称)。写出该反应的离子方程式,得到白色沉淀的方法是。检验硫酸根离子的操作。
-
(4) A的化学式为。
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向某溶液中先加入氯化钡溶液,再滴入盐酸 | 先产生白色沉淀,后白色沉淀不消失 | 该溶液中一定含有SO |
| B | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2(g) |
| C | 在0.1mol·L-1K2S溶液中滴加少量等浓度的ZnSO4溶液,再加入少量等浓度的CuSO4溶液 | 先产生白色沉淀,后产生黑色沉淀 | Ksp(ZnS)>Ksp(CuS) |
| D | 室温下,用pH试纸分别测定浓度均为0.1mol·L-1的Na2SO3和NaHSO3两种溶液的pH | pH:Na2SO3>NaHSO3 | HSO |
| 选项 | 实验操作 | 结论 |
| A | 溶液X的焰色反应呈黄色 | X中含 |
| B | 向固体Y中加入稀盐酸,有无色气体生成 | Y一定是碳酸盐 |
| C | 向固体Z中加入盐酸酸化的 | Z一定含有 |
| D | 向固体W中加入浓 | W一定含有 |
 溶液,产生白色沉淀,则溶液中一定含有大量的
溶液,产生白色沉淀,则溶液中一定含有大量的  B . 加入足量的
B . 加入足量的 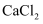 溶液,产生白色沉淀,则溶液中一定含有大量的
溶液,产生白色沉淀,则溶液中一定含有大量的  C . 向溶液中加
C . 向溶液中加  溶液,无明显变化,再加少量氯水,溶液呈血红色,则溶液中一定有
溶液,无明显变化,再加少量氯水,溶液呈血红色,则溶液中一定有  D . 先加入适量的盐酸酸化,再加入
D . 先加入适量的盐酸酸化,再加入 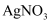 溶液,产生白色沉淀,则溶液中一定含有大量的
溶液,产生白色沉淀,则溶液中一定含有大量的 
选项 | 实验 | 现象 | 结论 |
A | ①某溶液中加入硝酸钡溶液 ②再加入足量盐酸 | ①产生白色沉淀 ②仍有白色沉淀 | 原溶液中不一定含有 |
B | 加热盛有NH4Cl固体的试管 | 试管底部固体消失、试管口有晶体凝结 | NH4Cl固体可以升华 |
C | 向久置于空气中的FeSO4溶液中滴入KSCN溶液 | 溶液变红 | FeSO4溶液完全变质 |
D | 水浴加热蔗糖与稀硫酸混合溶液,然后加入新制氢氧化铜悬浊液,再加热 | 未出现砖红色沉淀 | 蔗糖未发生水解 |
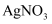 溶液产生白色沉淀,则证明该溶液中一定含
溶液产生白色沉淀,则证明该溶液中一定含 B . 取少量溶液加入足量稀盐酸,产生能使澄清石灰水变浑浊的气体,则证明该溶液中一定含有
B . 取少量溶液加入足量稀盐酸,产生能使澄清石灰水变浑浊的气体,则证明该溶液中一定含有 或
或 C . 先加入足量稀盐酸无明显现象,再加入
C . 先加入足量稀盐酸无明显现象,再加入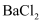 溶液,产生白色沉淀,证明该溶液中含有
溶液,产生白色沉淀,证明该溶液中含有 D . 用洁净的铂丝蘸取少许溶液,于酒精灯上灼烧,火焰的颜色为黄色,证明该溶液一定含
D . 用洁净的铂丝蘸取少许溶液,于酒精灯上灼烧,火焰的颜色为黄色,证明该溶液一定含
选项 | 实验操作 | 现象 | 结论 |
A | 向某溶液中加入稀盐酸酸化,再加入BaCl2溶液 | 酸化后溶液中无现象,再加溶液后观察到有白色沉淀生成 | 该溶液中存在SO |
B | 向苯酚浊液中加入Na2CO3溶液 | 溶液变澄清 | 酸性:苯酚>碳酸 |
C | 用洁净的铂丝蘸取某溶液进行焰色反应 | 焰色呈黄色 | 该溶液为钠盐溶液 |
D | 向FeCl2溶液中滴加KSCN溶液 | 溶液变红 | FeCl2已完全变质 |
- “木无本必枯,水无源必竭”。某市政府广开言路,首创了“信访民主听证评议制”。通过体察民情、了解民意,该市决定不建大广场大
- 李克强在全国综合配套改革试点工作座谈会上强调,我国30多年来取得的巨大成就,靠的是改革开放。从制度层面讲,改革为中国带来
- —I think you can ______ moneyto buy a birthday present for y
- 能分泌胆汁的器官是( ) A.胆囊 B.肝脏 C.胰腺 D.唾液腺
- 2009年9月,中国十七届四中全会提出:要在新形势下加强和改进党的建设。回答下题 在新形势下加强和改进党的建设的政治学依
- The workers _________ the glasses and marked on each box “Th
- 某工厂现有职工2a人(140<2a<280),且a为偶数,每人每年可创利b万元,据评估在生产条件不变的条件下,每裁员1人
- 下列不是19世纪中叶俄国批判现实主义作家列夫托尔斯泰的代表作的是( )A 、《战争与和平》 B、《
- 下列命题中,真命题是() A.相等的角是直角 B.不相交的两条线段平行 C.两直线平行,同位角互补 D.
- 为了证明酶的作用具有专一性,某同学设计了如下5组实验,分别选择一定的试剂进行检测,合理的实验方案是() 组别
- 有学者认为:“在文字发明以前,它是先民们对上古洪荒时代历史的一种夸张的记述,只要加以科学的分析,便不难发现其中蕴含的可靠
- 2010年11月17日国务院总理温家宝主持召开国务院常务会议,分析当前价格形势,研究部署稳定消费价格总水平、保障群众基本
- 体育课上,老师测量某同学的跳远成绩的依据是 ( )A.经过直线外一点,有且只有一
- 通货膨胀是2011年全球经济的最大风险,而新兴经济体面临的冲击将明显超过发达经济体。如何应对“通胀”成为我国2011年经
- 综合性学习。(6分) 活动一:班级准备开展“感受自然”的活动,请你完成下面两件事。 (1)为这次活动书写一条主题语
- 在图中画出斜面上“不倒翁”受重力的示意图,井画出重力相对于O点的力臂玩。(黑点表示“不倒翁”的重心)
- 肌肉注射时,药液进人人体后经过的一般途径是 ( ) A.血浆→组织液→淋巴→血浆→病原体 B.淋巴→血浆
- 若二次函数y=x2-6x+c的图像过A(-1,y1),B(2,y2),C(5,y3),则y1,y2,y3的大小关系是()
- Fans from miles around crowded into the stadium for the conc
- 图3为“某地地质剖面图”,其中C为沉积物,B、F、G为沉积岩,A、D为不同时期的岩浆岩,E为变质岩,据此完成5—6题。5
 溶液中
溶液中


 N2O4(g) △H<0
N2O4(g) △H<0 结合H+能力比SO
结合H+能力比SO  的强
的强 不含
不含 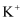

 溶液,产生的气体能使湿润的红色石蕊试纸变蓝
溶液,产生的气体能使湿润的红色石蕊试纸变蓝
 离子
离子


