硝酸的化学性质 知识点题库
检验Cl﹣所用的试剂为AgNO3和HNO3 , HNO3的作用是( )
A . 防止CO32﹣的干扰
B . 防止Cl﹣的干扰
C . 生成AgNO3沉淀
D . 防止NO3﹣的沉淀
下列叙述正确的是( )
A . Na、C,P,S分别在足量氧气中燃烧均生成一种相应氧化物:Na2O2、CO2、P2O5、SO3
B . 稀硝酸、稀硫酸均能将木炭氧化成二氧化碳,浓硝酸、浓硫酸都能使铁、铝钝化
C . 欲鉴别NO2、Br2(g)两种红棕色气体,将两种待测气体分別通入AgNO3溶液中
D . 将久置于空气中的Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,溶液变为红色,说 明Fe(NO3)2样品在空气中已变质
按要求完成以下方程式:
-
(1) 铝粉与四氧化三铁发生铝热反应的化学方程式:.
-
(2) 氯化铁溶液中通入SO2气体的离子方程式:.
-
(3) 偏铝酸钠溶液中加入氯化铝溶液的离子方程式:.
-
(4) 碳单质和浓硝酸反应的化学方程式:.
下列反应所得溶液中一定只含有一种溶质的是( )
A . 向稀硝酸中加入铁粉
B . 向稀盐酸中滴入少量的NaAlO2溶液
C . 向NaOH溶液中通入CO2气体
D . 向MgSO4、H2SO4的混合溶液中加入过量的Ba(OH)2溶液
在下列反应中,HNO3既表现出氧化性,又表现出酸性的是( )
A . H2S+2HNO3═S↓+2NO2↑+2H2O
B . CuO+2HNO3═Cu(NO3)2+H2O
C . 3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
D . 4HNO3  4NO2↑+O2↑+2H2O
4NO2↑+O2↑+2H2O
 4NO2↑+O2↑+2H2O
4NO2↑+O2↑+2H2O
取3张蓝色石蕊试纸放在玻璃上,然后按顺序分别滴加浓硝酸、浓硫酸、新制的氯水,3张试纸最后呈现的颜色是( )
A . 白、红、白
B . 红、黑、红
C . 红、红、白
D . 白、黑、白
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
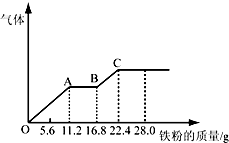
A . 混合酸中NO3-物质的量为0.2mol
B . OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+ , BC段产生氢气
C . 第二份溶液中最终溶质为FeSO4
D . H2SO4浓度为4mol•L-1
-
(1) 两个试剂瓶各盛装质量相同的浓硫酸和浓硝酸,分别敞口放置一段时间后,两溶液质量关系为m(硫酸) m(硝酸)(填“>”、“<”或“=”),由于浓硫酸和浓硝酸都具有强氧化性,所以冷的浓硫酸和浓硝酸都可以用(写金属名称)制容器盛放。
-
(2) 制备CuSO4和Cu(NO3)2
①下列有四种制备Cu(NO3)2的途径,其中最佳途径是(选填字母)
a. Cu
 Cu(NO3)2
Cu(NO3)2b. Cu
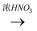 Cu(NO3)2
Cu(NO3)2c. Cu
 CuO
CuO  Cu(NO3)2
Cu(NO3)2d. Cu
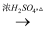 CuSO4
CuSO4  Cu(NO3)2
Cu(NO3)2② 向稀硫酸溶液中加入铜粉,然后通入热空气,可制得硫酸铜溶液,则发生反应的离子方程式为。
-
(3) 向200mL2mol/LHNO3溶液中加入足量铜粉,充分作用后,有m1g固体不溶物,继续 加入100mL 1mol/L硫酸溶液,充分作用后,还有m2g固体不溶物,则 m1 m2(填“>”、“<”或“=”),两者质量相差g(若两者相等,则此问不答)
在烧瓶中加入铜片和稀硝酸以制取较纯净的一氧化氮,反应开始后发现烧瓶中充满红棕色气体,这时的操作应是( )
A . 立即接上收集容器,用向下排空气法收集
B . 立即用排空气法收集
C . 待烧瓶中红棕色气体消失后,用排水法收集
D . 待烧瓶中的红棕色气体消失后,用向上排空气法收集
下列实验方案能达到实验目的的是( )
| 选项 | 实验方案 | 实验目的或结论 |
| A | 将盐酸酸化的双氧水滴入Fe(NO3)2溶液中,溶液变黄色 | H2O2的氧化性比Fe3+强 |
| B | 将一小块钠分别投入盛有水和乙醇的小烧杯中,钠与乙醇反应要平缓得多 | 乙醇羟基中的氢原子不如水分子中的氢原子活泼 |
| C | 将某气体通入品红溶液,溶液褪色 | 气体中一定有SO2 |
| D | 将铁棒和铜棒用导线连接后放入浓硝酸中,铜棒变细 | 铜的金属性强于铁 |
A . A
B . B
C . C
D . D
下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 | 实 验 操 作 | 现 象 | 解 释 或 结 论 |
| A | 过量的Fe粉中加入稀HNO3 , 充分反应后,滴入KSCN溶液 | 溶液呈 红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | 将少量浓硫酸滴入浓盐酸中 | 大量气体产生 | 硫酸的酸性比盐酸强 |
| C | 向蔗糖晶体中滴入几滴浓硫酸 | 白色固体变为黑色海绵状,有气体放出 | 说明浓硫酸有吸水性、氧化性 |
| D | 常温下,Fe、Al放入浓HNO3或浓H2SO4中 | 无明显 现象 | Fe、Al与浓HNO3或浓H2SO4发生钝化 |
A . A
B . B
C . C
D . D
硝酸铜受热分解产生的气体能使带火星的木条复燃,其原因是。
为证明稀硝酸与铜反应产物中气体为NO,设计如图实验(实验过程中活塞2为打开状态),下列说法中错误的是( )
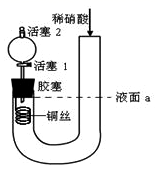
A . 关闭活塞1,加入稀硝酸至液面a处
B . 在装置左侧稍加热可以加快稀硝酸与铜的反应速率
C . 通过关闭或开启活塞1可以控制反应的进行
D . 反应开始后,胶塞下方有无色气体生成,还不能证明该气体为NO
下列化学实验事实及其解释都正确的是( )
A . 过量的铜屑与稀硝酸作用,反应停止后,再加入1 mol/L稀硫酸,铜屑又逐渐溶解是因为铜 可直接与1 mol/L稀硫酸反应
B . 粗锌与稀硫酸反应制氢气比纯锌快,是因为粗锌比纯锌还原性强
C . 铁钉放在浓硝酸中浸泡后,再用蒸馏水冲洗,然后放入CuSO4溶液中不反应,说明铁钉表面 形成了一层致密稳定的氧化膜
D . 工业制玻璃的主要反应之一:Na2CO3+SiO2  Na2SiO3+CO2↑,该反应原理可用“强酸H2CO3制弱酸H2SiO3”来解释
Na2SiO3+CO2↑,该反应原理可用“强酸H2CO3制弱酸H2SiO3”来解释
 Na2SiO3+CO2↑,该反应原理可用“强酸H2CO3制弱酸H2SiO3”来解释
Na2SiO3+CO2↑,该反应原理可用“强酸H2CO3制弱酸H2SiO3”来解释
化学与生产和生活密切相关,下列说法错误的是( )
A . 光导纤维的主要成分是二氧化硅
B . 二氧化硫能漂白织物利用了二氧化硫的强氧化性
C . 铝槽罐车可用于储运浓硝酸
D . 雷雨发庄稼体现了“自然固氮”的原理
部分含氮物质的类别与相应氮元素的化合价关系如图所示。下列说法正确的是( )
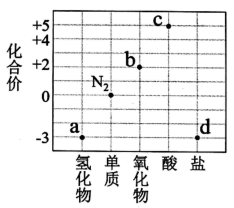
A . a与b在一定条件下可发生反应生成 B . 汽车尾气中的b物质是汽油不完全燃烧导致的
C . 常温下,金属
B . 汽车尾气中的b物质是汽油不完全燃烧导致的
C . 常温下,金属 在c的浓溶液中会钝化
D . 室温时,d的水溶液一定呈酸性
在c的浓溶液中会钝化
D . 室温时,d的水溶液一定呈酸性
 B . 汽车尾气中的b物质是汽油不完全燃烧导致的
C . 常温下,金属
B . 汽车尾气中的b物质是汽油不完全燃烧导致的
C . 常温下,金属 在c的浓溶液中会钝化
D . 室温时,d的水溶液一定呈酸性
在c的浓溶液中会钝化
D . 室温时,d的水溶液一定呈酸性
下列对有关事实的解释中正确的是( )
A . 常温下,浓硝酸、浓硫酸均可用铝槽贮存,说明铝既不与浓硝酸反应也不与浓硫酸反应
B . 浓硝酸在光照条件下颜色变黄,说明浓硝酸不稳定且见光容易分解
C .  可与NaOH溶液反应,也可与氢氟酸反应,说明
可与NaOH溶液反应,也可与氢氟酸反应,说明 为两性氧化物
D . Fe与稀
为两性氧化物
D . Fe与稀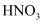 、稀
、稀 反应均有气泡产生,说明Fe与两种酸均发生了置换反应
反应均有气泡产生,说明Fe与两种酸均发生了置换反应
 可与NaOH溶液反应,也可与氢氟酸反应,说明
可与NaOH溶液反应,也可与氢氟酸反应,说明 为两性氧化物
D . Fe与稀
为两性氧化物
D . Fe与稀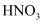 、稀
、稀 反应均有气泡产生,说明Fe与两种酸均发生了置换反应
反应均有气泡产生,说明Fe与两种酸均发生了置换反应
铁与不同浓度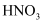 反应时的主要还原产物如图所示。下列说法正确的是( )
反应时的主要还原产物如图所示。下列说法正确的是( )
 反应时的主要还原产物如图所示。下列说法正确的是( )
反应时的主要还原产物如图所示。下列说法正确的是( )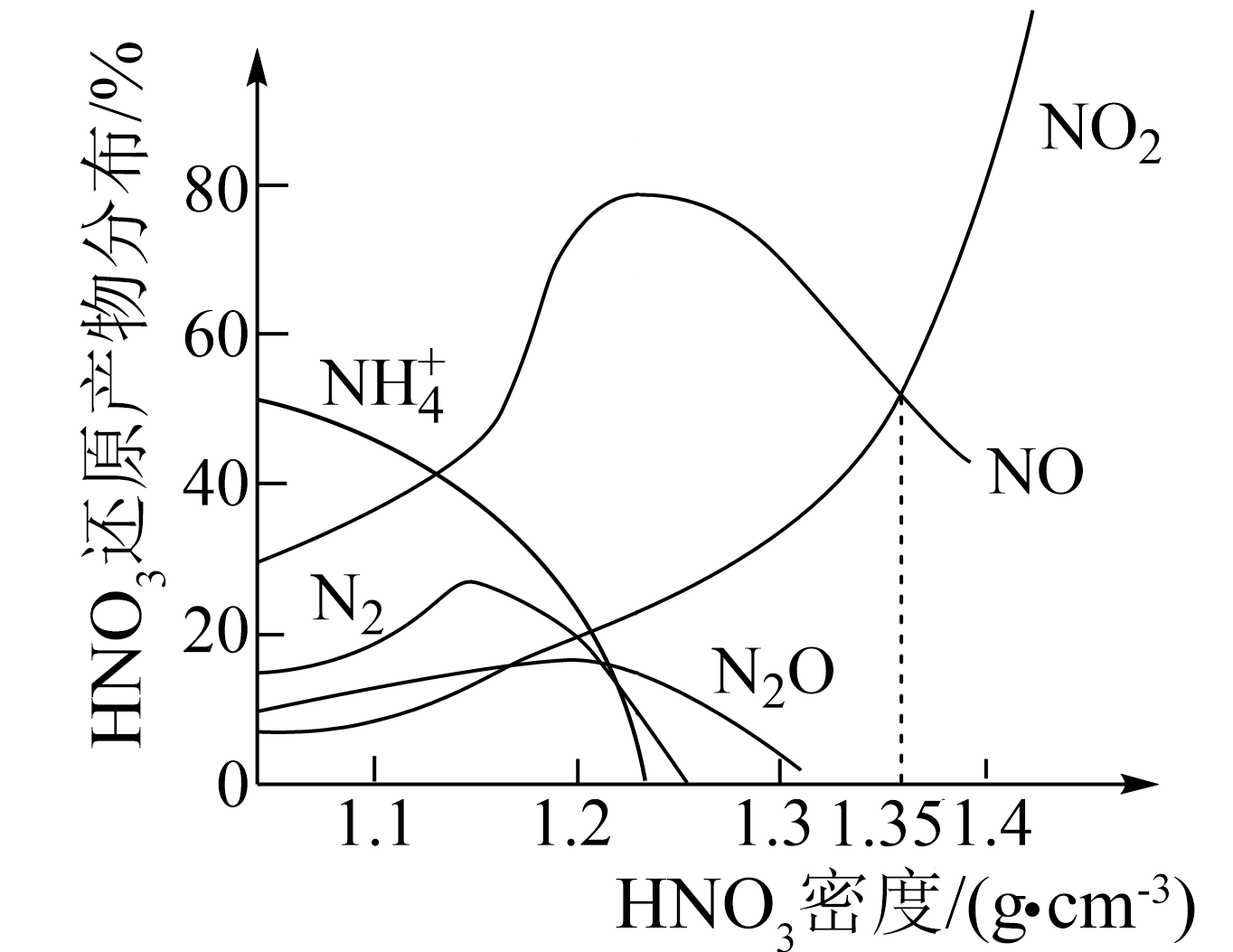
A . 无论硝酸的浓度大小,反应都一定会生成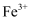 B . 浓硝酸为
B . 浓硝酸为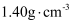 时,反应的主要还原产物为
时,反应的主要还原产物为 C . 浓硝酸为
C . 浓硝酸为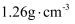 时,反应生成
时,反应生成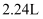 (标准状况下)气体,则参加反应的
(标准状况下)气体,则参加反应的 D . 铁与过量浓硝酸
D . 铁与过量浓硝酸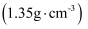 反应可表示为:
反应可表示为:
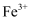 B . 浓硝酸为
B . 浓硝酸为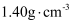 时,反应的主要还原产物为
时,反应的主要还原产物为 C . 浓硝酸为
C . 浓硝酸为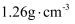 时,反应生成
时,反应生成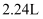 (标准状况下)气体,则参加反应的
(标准状况下)气体,则参加反应的 D . 铁与过量浓硝酸
D . 铁与过量浓硝酸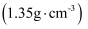 反应可表示为:
反应可表示为:
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析错误的是( )
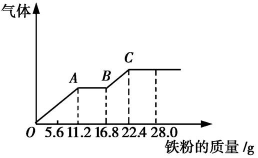
A . 混合酸中HNO3的物质的量浓度为2 mol·L-1
B . 原混合酸中H2SO4的物质的量为0.4 mol
C . OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+ , BC段产生氢气
D . 第二份溶液中的最终溶质为FeSO4
下列有关一些物质的性质说法正确的是( )
A .  能使鲜艳的红花褪色,说明
能使鲜艳的红花褪色,说明 具有漂白性
B . 加热条件下浓
具有漂白性
B . 加热条件下浓 能溶解金属铜,说明其具有强酸性
C . 常温下浓
能溶解金属铜,说明其具有强酸性
C . 常温下浓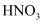 能使金属铝钝化,可以用铝槽车运输浓
能使金属铝钝化,可以用铝槽车运输浓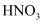 D . 金属钠保存在煤油中,实验剩余的金属钠不能放回原瓶
D . 金属钠保存在煤油中,实验剩余的金属钠不能放回原瓶
 能使鲜艳的红花褪色,说明
能使鲜艳的红花褪色,说明 具有漂白性
B . 加热条件下浓
具有漂白性
B . 加热条件下浓 能溶解金属铜,说明其具有强酸性
C . 常温下浓
能溶解金属铜,说明其具有强酸性
C . 常温下浓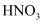 能使金属铝钝化,可以用铝槽车运输浓
能使金属铝钝化,可以用铝槽车运输浓 D . 金属钠保存在煤油中,实验剩余的金属钠不能放回原瓶
D . 金属钠保存在煤油中,实验剩余的金属钠不能放回原瓶
最近更新
- 正方形ABCD的边长为4,M为BC的中点,以MC为边在正方形ABCD内部作正方形CMNE(如图1),将正方形CMNE绕C
- (2012全国高考上海物理卷)质量相等的匀质柔软细绳A、B平放于水平地面,绳A较长。分别捏住两绳中点缓慢提起,直至全部离
- 23.阅读下面的材料,根据要求作文。 公鸡登上一堆沙土想找点食物,最后却翻出了一颗珍珠。公鸡说:“这个宝物尽管光彩夺目,
- --- Is this wine made grapes? --- Yes,
- 下图所示实验操作正确的是A.检查装置气密性 B.往试管中加入大理石 C.加热液体 D.固体药品的取用
- In 1988, a company in Ohio invented an alcohol-based hand cl
- (2014秋•东港市期中)读图,回答下列问题. (1)地球上海陆分布是(均匀,不均匀)的,陆地主要集中在北半球,地球上七
- 遗传物质脱氧核糖核酸(DNA)的分子直径为0.00000023cm,用科学记数法表示为cm.
- 设中,三个内角所对的边分别为,且 (1)求角的大小; (2)若.
- 实验室配制溶质质量分数一定的溶液时,可能涉及以下操作:A.称量 B.计算 C.溶解 D.装瓶贴标签。回答下列问题:
- 要鉴别己烯中是否混有少量甲苯,正确的实验方法是( ) A.先加足量的酸性高锰酸钾溶液,然后再加入溴水 B.先加
- You’ve probably heard such reports. Thenumber of college stu
- 下列各句中,加点的成语使用恰当的一句是( ) A.总书记提出了“三个代表”的重要理论,物理系半导体专业教研组的全体同志认
- 在120 ℃时,将12.4 g CO2和H2O(g)的混合气体缓缓通过过量的过氧化钠固体,充分反应之后,固体的质量增加6
- 阅读下面文言文,完成1—4题。 张克戬,字德祥,侍中耆曾孙也。第进士,历河间令,知吴县。吴为浙剧邑,民喜争,大姓
- 有关下列命题,其中说法错误的是 (A)命题“若,则
- 两个相同的容器分别装了质量相同的两种液体,用同一热源分别加热,液体温度与加热时间关系如图所示.根据图线可知() A.
- 基因工程与蛋白质工程的区别是 A.基因工程需对基因进行分子水平操作,蛋白质工程不对基因进行操作 B.基因工程合成的是天然
- 下列物质属于常见氧化剂的一组是() A.Cl2、O2、FeCl3、KMnO4 B.O2、KMnO4、C、H2 C.Na、
- 1.下列词语中加点的字,每对读音都不相同的一项是( ) A.星宿/宿舍 角色/角逐 狭隘/宁谧 隽永/隽秀



