硝酸的化学性质 知识点题库
-
(1) 美蓝是亚硝酸盐中毒的有效解毒剂,下列说法正确的是 .(选填编号)
a.解毒时美蓝表现氧化性b.中毒时亚硝酸盐发生氧化反应
c.解毒时高铁血红蛋白被还原d.中毒过程中血红蛋白显氧化性
-
(2) NaNO2中钠离子核外有 种不同能级的电子,三种元素对应的简单离子半径由大到小的顺序为
-
(3) Na、N、O分别与H形成的简单化合物中熔点最高的是 (填化合物化学式),试解释原因
-
(4) 已知NaNO2能发生如下反应(未配平):NaNO2+HI→NO+I2+NaI+H2O当有0.75mol HI被氧化时,在标准状况下产生气体的体积是 L.
-
(5) 有人将26中反应产生的NO收集到一个固定容积的密闭容器中,并在常温下将其压缩到1.01×107Pa,然后加热至50℃时,发现气体的压力迅速下降.当温度恢复到常温,压强降至略小于1.01×107Pa的
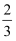 时,就不再改变.已知此过程中有一种产物是N2O.请写出生成N2O的反应方程式: .解释最后的气体压强略小于1.01×107Pa的
时,就不再改变.已知此过程中有一种产物是N2O.请写出生成N2O的反应方程式: .解释最后的气体压强略小于1.01×107Pa的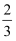 原因:
原因:
-
(6) 某工厂的废液中含有2%~5%的NaNO2直接排放会造成污染,下列试剂中①NaCl、②NH4Cl、③HNO3、④浓H2SO4 , 能使NaNO2转化为N2的是 .(选填编号)
-
(1) 写出下列反应的化学方程式:
①工业制漂白粉:;
②氯化亚铁溶液中通入氯气:.
-
(2) 写出下列反应的离子方程式:
③铁粉溶于稀硫酸:;
④稀硝酸与铜片的反应:.
①浓硝酸中滴入石蕊试液并微热
②氧化亚铁与浓硝酸反应
③氢氧化铝与浓硝酸反应
④碳与浓硝酸.
-
(1) 写出硝酸工业生产中相关的三个化学方程式:,,;
-
(2) 铝片与氢氧化钠溶液反应的离子方程式;
-
(3) 明矾溶液与过量氢氧化钡溶液反应的离子方程式;
-
(4) 在偏铝酸钠溶液中通入足量二氧化碳气体的离子方程式.
-
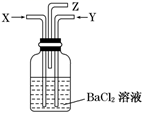
(1) 甲同学欲探究铜与稀硝酸反应产生的气体主要是NO,设计装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是含有一半空气的注射器。
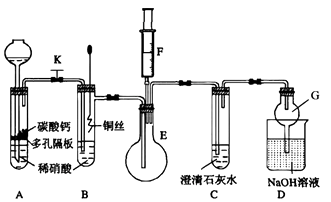
请回答有关问题:
①装置A中进行反应时打开止水夹K,当装置C中时,关闭止水夹K,试分析这样操作的目的是,A中反应的离子方程式为。
②在完成①中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是,B中反应的离子方程式为。
③为进一步证明产物是NO,将注射器F中的空气推入E中,看到的现象是。
④装置G的作用是。
-
(2) 同学们发现铜与稀、浓硝酸反应所得溶液的颜色不同,并记录如下:
将1 g细铜丝放入盛有10 mL的1 mol·L-1 HNO3溶液的试管中加热
铜丝表面有无色气体逸出,溶液变为天蓝色
将1 g细铜丝放入盛有10 mL的14 mol·L-1HNO3溶液的试管中
产生大量红棕色气体,溶液变为绿色,绿色由深到浅,未见到蓝色
有同学认为是铜与浓硝酸反应的溶液中溶解了生成的气体,也有同学认为是溶液中剩余硝酸浓度较大所致,同学们分别设计了以下4个实验来判断该看法是否正确,以下方案中可行的是(选填序号字母)。
a. 向上述绿色溶液中通入氮气,观察颜色变化
b. 加水稀释上述绿色溶液,观察颜色变化
c. 向饱和的硝酸铜溶液中不断滴加14 mol·L-1HNO3溶液
d. 向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
 Cu(NO3)2
B . Cu
Cu(NO3)2
B . Cu 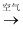 CuO
CuO 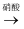 Cu(NO3)2
C . Cu
Cu(NO3)2
C . Cu 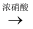 Cu(NO3)2
D . Cu
Cu(NO3)2
D . Cu 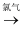 CuCl2
CuCl2  Cu(NO3)2
Cu(NO3)2
| 选项 | 实验操作 | 实验现象 | 实验推论 |
| A | 向某溶液中加入 | 未产生能使湿润红色石蕊试纸变蓝的气体 | 原溶液中不含有 |
| B | 测定饱和 | 前者 | |
| C | 向红热的木炭滴加浓硝酸 | 产生大量的红棕色气体 | 木炭和浓硝酸反应生成 |
| D | 向 | 有白色沉淀生成,四氯化碳层呈紫色 | 白色沉淀可能为 |
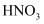 说法错误的是( )
说法错误的是( )
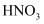 分解产生的
分解产生的  会溶解在其中
B . 将
会溶解在其中
B . 将 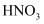 分解产生
分解产生  与
与  ,比值为
,比值为 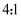 ,若将带火星的木条伸入该混合气体内,木条复燃,说明
,若将带火星的木条伸入该混合气体内,木条复燃,说明  也支持燃烧
C . 常温下,
也支持燃烧
C . 常温下,  和
和 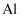 遇到浓硝酸会发生“钝化”,因此可以用
遇到浓硝酸会发生“钝化”,因此可以用  制容器来储存浓硝酸
D . 浓盐酸和浓硝酸体积按
制容器来储存浓硝酸
D . 浓盐酸和浓硝酸体积按 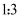 混合,可以得到“王水”
混合,可以得到“王水”
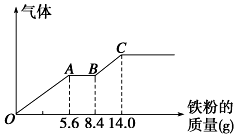
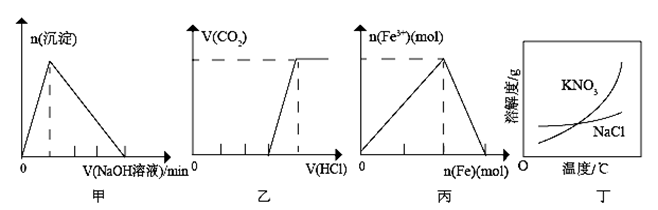
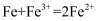 C . C点之后的溶液中溶质只有
C . C点之后的溶液中溶质只有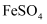 D . 原混合溶液中
D . 原混合溶液中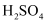 的浓度为1.5mol/L
的浓度为1.5mol/L
- 已知向量=(2,1),=(1,m),且,则实数m=.
- 某有机物含C 60%、H 13.33%,0.2 mol该有机物的质量为12 g,则它的分子式为() A.CH4
- 下列与生物进化相关的描述错误的是 A.不同物种之间、生物与无机环境之间在相互影响中,不断进化进而形成生物多样性 B.在自
- My elder brother wants to buy a _____ computer, so that he
- 22.阅读下面的材料,写一篇不少于800字的文章。 一只鸟站在树上,从来不怕树枝折断。因为它相信的不是树枝,而是它的翅膀
- 下列图象中x轴表示社会劳动生产率,y轴表示单位商品价值量。其中正确反映两者关系的是
- 短周期元素X、Y、Z在周期表中的位置关系如图所示,则下列叙述中正确的是 ( ) A.Z一定是活泼的金属元素 B.Y的最
- 对于短周期元素,下列说法正确的是( ) A.若两元素原子序数相差8,则周期数一定相差1 B.两种简单离子不可能相差
- 下面的漫画启示我们,办事情应当( )A. 脚踏实地,注重量的积累 B. 把握时机,促成质的飞跃 C.
- ﹣2,﹣1,0,四个数中,绝对值最小的数是() A. B.﹣2 C.0 D.﹣1
- 2004年4月,韩国拟将“端午节”申报世界文化遗产,此消息传来,引起国内强烈反响,“端午节”是中国的传统节日,有着深厚的
- 某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。 (1)A的分子式为_______________
- 历史学家萧功秦评述模式时说:“模式是如何从历史上演变过来的?可以用八个字来概括,那就是‘路径障碍,试错反弹’。”下列各项
- 如图2-2-10是某班50名学生身高的频率分布直方图(精确到1 cm),从左边起第一、二、三、四个小长方形的高的比是1∶
- 10.补写出下列名篇名句中的空缺部分。(6分) (1)白居易的《长恨歌》中以比喻手法描绘太真见汉家天子使者悲楚委屈落泪的
- 碘元素(元素符号I)具有预防和治疗甲状腺肿大的作用,人体缺碘时易患粗脖子病。为了消除碘缺乏症,我国政府规定居民的食用盐必
- 洋葱根尖生长点细胞所含的核酸中,含有碱基A、G、C、U的核苷酸种类有 A.4种 B.5种
- 你们班确定下星期一举行演讲会,大家推举你的同桌主持。为此他(她)心事重重。作为同学,请你为他(她)选择一种方法来控制不良
- 右边漫画《追星女》对美容的要求,主要没 有看到( ) A.关键的部分对事物整体的决定作用 B.部分要服从于
- 古代文天祥“人生自古谁无死,留取丹心照汗青”;今有夏明翰“砍头不要紧,只要主义真,杀了夏明翰,还有后来人。”这说明(
 溶液
溶液
 溶液和饱和
溶液和饱和  溶液的
溶液的  值
值 的水解程度小于
的水解程度小于 
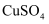 溶液中加入
溶液中加入  溶液,再加入四氯化碳振荡
溶液,再加入四氯化碳振荡