铵离子检验 知识点题库
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸.
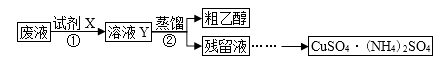
已知:[Cu(NH3)4]2++4H+=Cu2++4NH4+
请回答:
-
(1) 步骤①中,试剂X应采用。
-
(2) 甲、乙两同学取相同量的溶液Y分别进行蒸馏,收集到的馏出液体积相近,经检测,甲同学的馏出液中乙醇的含量明显偏低,可能的原因是。
-
(3) 设计实验方案验证硫酸铜铵固体中的NH4+。
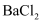 溶液,成白色沉淀,证明一定含有
溶液,成白色沉淀,证明一定含有 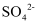 ,
C . 某无色溶液滴入酚酞试液是红色,该溶液一定是含有大量的
,
C . 某无色溶液滴入酚酞试液是红色,该溶液一定是含有大量的 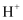 D . 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有
D . 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有 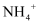
①钠放入水中后,沉在水下缓缓冒出气体
②Na2CO3和NaHCO3的溶液都可以使无色酚酞试液变红
③氢气在氧气或氯气中燃烧,都能观察到淡蓝色火焰
④将某气体通入品红溶液中,红色褪去,说明该气体一定是SO2
⑤向某溶液中加入烧碱溶液,加热后生成使湿润红石蕊试纸变蓝的气体,说明原溶液中有NH4+。
⑥过氧化钠与水反应放出大量热
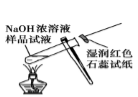 检验样品中是否含有NH4+
B .
检验样品中是否含有NH4+
B . 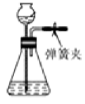 向长颈漏斗中加一定量水,并形成水柱,随后水柱下降至与瓶中液面相平,说明气密性好
C .
向长颈漏斗中加一定量水,并形成水柱,随后水柱下降至与瓶中液面相平,说明气密性好
C . 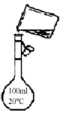 转移溶液
D .
转移溶液
D . 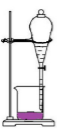 分离汽油和水
分离汽油和水
下列说法错误的是( )
-
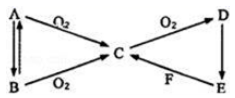
(1) 若A为淡黄色固体,B为气体,F为非金属单质。
①写出E转变为C的化学方程式。
②B在空气中能使银器表面失去金属光泽、逐渐变黑,反应的化学方程式为。
-
(2) 若B为能使湿润的红色石蕊试纸变蓝的气体。
①A的电子式为。
②做过银镜反应后的试管可用E的稀溶液清洗,反应的离子方程式为。
③在干燥状态下,向②反应得到的溶质中通入干燥的氯气,得到N2O5和一种气体单质,写出反应的化学方程式。
-
(1) 三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图所示,下列说法正确的是。
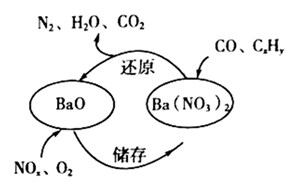
a.在转化过程中,氮元素均被还原
b.依据图示判断催化剂不参与储存和还原过程
c.还原过程中生成
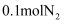 ,转移电子数为
,转移电子数为 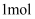
d.三效催化剂能有效实现汽车尾气中
 、
、 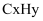 、
、  三种成分的净化
三种成分的净化 -
(2) 利用
 氧化氮氧化物反应过程如下:
氧化氮氧化物反应过程如下: 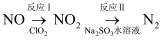 。反应Ⅰ的化学方程式是
。反应Ⅰ的化学方程式是 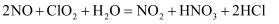 ,反应Ⅱ的离子方程式是。
,反应Ⅱ的离子方程式是。
-
(3) 加入过量次氯酸钠可使废水中
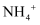 完全转化为
完全转化为  ,而本身被还原为
,而本身被还原为  。
。 ①检验废水中是否存在
 的方法是。
的方法是。②若处理废水产生了
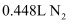 (标准状况),则需消耗浓度为
(标准状况),则需消耗浓度为 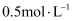 的次氯酸钠的体积为L。
的次氯酸钠的体积为L。
 4NO+6H2O
C . 氨的催化氧化反应中,若氧气过量,则有红棕色气体生成
D . 可以用玻璃棒蘸取浓硫酸检验氨的存在
4NO+6H2O
C . 氨的催化氧化反应中,若氧气过量,则有红棕色气体生成
D . 可以用玻璃棒蘸取浓硫酸检验氨的存在
|
选项 |
操作 |
现象 |
结论 |
|
A |
测定等浓度的NaCO3和Na2SO3溶液的pH |
前者pH比后者大 |
非金属性:S > C |
|
B |
滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 |
试纸不变蓝 |
不能确定原溶液中 含NH4+ |
|
C |
将HI溶液与CCl4溶液在试管中混合,加入 Fe(NO3)3溶液,振荡,静置 |
下层液体显紫红色 |
氧化性:Fe3+> I2 |
|
D |
将淀粉溶液与少量稀硫酸混合加热,然后加入新制的Cu(OH)2 , 悬浊液,并加热 |
无砖红色沉淀 |
淀粉未发生水解 |
选项 | 离子 | 试剂(或方法) | 实验现象 |
A |
|
| 溶液变红 |
B |
| 稀盐酸、 | 产生白色沉淀 |
C |
|
| 红色石蕊试纸变为蓝色 |
D |
| 稀盐酸 | 产生气泡 |
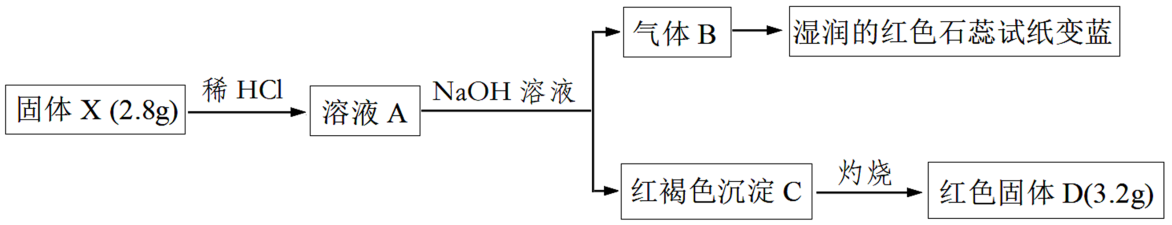
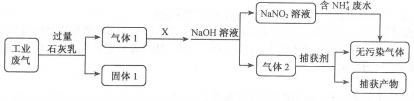
请回答:
-
(1) 固体X含有的元素是(用元素符号表示),其化学式为:
-
(2) 写出溶液A与NaOH溶液产生气体B的离子方程式:
-
(3) 写出固体X与稀HCl反应的化学方程式:
选项 | 实验操作和现象 | 结论 |
A | 向铜和浓硫酸反应后的混合液中加少量水,出现蓝色 | 该反应生成 |
B | 向碳酸钠粉末中加过量水,碳酸钠结块变成晶体,温度升高 | 该过程放热 |
C | 向某溶液中加入足量浓NaOH溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体 | 该溶液中含 |
D | 常温下将铝片放入浓硝酸中,没有明显现象 | 常温下铝与浓硝酸不反应 |
-
(1) 实验室制备FeCO3的流程如下:
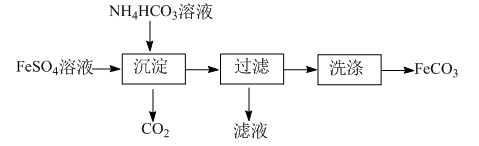
①保存FeSO4溶液时通常加入。
②“沉淀”时需要控制温度在35℃以下,其原因是;若将FeSO4溶液与氨水-NH4HCO3混合溶液反应,也能生成FeCO3沉淀,则此反应的离子方程式为;与图中流程相比,这种方法的优点是。
③检验滤液中是否含有NH
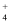 方法是。
方法是。 -
(2) 甲同学为了验证FeCO3高温下煅烧是否得到Fe2O3 , 做了如下实验:
步骤
实验操作
Ⅰ
取一定质量的FeCO3固体置于坩埚中,高温煅烧至质量不再减轻,冷却至室温
Ⅱ
取少量步骤Ⅰ所得固体置于一洁净的试管中,用足量的稀硫酸溶解
Ⅲ
向步骤Ⅱ所得溶液中滴加KSCN溶液,溶液变红
①根据上述现象写出空气中煅烧FeCO3 , 制备高纯氧化铁的化学方程式:。
②乙同学提出了不同的看法:因为Fe3O4也可以溶于硫酸,且所得溶液中也含有Fe3+。于是乙同学对步骤Ⅲ进行了补充:另取少量步骤Ⅱ所得溶液然后滴加(填试剂名称),若观察到,则说明溶液中含有Fe2+ , 煅烧产物可能是Fe3O4。
- 如下图示表明的是物种A与物种B的关系,则物种A与物种B之间的信息传递的方向是 ()A.信息只能由A传递给B B.信息只能
- —How did your students express their thanks to you on Teache
- There is a problem eachof us faces in following advice on em
- 若一个多边形的内角和与它的外角和相等,则这个多边形是() A.三角形 B.四边形 C.五边形 D.六边形
- 图为两湖泊(R1、R2)分布示意图,读图完成题。R1、R2湖泊分布在不同的 ( ) A.大洲
- 下列有关比较中,大小顺序排列错误的是
- 欧洲西部畜牧业发达的自然原因是()。 A.发达国家多 B.温带海洋性气候分布广 C.地形以高原为主 D.乳产品生产过程现
- 如图所示,小明体重600N,物体重180N,动滑轮重20N,绳重和摩擦不计。在拉力F的作用下,物体以0.1m/s的速度匀
- 基因型为AaBb和Aabb的两个体杂交,按照自由组合定律遗传,下列有关推测正确的是 () A. 表现型有4
- 读下图,回答关于图中山脉东西两侧水系特征叙述正确的是A.流域面积东部小、西部大B.河床坡度东部缓、西部陡C.流量季节变化
- 下列词语中有错别字的一组是 A.魁梧 磨炼 想像 相辅相成 B.蹩脚 扭扣 预告
- 下列各点既位于东半球又位于北半球的是( ) A、30°N,10°W B、30°S,10°W C、40°S,16
- 右图是创作于1958年的漫画,图中内容出现的主要原因是 A. 土地改革激发了农民的生产积极性
- 在一个密闭的容器内,用含有同位素14C的脱氧核苷酸合成一个DNA分子,然后加入普通的含有12C的脱氧核苷酸,经过n次复制
- 明代内阁和清代军机处的共同之处在于( ) A.统领六部处理各种事务 B.都是中央常设行政机构 C.体现
- 下表为我国甲、乙两城市某日日出日落时间(北京时间)统计表,据此完成: 城 市日出时间日落时间 甲5:2819:00 乙
- 阅读下面的文言文,完成下面试题。 道学传序 陈献章 自炎汉迄今,文字记录著述之繁,积数百千年于天下,至于汗牛充栋,犹未已
- 化学与人类生活息息相关。请回答下列问题。 (1)生活中鉴别羊毛线和棉线的方法是 。 (2)可用 (填名称)来
- 下列反应的离子方程式书写正确的是( ) A.氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-=BaSO4↓
- (本题满分50分)已知无穷数列满足,, .1)对于怎样的实数与,总存在正整数,使当时恒为常数? 2)求通项

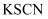 溶液
溶液
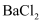 溶液
溶液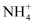
 溶液共热、干燥的红色石蕊试纸
溶液共热、干燥的红色石蕊试纸





