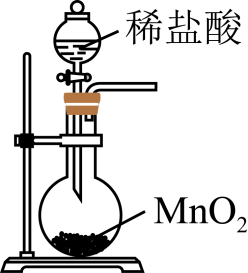
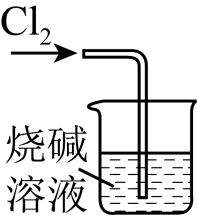氯气的实验室制法 知识点题库
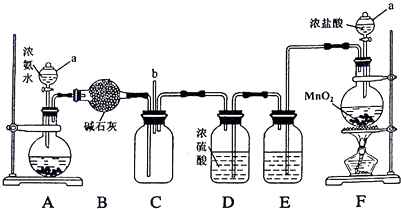
请回答下列问题:
-
(1) 仪器a的名称为;装置A的圆底烧瓶中盛放的固体物质可选
用(填序号).
a.氯化钠 b.氢氧化钠 c.碳酸钙
-
(2) 装置F的圆底烧瓶中发生反应的离子方程式为;装置E的洗气瓶中盛放的试剂为,其作用是.装置D中浓硫酸的作用是.
-
(3) 反应过程中,装置C的集气瓶中有大量白烟产生,另一种产物为空气的主要成分之一,该反应的化学方程式为.
-
(4) 从装置C的b处逸出的尾气中含有少量Cl2 , 为防止其污染环境,可将尾气通过盛有溶液的洗气瓶.
-
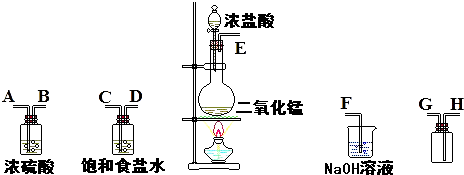
(1) 连接上述仪器的正确顺序(填各接口处的字母):接;接;接;接.
-
(2) 在制备氯气的发生装置中,用到的玻璃仪器除酒精灯外,还有.
-
(3) 写出用如图装置制备氯气的离子方程式:
-
(4) A、B两组同学分别用两种方法制取氯气:A组用含146g HCl的浓盐酸与足量的二氧化锰反应;B组用87g二氧化锰与足量的浓盐酸反应,则所得氯气的物质的量的关系为AB(填“>”、“<”或“=”)
-
(5) 实验中饱和食盐水的作用是:
-
(6) 写出氯气尾气吸收的化学方程式:.
-
(7) 如何验证氯气已经收集满?
-
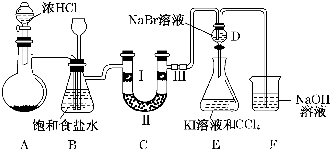
(1) 若A装置中固体药品为MnO2 , 其化学方程式为
-
(2) 装置B的作用:.
-
(3) 装置C的作用是验证氯气是否具有漂白性,Ⅰ处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是、.
-
(4) 设计装置D、E的目的是比较氯、溴、碘的氧化性,反应一段时间后关闭D取下E并充分振荡,可观察到E中的现象为.
-
(5) 请用化学方程式说明装置F的作用:.
-
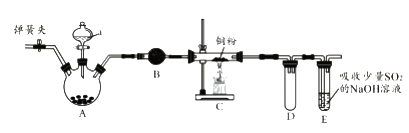
(1) A中固体是氯酸钾,液体a是浓盐酸,写出该反应的化学方程式:。
-
(2) B为干燥装置,加入的固体是;欲净化氯气,A、B间应添加一个盛有的洗气瓶。
-
(3) C中的反应现象是;D的作用是。
-
(4) 已知E中发生的反应为:Cl2+Na2SO3+2NaOH
 2NaCl+Na2SO4+H2O。E中吸收尾气一段时间后,吸收液(强碱性)中肯定存在:Cl-、OH-和SO42-。某兴趣小组认为该吸收液中还可能存在ClO-和SO32-。
2NaCl+Na2SO4+H2O。E中吸收尾气一段时间后,吸收液(强碱性)中肯定存在:Cl-、OH-和SO42-。某兴趣小组认为该吸收液中还可能存在ClO-和SO32-。a.甲同学认为该吸收液中ClO-和SO32-不能同时存在,其理由是(用离子方程式表示)。
b.乙同学为了检验吸收液中是否含有SO32- , 取少量吸收液于试管中,加适量稀硫酸酸化后,滴加品红溶液,发现品红溶液褪色。据此推断该吸收液中一定有SO32-。乙同学的推断是否正确?(填“正确”或“不正确”),理由是。
c.请设计实验检验吸收液中是否含有ClO-(写出实验步骤、现象和结论)。
-
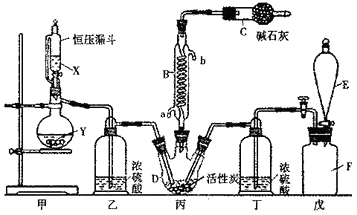
(1) 仪器E的名称是,由B的使用可知SO2与氯气之间的反应属于(填“放”或“吸”)热反应,B处反应管冷却水应从 (填“a”或“b”)接口通入。如果将丙装置放入冰水中,会更有利于二氯化砜的生成,其原因是。
-
(2) 试剂X、Y的组合最好是。
a.98%硫酸和铜 b.稀硝酸和亚硫酸钠固体 c.60%硫酸和亚硫酸钾固体
-
(3) 戊是贮气装置,则E中的试剂是;若缺少装置乙和丁,潮湿的氯气和二氧化硫之间发生反应的化学方程式是.
-
(4) 取1.00g蒸馏后的液体,小心地完全溶于水,向所得的溶液中加入足量氯化钡溶液,测得生成沉淀的质量为1.50g,则所得馏分中二氯化砜的质量百分含量为 %(结果保留小数点后1位)。
-
(5) 二氯化砜应储存于阴凉、干燥、通风良好的库房,但久置后微显黄色,其原因是。
-
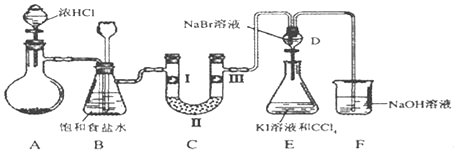
(1) 若装置A中制备氯气选用的药品为固体二氧化锰和浓盐酸,请写出装置 A 中的化学反应方程式:.
-
(2) 装置 B 中长颈漏斗的作用是
-
(3) 装置 C 为研究 Cl2 是否具有漂白性,现有:
①干燥的有色布条
②湿润的有色布条
③碱石灰
④浓硫酸
⑤无水氯化钙,其中Ⅰ处为Ⅲ处为①,则Ⅱ处为:(填上述物质中的序号)
-
(4) 设计装置 D、E 的目的是比较氯、溴、碘单质的氧化性强弱.当向 D 中缓缓通入一定量氯气时,可以 看到 D 中无色溶液逐渐变为橙色,再打开 D 装置的活塞,使 D 中溶液滴入 E 装置,振荡锥形瓶后静置一会儿,可以观察到下层液体呈紫红色.同学们经过认真讨论后认为该实验方案仍有不足,理由是
-
(5) 装置 F 的作用是吸收尾气,在烧杯中发生反应的化学方程式为.
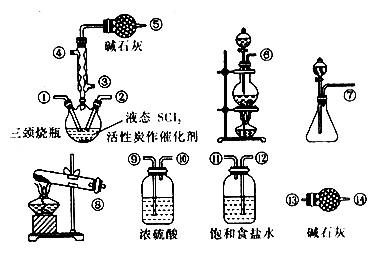
已知:①SOCl2遇水剧烈反应,液面上产生白雾,并有气体产生。
②SOCl2沸点为77℃,SCl2的沸点为 50 ℃。
请回答:
-
(1) 实验室制取SOCl2的反应方程式为。
-
(2) 实验室制取SOCl2在三颈烧瓶中合成,整个装置所选仪器的连接顺序是⑥→ →①,→②(某些仪器可以重复使用)。
-
(3) 使用冷凝管的作用是;冷凝管上连接的干燥管的作用是 。
-
(4) 实验结束后,将三颈烧瓶中混合物分离实验操作名称是。
-
(5) 若反应中消耗的Cl2的体积为896mL (已折算为标准状况,SO2足量) 最后得到纯净的SOCl26.76g,则SOCl2的产率为(保留二位有效数字)。
-
(6) 取少量的SOCl2加入足量NaOH溶液,振荡静置得到无色溶液,检验溶液中存在Cl-的方法是。
-
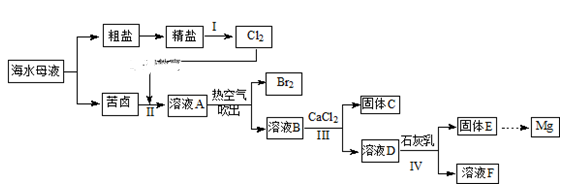
(1) 写出实验室制备氯气的化学方程式;
-
(2) 海水淡化的方法还有(写出一种);
-
(3) I中,电解饱和食盐水的工业生产叫做氯碱工业,写出该反应的离子方程式;
-
(4) Cl2和Br2均为双原子分子,从原子结构的角度解释其原因;
-
(5) Ⅲ中,加入适量CaCl2固体的目的是;
-
(6) 写出IV中反应的离子方程式;
-
(7) 与过程II类似,工业上常用“空气吹出法”实现海水提溴,将1m3海水浓缩至1L,使用该法最终得到36g Br2 , 若提取率为60%,则原海水中溴的浓度为 mg/L。
-
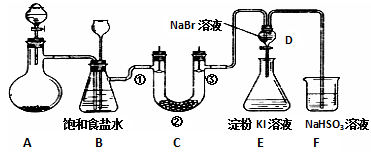
(1) 制备氯气选用的药品为:漂白粉固体和浓盐酸,相关的化学反应方程式为。
-
(2) 装置B的作用之一是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象。
-
(3) 装置C的实验目的是验证氯气是否具有漂白性,为此C中①、②、③依次放入(选填表中字母)。
①
②
③
a
干燥的有色布条
碱石灰
湿润的有色布条
b
干燥的有色布条
硅胶
湿润的有色布条
c
湿润的有色布条
浓硫酸
干燥的有色布条
d
湿润的有色布条
无水氯化钙
干燥的有色布条
-
(4) 设计装置D、E的目的是比较氯、溴、碘的非金属性强弱。当向D中缓缓通入一定量氯气时,可以看到无色溶液逐渐变为色,说明氯的非金属性大于溴;之后打开活塞,将装置D中少量溶液加入装置E中,振荡;观察到的现象是,则说明溴的非金属性大于碘。
-
(5) 有同学提出该实验方案仍有不足,请说明其中的不足及后果。
①;②。
请完成下列问题:
-
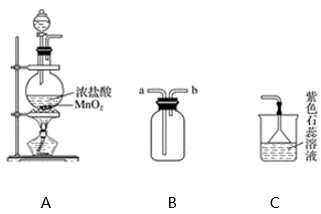
(1) 装置A中发生反应的离子方程式为。
-
(2) 装置B如图中所示正放,则连接A的接口是(填序号)。
-
(3) 实验中可观察到装置C中紫色石蕊溶液的现象是,其原因。
-
(4) 取出B中的集气瓶进行氯气与铜的反应实验,应该进行的操作是,然后立刻放入充满氯气的集气瓶中。实验中有同学提出应该在集气瓶底先放少量的水或细沙,你认为(填“需要”或“不需要”)放,理由是。
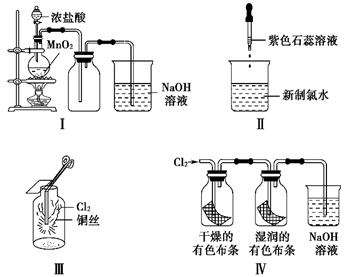
 MnCl2+Cl2↑+2H2O,据此回答下列问题:
MnCl2+Cl2↑+2H2O,据此回答下列问题:
-
(1) 其中MnO2发生了反应,是剂;每4分子氯化氢中只有分子发生了反应,盐酸是剂,氧化剂和还原剂个数比是。
-
(2) 用双线桥法表示电子转移的方向和数目:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
-
(3) 该实验室制取氯气反应的离子方程式为
-
(1) 制备CuCl2·2H2O晶体:
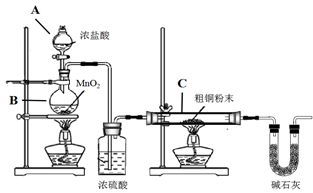
① B装置中发生反应的化学方程式是
② 装置C中粗铜粉末(含杂质Fe)与气体充分反应时的生成物是
③ 反应完成后,将C中的固体用稀盐酸完全溶解,再调节pH值除杂,经一系列操作便可获得CuCl2·2H2O晶体。溶解C中生成物固体时,有时会加入少量双氧水,目的是
-
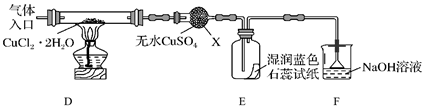
(2) 制取CuCl,为了制取CuCl采用如图所示装置进行实验(夹持仪器略):
已知:
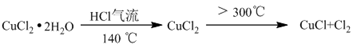
④仪器X的名称是
⑤实验操作的先后顺序是a→→e(填操作的编号)。
a.检查装置的气密性后加入药品 b.熄灭酒精灯,冷却
c.在“气体入口”处通入干燥HCl d.点燃酒精灯,加热
e.停止通入HCl,然后通入N2
⑥装置F中NaOH溶液的作用是。
⑦ 反应结束后,取出CuCl产品进行实验,发现其中含有少量的CuCl2或CuO杂质。请分析产生CuCl2杂质的原因是
方法Ⅰ NaClO + 2HCl(浓) = NaCl + Cl2↑ + H2O;
方法Ⅱ 4HCl(g) + O2(g) = 2H2O(g) + 2Cl2(g) ΔH = a kJ·mol−1
上述两种方法涉及的反应在一定条件下均能自发进行。利用方法Ⅰ制备Cl2时,下列装置能达到实验目的的是( )
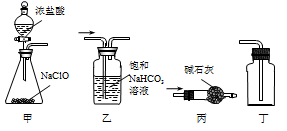
-
(1) 工业利用氯气和石灰乳反应可制得漂白粉, 其化学方程式为,漂白粉的有效成分是。
-
(2) 下列收集
 的正确装置是_______。
A .
的正确装置是_______。
A .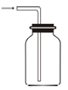 B .
B . 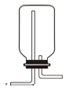 C .
C . 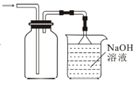 D .
D . 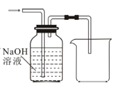
-
(3) 某同学设计了如图实验装置进一步研究氯气的漂白性并确定真实起漂白作用的物质,已知通入的氯气中还含有空气和水蒸气。回答下列问题:
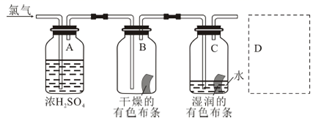
①浓
 的作用是。
的作用是。②与研究目的直接相关的实验现象是。
③将
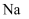 在盛有氯气的集气瓶中燃烧,其反应的化学方程式是。
在盛有氯气的集气瓶中燃烧,其反应的化学方程式是。④该实验设计存在事故隐患,应在D处增加一装置,该装置中应加入
 溶液以除去多余的氯气,请用化学方程式表示反应原理。
溶液以除去多余的氯气,请用化学方程式表示反应原理。
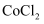 )常用作干湿指示剂、氨的吸收剂、防毒面具和肥料添加剂等。
)常用作干湿指示剂、氨的吸收剂、防毒面具和肥料添加剂等。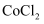 为蓝色粉末,易溶于水和有机溶剂,易升华,吸水潮解会变成红色。某化学实验小组拟选取下列装置来制备无水二氯化钴(装置不能重复使用)。
为蓝色粉末,易溶于水和有机溶剂,易升华,吸水潮解会变成红色。某化学实验小组拟选取下列装置来制备无水二氯化钴(装置不能重复使用)。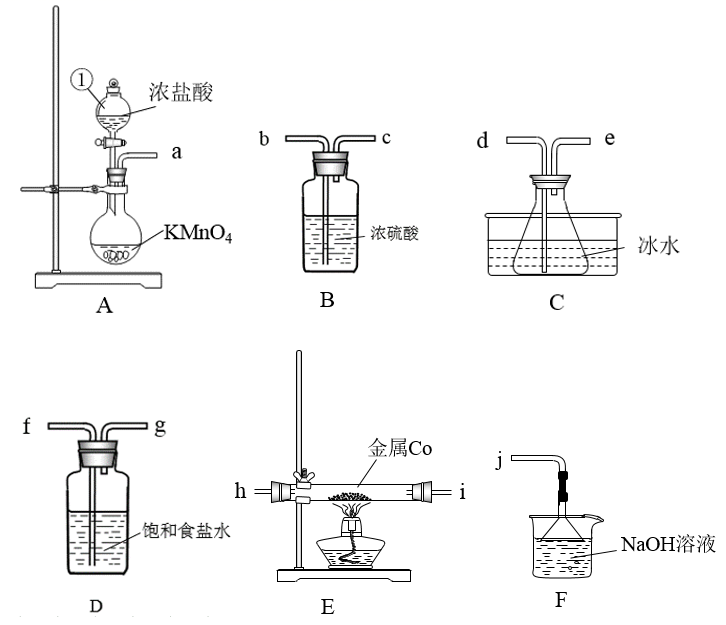
-
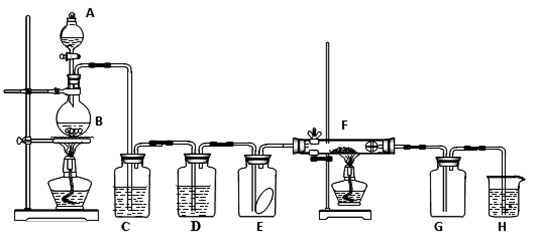
(1) 仪器①的名称是,装置
 中发生反应的离子方程式为。
中发生反应的离子方程式为。
-
(2) 根据气流的方向,装置导管口的连接顺序为
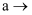
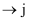 。
。
-
(3) 连接装置,检查气密性,装入药品后,先让
 中发生反应,再点燃
中发生反应,再点燃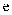 处酒精灯的目的是。
处酒精灯的目的是。
-
(4)
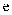 中发生反应的化学方程式为。实验过程中发现,用上述装置制备得到的
中发生反应的化学方程式为。实验过程中发现,用上述装置制备得到的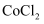 不是蓝色的,而是红色的,原因可能是,若要避免此现象的发生,可采取的措施是。
不是蓝色的,而是红色的,原因可能是,若要避免此现象的发生,可采取的措施是。
-
(5) 实验过程中,装置
 所起的作用是。
所起的作用是。
-
(1) 仪器A的名称是。
-
(2) 写出MnO2与浓盐酸反应的化学方程式。
-
(3) 装置C中盛装的溶液是,D中试剂的作用是。
-
(4) E中的红色布条是否褪色?(填“是”或“否”),写出F中反应的化学方程式:。
-
(5) H中的试剂为,其作用是,写出H中发生反应的离子方程式。
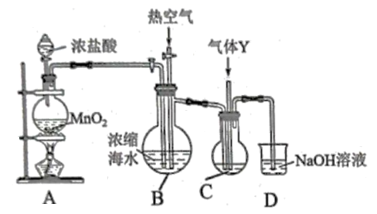
回答下列问题:
-
(1) 浓缩海水中主要存在的一种含溴微粒是。
-
(2) 装置A中制备
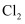 的化学方程式为。
的化学方程式为。
-
(3) 写出装置B中的离子反应方程式。
-
(4) 装置C中可装
 的水溶液或者
的水溶液或者 溶液,吸收从装置B中热空气吹出来的
溶液,吸收从装置B中热空气吹出来的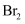 蒸汽。
蒸汽。①若用
 的水溶液吸收,反应的方程式为.吸收完毕后,通入的气体Y可为(填化学式),充分反应可得
的水溶液吸收,反应的方程式为.吸收完毕后,通入的气体Y可为(填化学式),充分反应可得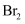 单质。
单质。②若用
 溶液吸收,反应后有
溶液吸收,反应后有 、
、 产生,写出此反应的离子方程式:,待吸收完后通入
产生,写出此反应的离子方程式:,待吸收完后通入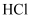 气体,可生成
气体,可生成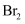 单质。
单质。③为提取装置C混合液中
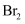 单质,可以加入萃取其中的
单质,可以加入萃取其中的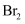 。
。 -
(5) 装置B已经得到
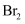 单质,增加装置C及对应实验操作的目的是。装置D的作用是。
单质,增加装置C及对应实验操作的目的是。装置D的作用是。
 共热[或用
共热[或用 (s)与浓盐酸混合]制取氯气,实验室制取氯气并探究其性质,下列装置不能达到相应实验目的的是 ( )
(s)与浓盐酸混合]制取氯气,实验室制取氯气并探究其性质,下列装置不能达到相应实验目的的是 ( )A | B | C | D |
|
|
|
|
制取氯气 | 验证氧化性 | 验证漂白性 | 吸收尾气 |
- 以下家庭食品制作中,发生化学变化的是 ( ) A.
- 下列对基因突变描述正确的是 () A.诱变育种能明显缩短育种年限 B.它为生物进化提供了原始材料 C.产生了等位基因,丰
- 化学课外活动中,老师为大家演示了如图1所示的趣味实验﹣﹣“魔棒生烟”,该实验原理的微观示意图如图2所示.(1)图示2反应
- B......
- 一定体积0.01mol/L的稀硝酸溶液恰好能氧化一定质量的铁、铝混合物,已知两种金属均被氧化为最高价态,还原产物只有NO
- R1和R2两只电阻器串联在某电路中,R1、R2两端的电压之比为5:4,若把它们并联后接到另一电路中,通过R1、R2的电
- 如图,△ACB中,∠ACB=90°,在AB的同侧分别作正△ACD、正△ABE和正△BCF. 若四边形CDEF的周长是24
- 如图,已知⊙O圆心是数轴原点,半径为1,∠AOB=45°,点P在数轴上运动,若过点P且与OA平行的直线与⊙O有公共点,设
- 在ABC中,内角A,B,C的对边分别为a,b,c.已知. (I) 求的值; (II)
- 设x,y满足约束条件,则的取值范围是 A.[0,2] B.[0,3]
- 水冷却后,除了会凝固成冰晶体外,还会形成玻璃态。它是由液态水急速冷却到-108℃时形成的,玻璃态的水与普通液态水的密度相
- ......
- What can we students do _____ the environment? A.to protect
- 由Na2SO4、Na2SO3和Na2S三种物质组成的混合物中,含氧元素的质量分数为22%,则其中钠元素的质量分数为()
- The hostess left the money on the table _____purpose to test
- 下面四幅图是同纬度的四个地区,其中气温日较差最小的是① ② ③
- 下列加点字读音完全不相同的一组是:( ) A.惶急 皇冠 装潢 炎皇子孙
- -Can you understand me? -Sorry. I can _________ understand
- 15.(1)、 ,不尽长江滚滚来。 (2)、地崩山摧壮士死,
- 上题中反射弧的中枢神经和反射类型分别是( ) A.脊髓和简单反射 B.脊髓和复杂反射C.大脑和简单反