铜的电解精炼 知识点题库
粗铜中一般含有锌、铁、银、金等杂质.在如图所示的装置中,甲池的总反应方程式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.接通电路一段时间后,纯Cu电极质量增加了3.2g.在此过程中,下列说法正确的是( )

A . 甲池中电解质溶液的pH值减小
B . 乙池中CuSO4溶液的浓度不变
C . 甲池中理论上消耗空气的体积是2.8L(空气中O2体积分数以20%计算)
D . 甲池通入CH3OH一极的电极反应为:CH3OH﹣6e﹣+2H2O═CO32﹣+8H+
中学阶级介绍的电解原理的应用主要有三种:一是氯碱工业、二是电解精炼铜、三是电解冶金.下列关于这三个工业生产的描述中正确的是( )
A . 电解精炼铜时,负极反应式:Cu2++2e﹣=Cu
B . 氯碱工业和电解精炼铜中,阳极都是氯离子放电放出氯气
C . 在氯碱工业中,电解池中的阴极产生的是H2 , NaOH在阳极附近产生
D . 电解精炼铜时,应用粗铜作阳极、精铜作阴极,可溶性铜盐作电解质溶液
电解精炼粗铜时,下列叙述不正确的是( )
A . 与电源正极相连的电极是粗铜板
B . 阴极发生反应:Cu2++2e﹣═Cu
C . 电解池的阳极材料为粗铜
D . 粗铜板上发生还原反应
下列描述中,不符合生产实际的是( )
A . 电解法精炼粗铜,用纯铜作阴极
B . 电解熔融的氧化铝制取金属铝,用铁作阳极
C . 在镀件上电镀锌,用锌作阳极
D . 电解饱和食盐水制烧碱,用涂镍碳钢网作阴极
下列关于电解法精炼粗铜的叙述中不正确的是( )
A . 粗铜板与电源的正极相连
B . 电解时,阳极发生氧化反应,而阴极发生的反应为:Cu2++2e﹣=Cu
C . 粗铜中所含Ni、Fe、Au、Ag等金属杂质,电解后以单质形式沉积槽底,形成阳极泥
D . 电解铜的纯度可达99.95%~99.98%
下列关于铜电极的叙述中正确的是( )
A . 铜锌原电池中铜是负极
B . 用电解法精炼粗铜时粗铜作阳极
C . 在铁上电镀铜时用铜作阴极
D . 电解稀硫酸时用铜作阳极,阳极产生氧气
根据图示回答,下列说法不正确的是( )
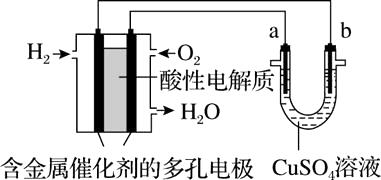
A . 此装置用于铁表面镀铜时,a极为铁
B . 此装置用于电镀铜时,硫酸铜溶液的浓度不变
C . 燃料电池中正极反应为  O2+2e-+2H+=H2O
D . 若用该装置进行粗铜的精炼,当有1 mol水生成时,可得到64 g精铜
O2+2e-+2H+=H2O
D . 若用该装置进行粗铜的精炼,当有1 mol水生成时,可得到64 g精铜
 O2+2e-+2H+=H2O
D . 若用该装置进行粗铜的精炼,当有1 mol水生成时,可得到64 g精铜
O2+2e-+2H+=H2O
D . 若用该装置进行粗铜的精炼,当有1 mol水生成时,可得到64 g精铜
如下图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
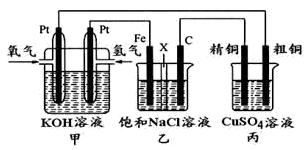
根据要求回答相关问题:
-
(1) 甲装置中通入氧气的电极为(填“正极”或“负极”),负极的电极反应式为。
-
(2) 乙装置中铁电极为(填“阳极”或“阴极”),石墨电极(C)上发生反应(填“氧化”或“还原”),其电极反应式为。
-
(3) 反应一段时间后,乙装置中生成氢氧化钠主要在区。(填“铁极”或“石墨极”)
-
(4) 如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将(填“增大”“减小”或“不变”)。
-
(5) 若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为;丙装置中阴极析出铜的质量为。
-
(1) 工业上制取纯净的CuCl2·2H2O的主要过程是
①将粗氧化铜(含少量Fe)溶解于稀盐酸中,加热、过滤,调节滤液的pH为3;
②对①所得滤液按下列步骤进行操作:
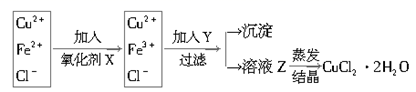
已知:
物质
Fe(OH)2
Cu(OH)2
Fe(OH)3
Ksp/25 ℃ mol3·L-3
8.0×10-16
2.2×10-20
4.0×10-38
完全沉淀时的pH范围
≥9.6
≥6.4
3~4
请回答下列问题:
①加入的氧化剂X,下列物质最好选用的是 .
A.KMnO4 B.H2O2 C.氯水 D.HNO3
②加入Y的作用是,Y的化学式为。
③溶液乙在蒸发结晶时应注意:。
-
(2) 如图为相互串联的甲、乙两个电解池,试回答下列问题:
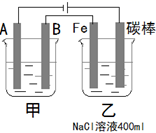
甲池若为用电解原理精炼铜的装置,阴极增重19.2 g,则乙池阳极放出气体在标准状况下的体积为L(不考虑气体的溶解情况)
关于下列装置说法正确的是( )
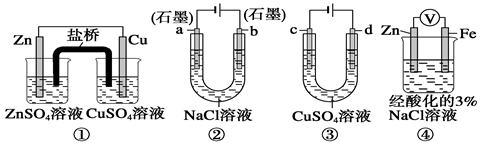
A . 装置①中,盐桥中的K+移向ZnSO4溶液
B . 装置②工作一段时间后,a极附近溶液的pH增大
C . 用装置③精炼铜时,溶液中Cu2+的浓度一定始终不变
D . 装置④中电子由Zn流向Fe,装置中有Fe2+生成
设NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 0.1mol·L-1的Na2CO3溶液中含有CO32-的数目一定小于0.1NA
B . 用惰性电极电解CuSO4溶液时,阳极产生1.12L(标准状况)气体,则电路中通过的电子数为0.2NA
C . 将0.1 molHI完全溶解于1L水中,则溶液中氢原子数为0.1NA
D . 一定条件下,某密闭容器中发生反应:N(g)+3H2(g)  2NH3(g)。该条件下,投入1molN2和3molH2 , 反应达到平衡时,转移的电子数为6NA
2NH3(g)。该条件下,投入1molN2和3molH2 , 反应达到平衡时,转移的电子数为6NA
 2NH3(g)。该条件下,投入1molN2和3molH2 , 反应达到平衡时,转移的电子数为6NA
2NH3(g)。该条件下,投入1molN2和3molH2 , 反应达到平衡时,转移的电子数为6NA
下列说法错误的是( )
A . 钠可用于制备一些贵重金属
B . 铁制容器可用来运送浓硫酸
C . 工业上可采用高温冶炼黄铜矿的方法获得粗铜
D . 电解法不能使非自发反应发生
利用如图所示装置(示意图),当X、Y选用不同材料时,可将电解原理广泛用于工业生产。下列说法中错误的是( )
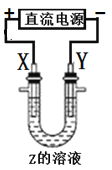
A . 氯碱工业中,Y附近能得到氢氧化钠溶液
B . 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4
C . 电镀工业中,Y是待镀金属,X是镀层金属
D . 外加电流的阴极保护法中,Y是待保护金属
科学家最近设计出了质子膜H2S电池,实现了H2S废气变废为宝,电池结构原理如图,下列相关说法正确的是( )
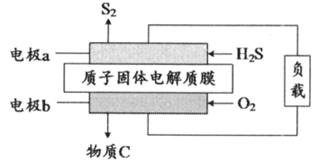
A . 电极a为正极,发生还原反应
B . H+经过固体电解质膜向a电极移动
C . 电极b的反应为:O2+4e-+4H+=2H2O
D . 用该电池进行粗铜的精炼,当电路中转移2 mol e-时,阳极减轻64g
如图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
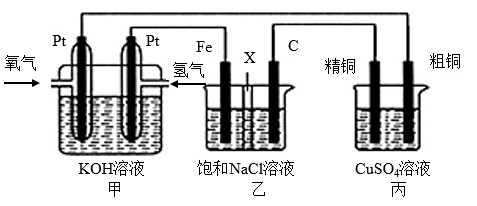
根据要求回答相关问题:
-
(1) 通入氢气的电极为(填“正极”或“负极”),该电极反应式为。
-
(2) 乙装置中石墨电极(C)为(填“阳极”或“阴极”),铁电极的电极反应式为。
-
(3) 反应一段时间后,如何检验乙装置中石墨电极的产物。
-
(4) 如果粗铜中含有锌、银、金等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将。(填“增大”、“减小”或“不变”)。
-
(5) 若在标准状况下,有2.24L氧气参加反应,则乙装置中(NaCl足量)C电极上生成的气体的物质的量为;丙装置中阴极析出铜的质量为。
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A . 0.1 mol H2和0.1 mol I2于密闭容器中充分反应后,其分子总数为0.2NA
B . 1 L0.1 mol·L-1的H3BO3溶液中,含有0.3NA个H+
C . 将53.5 g NH4Cl晶体投入1 L水中,  离子的数目为NA
D . 电解精炼铜时,外电路中每通过2NA个电子,阳极质量减少64 g
离子的数目为NA
D . 电解精炼铜时,外电路中每通过2NA个电子,阳极质量减少64 g
 离子的数目为NA
D . 电解精炼铜时,外电路中每通过2NA个电子,阳极质量减少64 g
离子的数目为NA
D . 电解精炼铜时,外电路中每通过2NA个电子,阳极质量减少64 g
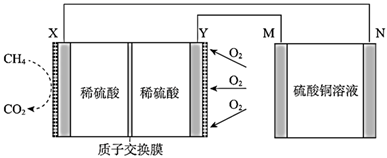
一种甲烷燃料电池的工作原理如图所示。
-
(1) X电极为(填“正极”或“负极”),该电极的电极反应式为。
-
(2) 放电过程中,
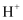 向(填“X极”或“Y极”)移动。
向(填“X极”或“Y极”)移动。
-
(3) 若用该燃料电池进行粗铜精炼,则M极连接的是(填“粗铜”或“精铜”),N极的电极反应式为。
-
(4) 若用该燃料电池进行电镀铜,则N极连接的是(填“镀件”或“精铜”),理论上每消耗
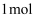 甲烷时,M极变化(增加或减少)的质量为g。
甲烷时,M极变化(增加或减少)的质量为g。
下列叙述错误的是( )
A . 闪锌矿(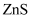 )经
)经 溶液作用后,转化为铜蓝(
溶液作用后,转化为铜蓝(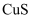 ):
):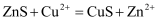 B .
B . 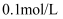 醋酸溶液
醋酸溶液 约为3:
约为3: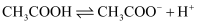 C .
C . 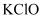 溶液显碱性:
溶液显碱性: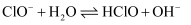 D . 粗铜精炼时,与电源负极相连的是纯铜,阴极反应式为:
D . 粗铜精炼时,与电源负极相连的是纯铜,阴极反应式为: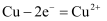
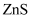 )经
)经 溶液作用后,转化为铜蓝(
溶液作用后,转化为铜蓝(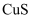 ):
):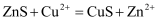 B .
B . 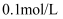 醋酸溶液
醋酸溶液 约为3:
约为3: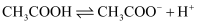 C .
C . 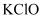 溶液显碱性:
溶液显碱性: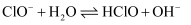 D . 粗铜精炼时,与电源负极相连的是纯铜,阴极反应式为:
D . 粗铜精炼时,与电源负极相连的是纯铜,阴极反应式为: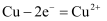
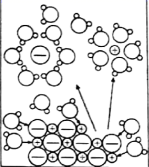
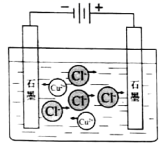
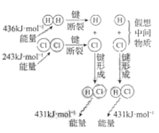
下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)( )
A | B | C | D |
NaCl溶于水 |
电解CuCl2溶液 |
CH3COOH在水中电离 | H2与Cl2反应能量变化 |
NaCl=Na++Cl− | CuCl2=Cu2++2Cl− | CH3COOH | H2(g)+Cl2(g)=2HCl(g) ΔH=−183kJ·mol−1 |
A . A
B . B
C . C
D . D
关于下列各装置图的叙述中,不正确的是( )
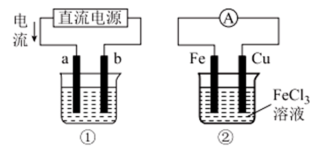
A . 用装置①精炼铜,则a极为粗铜,电解质溶液为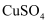 溶液
B . 用装置①进行电镀,镀件接在b极上
C . 装置②的总反应:
溶液
B . 用装置①进行电镀,镀件接在b极上
C . 装置②的总反应: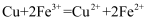 D . 装置②可将化学能转化为电能
D . 装置②可将化学能转化为电能
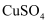 溶液
B . 用装置①进行电镀,镀件接在b极上
C . 装置②的总反应:
溶液
B . 用装置①进行电镀,镀件接在b极上
C . 装置②的总反应: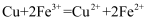 D . 装置②可将化学能转化为电能
D . 装置②可将化学能转化为电能
最近更新
- 我国淡水污染形势严峻,直接影响到人民的生产和生活.江河湖水污染主要来自于农业生产中流失的化肥、城市生活污水中的含磷洗涤剂
- 非结合胆红素(VCB)分子中有羟基,被氧化后(生成羧基)与钙离子结合形成胆红素钙的反应,就是一个沉淀生成的离子反应,从动
- 先化简,再求值:12xy+(3x2-5xy)-2(3xy+2x2),其中,x=2,y=.
- 对一切实数x,不等式x2+a|x|+1≥0恒成立,则实数a的取值范围是( ) A.(-∞,-2] B.[-2,2
- 魏晋南北朝时期,以九品中正制为基础选拔官吏,逐渐形成了“上品无寒门,下品无士族”的局面。其中“品”主要是指( )
- 我国法律规定:公民对于任何国家机关和国家机关工作人员的违法失职行为,有向有关国家机关提出 ( ) A.批评和建议的权利
- 补写出下列名篇名句中的空缺部分。 (1)沧海月明珠有泪, 。 (2)
- 读下列四幅我国不同地区的景观图,回答问题。1.四幅景观与可能所在的省区对应正确的是A.①图—浙江 B.②图—新疆
- 清平乐
- 下列各种现象与所涉及的物理知识说法错误的是 A. 红外线夜视仪——红外线的热效应B. 书桌上的玻璃板“反光”——发生了
- She is the only one of the students who a winner of the
- 下图为正常人体内肝细胞与内环境之间物质交换的示意图,其中①②③④分别表示体液的成分,a、b、c、d、e分别表示物质运输的
- We do eye ________ _____ 10 o’clock at school. A. exe
- 短周期的三种元素X、Y、Z,原子序数依次减小,原子核外电子层数之和是5。X元素原子最外电子层上的电子数是Y和Z两元素原子
- _____ there apost office and a bank near here? A.Are B. Is
- 从4名男生、3名女生中任选3人参加一次公益活动,其中男生、女生均不少于1人的组合种数为 (用数字作答)
- 山东省已有成千上万名青年成功创业。这与前几年大学生回乡创业孤军奋战的状态完全不同,如今大学生回乡创业在多方支持下,道路越
- Progress______ so far very good and we sure that the work w
- 图是1936年《西安文化日报》的报道。其反映的事件是( ) A.北伐战争 B.九一八事变
- 椋鸟喜食枸杞的果实,椋鸟对枸杞是( )。 A.有害的 B.有益的 C.无害、无益的 D.有
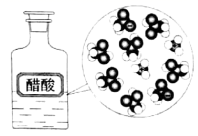
 CH3COO−+H+
CH3COO−+H+


