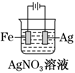
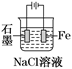
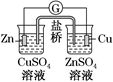
铜的电解精炼 知识点题库
下列有关说法中正确的是( )
A . 自来水厂可用明矾对水进行消毒杀菌
B . 氯碱工业中,NaOH是在阴极室中产生的
C . 电解法精炼铜时,粗铜接电源的负极
D . 实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用玻璃塞
下列关于工业生产说法不正确的是( )
A . 电解精炼铜时,用粗铜做阴极,纯铜做阳极
B . 在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率
C . 在炼铁工业,需要的原料有铁矿石、焦炭、空气、石灰石等
D . 在侯氏制碱工业中,向饱和氯化钠溶液中先通氨气,后通二氧化碳
下列说法中正确的是( )
A . 电解精炼铜时,纯铜作为阳极,粗铜作为阴极
B . 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
C . 氯碱工业中阳离子交换膜的主要作用是:防止阳极产生的氯气和阴极产生的氢气及氢氧化钠反应
D . 工业合成氨通常采用500℃的高温主要是为了提高氮气的转化率
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A . 粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu﹣2e﹣═Cu2+
B . 氢氧燃料电池的负极反应式:O2+2H2O+4e﹣═4OH﹣
C . 用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl﹣﹣2e﹣═Cl2↑
D . 钢铁发生电化学腐蚀的正极反应式:Fe﹣2e﹣═Fe2+
下列描述中,不符合生产实际的是( )
A . 电解法精炼粗铜,用纯铜作阴极
B . 在镀件上电镀锌,用锌作阳极
C . 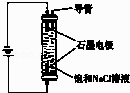 用如图装置生产家用消毒液(NaClO)
D .
用如图装置生产家用消毒液(NaClO)
D . 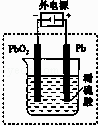 用如图装置为铅蓄电池充电
用如图装置为铅蓄电池充电
 用如图装置生产家用消毒液(NaClO)
D .
用如图装置生产家用消毒液(NaClO)
D .  用如图装置为铅蓄电池充电
用如图装置为铅蓄电池充电
下列说法正确的是( )
A . 工业上电解氯化镁溶液可以制备金属镁
B . 生物炼铜就是利用植物对铜离子的吸收达到富集铜的目的
C . 工业上用廉价的焦炭还原铁矿石得到铁
D . 工业上利用氢气在氯气中燃烧生成氯化氢,再将氯化氢溶于水制得盐酸
下列有关电化学装置完全正确的是( )
| A | B | C | D |
| | | | |
| 铜的精炼 | 铁上镀银 | 防止Fe被腐蚀 | 构成铜锌原电池 |
A . A
B . B
C . C
D . D
下列化学用语书写正确的是( )
A . 次氯酸的电离方程式:HClO=H++ClO-
B . 硫化钠水解的离子方程式:S2-+2H2O  H2S+2OH-
C . 电解精炼铜的阴极反应式:Cu-2e-=Cu2+
D . 碳酸钙的溶解平衡:CaCO3(s)
H2S+2OH-
C . 电解精炼铜的阴极反应式:Cu-2e-=Cu2+
D . 碳酸钙的溶解平衡:CaCO3(s)  Ca2+(aq)+CO32-(aq)
Ca2+(aq)+CO32-(aq)
 H2S+2OH-
C . 电解精炼铜的阴极反应式:Cu-2e-=Cu2+
D . 碳酸钙的溶解平衡:CaCO3(s)
H2S+2OH-
C . 电解精炼铜的阴极反应式:Cu-2e-=Cu2+
D . 碳酸钙的溶解平衡:CaCO3(s)  Ca2+(aq)+CO32-(aq)
Ca2+(aq)+CO32-(aq)
下列说法中正确的是( )
A . 在船体上镶嵌锌块,可以减缓船体被海水腐蚀的速率
B . 粗铜精炼时,电镀液中的c(Cu2+)保持不变
C . 纯银在空气中久置变黑发生的是电化学腐蚀
D . 阴极电保护法是将被保护的金属与外加电源的正极相连
关于下列装置的说法正确的是( )
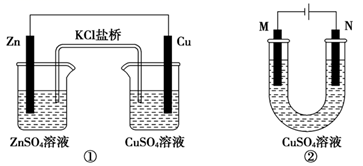
A . 装置①将电能转变为化学能
B . 装置①中盐桥内的 K+移向 CuSO4 溶液
C . 若装置②用于铁棒镀铜,则 N 极为铁棒
D . 若装置②用于电解精炼铜,溶液中的 Cu2+浓度保持不变
下列有关工业生产的叙述正确的是( )
A . 合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B . 从海水中可以得到NaCl,工业冶炼金属钠可以通过电解NaCl饱和溶液获得
C . 电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
D . 电解饱和食盐水制烧碱,采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
如图所示,某学生设计一个甲醚燃料电池并探究氯碱工业原理和粗铜精炼原理,其中乙装置中X为阳离子交换膜。
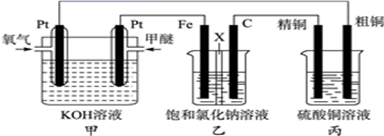
根据要求回答相关问题:(甲醚的化学式:CH3OCH3)
-
(1) 通入氧气的电极为(填“正极”或“负极”),写出负极的电极反应式。
-
(2) 铁电极为(填“阳极”或“阴极”),石墨电极(C)的电极反应式为。
-
(3) 如果粗铜中含有锌、银等杂质,反应一段时间,硫酸铜溶液浓度将 (填“增大”“减小”或“不变”)。
-
(4) 若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为;丙装置中阴极析出铜的质量为。
关于下列各装置图的叙述中,错误的是( )
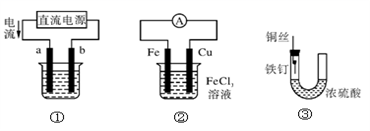
A . 用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B . 用装置①进行电镀,镀件接在b极上
C . 装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+
D . 装置③中的铁钉几乎没被腐蚀
下列关于铜电极的叙述中错误的是( )
A . 锌铜原电池中铜是正极
B . 在镀件上镀铜时可用金属铜作阳极
C . 用电解法精炼粗铜时粗铜作阳极
D . 用电解法精炼粗铜时纯铜作阳极
铜的氧化物及其盐有重要的用途。制泡铜发生如下反应:2Cu2S+3O2=2Cu2O+2SO2 , 2Cu2O+Cu2S=6Cu+SO2↑,将泡铜熔炼后再电解精炼制精铜。关于铜及铜的制备说法正确的是( )
A . 铜元素在元素周期表的d区,基态原子核外电子排布式为[Ar]3d104s1
B . 制泡铜过程中,制取6molCu共转移18mol电子
C . 电解精炼粗铜时,阴极减小的质量等于阳极增加的质量
D . 精炼后的电解液中存在:Cu2+、Zn2+、  、Fe2+、Ag+
、Fe2+、Ag+
 、Fe2+、Ag+
、Fe2+、Ag+
设NA表示阿伏加德罗常数的值。下列说法正确的是( )
A . 14 g聚丙烯中含C-H键总数目为NA
B . 氢氧燃料电池正极消耗22. 4 L(标准状况)气体时,电路中通过的电子数目为2NA
C . 2.3gNa与氧气完全反应,反应中转移的电子数介于0.1NA到0. 2NA之间
D . 电解精炼铜时,若阳极质量减少64 g,则阴极得到电子的数目为2NA
关于下列各装置图的叙述错误的( )
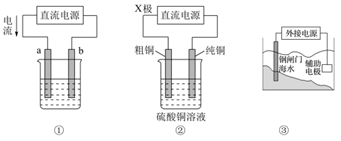
A . 图①装置可实现铁上镀铜,则a极为铜,b极为铁
B . 图②装置可实现粗铜的精炼,则X极为正极
C . 图①装置可用于氯碱工业,则电极总反应式为:2Cl-+2H2O  H2↑+Cl2↑+2OH-
D . 图③装置中钢闸门应与外接电源的负极相连以实现牺牲阳极的阴极保护法
H2↑+Cl2↑+2OH-
D . 图③装置中钢闸门应与外接电源的负极相连以实现牺牲阳极的阴极保护法
 H2↑+Cl2↑+2OH-
D . 图③装置中钢闸门应与外接电源的负极相连以实现牺牲阳极的阴极保护法
H2↑+Cl2↑+2OH-
D . 图③装置中钢闸门应与外接电源的负极相连以实现牺牲阳极的阴极保护法
NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 1L浓度为0.100mol/L的Na2CO3溶液中,阴离子总数为0.100NA
B . 常温下,pH=9的CH3COONa溶液中,水电离出的OH-数为10-5 NA
C . 电解精炼铜时,电路中通过的电子数为NA , 阳极有32g Cu转化为Cu2+
D . 4MnO  +5HCHO+12H+=4Mn2++5CO2↑+11H2O,1mol [4MnO
+5HCHO+12H+=4Mn2++5CO2↑+11H2O,1mol [4MnO  +5HCHO]完全反应转移的电子数为20 NA
+5HCHO]完全反应转移的电子数为20 NA
 +5HCHO+12H+=4Mn2++5CO2↑+11H2O,1mol [4MnO
+5HCHO+12H+=4Mn2++5CO2↑+11H2O,1mol [4MnO  +5HCHO]完全反应转移的电子数为20 NA
+5HCHO]完全反应转移的电子数为20 NA
下列关于电化学的说法正确的是( )
A . 钢板上的铁铆钉处在潮湿的空气中直接发生反应: 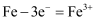 ,发生吸氧腐蚀
B . 电解精炼铜时,阳极为粗铜,阴极为精铜,电解过程中电解质溶液不需要更换
C . 在铁制器皿上镀锌,铁制器皿作阴极,锌片作阳极
D . 二次电池充电时,电池上标有“+”的电极应与外接电源的负极相连
,发生吸氧腐蚀
B . 电解精炼铜时,阳极为粗铜,阴极为精铜,电解过程中电解质溶液不需要更换
C . 在铁制器皿上镀锌,铁制器皿作阴极,锌片作阳极
D . 二次电池充电时,电池上标有“+”的电极应与外接电源的负极相连
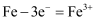 ,发生吸氧腐蚀
B . 电解精炼铜时,阳极为粗铜,阴极为精铜,电解过程中电解质溶液不需要更换
C . 在铁制器皿上镀锌,铁制器皿作阴极,锌片作阳极
D . 二次电池充电时,电池上标有“+”的电极应与外接电源的负极相连
,发生吸氧腐蚀
B . 电解精炼铜时,阳极为粗铜,阴极为精铜,电解过程中电解质溶液不需要更换
C . 在铁制器皿上镀锌,铁制器皿作阴极,锌片作阳极
D . 二次电池充电时,电池上标有“+”的电极应与外接电源的负极相连
辉铜矿(主要成分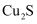 )可以用于制铜,化学反应方程式为
)可以用于制铜,化学反应方程式为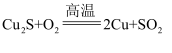 , 制得的粗铜(含
, 制得的粗铜(含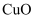 等杂质)可通过电解法进行精炼,下列相关说法正确的是( )
等杂质)可通过电解法进行精炼,下列相关说法正确的是( )
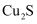 )可以用于制铜,化学反应方程式为
)可以用于制铜,化学反应方程式为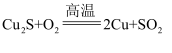 , 制得的粗铜(含
, 制得的粗铜(含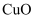 等杂质)可通过电解法进行精炼,下列相关说法正确的是( )
等杂质)可通过电解法进行精炼,下列相关说法正确的是( )
A . 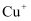 转化为基态
转化为基态 , 得到的电子填充在
, 得到的电子填充在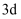 轨道上
B . S元素的电负性大于O元素的电负性
C . 电解精炼铜时,粗铜应与电源的负极相连
D . 如图所示的
轨道上
B . S元素的电负性大于O元素的电负性
C . 电解精炼铜时,粗铜应与电源的负极相连
D . 如图所示的 晶胞中,黑球表示的是
晶胞中,黑球表示的是
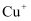 转化为基态
转化为基态 , 得到的电子填充在
, 得到的电子填充在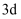 轨道上
B . S元素的电负性大于O元素的电负性
C . 电解精炼铜时,粗铜应与电源的负极相连
D . 如图所示的
轨道上
B . S元素的电负性大于O元素的电负性
C . 电解精炼铜时,粗铜应与电源的负极相连
D . 如图所示的 晶胞中,黑球表示的是
晶胞中,黑球表示的是
最近更新
- It ________ three years sincethey met in Shanghai last time
- 关于古代思想家,下列对应错误的是A.独与天地精神相往来——荀子B.虽千万人,吾往矣—
- 下列叙述正确的是() A.1个DNA分子中含有多个基因 B.DNA复制的过程就是基因表达的过程 C.DNA是蛋白质合成的
- 四川发生大地震后,许多财产受到损失的企业和农户迅速得到保险赔偿。这些企业和农户得到赔偿,是因为 ( )
- 香港和澳门的相同点有A.旅游业不发达B.位于珠江口东侧C.是我国的特别行政区D.人口密度小
- 22.在下面一段文字横线处补写恰当的语句,使之完整连贯,内容贴切,逻辑严密。每处不超过10字。 蔷薇算不上绝色,①
- 依次填入下列句子横线处的词语最恰当的一项是( ) (1)当他们再次相见的时候,曾经的心有灵犀已成过往,多年不通消息使
- 某水电站发电机的输出功率为100 kW,发电机的电压为250V。通过升压变压器升高电压后向远处输电,输电线总电阻为8Ω,
- 下图中,小圆圈有一处为太阳直射点,两条虚线均为晨昏线。读图回答下题。太阳直射点位于( ) A.亚洲
- 上周学校购买了一批水龙头,据商家说其材料是铜质的,实验室的老师组织九年级的一些同学通过实验来验证商家的说法。他们把一个水
- 要防止出现“把我们党和人民群众隔开”的无形之墙。为此,作为执政党应①坚持民主执政,保证人民当家作
- 中华文化历包含鼓励创新的丰富内涵,强调推陈出新、革故鼎新。这里的“推陈出新、革故鼎新”是指( ) A.淘汰所有的传统文
- 在20世纪60年代末,日本发展为资本主义世界第二号经济强国的诸因素中,表述错误的一项是 A.重视发展教育,大
- 镁在空气中燃烧,下列各组数据正确的是 A、镁的质量2 g,氧气质量3 g,氧化镁质量5 g B、镁的质量3 g,氧气质量
- 在10 L密闭容器中,1 mol A和3mol B在一定条件下反应:A(g)+xB(g)2C(g),2 min后反应达到
- 唐代诗人白居易的《大林寺桃花》诗曰:“人间四月芳菲尽,山寺桃花始盛开。”许多人对此提出疑义,北宋科学家沈括曾在四月登庐山
- 发电机的端电压为220 V,输出的电功率为44 kW,输电线电阻为0.2 Ω,求用户得到的电压和电功率各是多少?如果发电
- 明代《闽部疏》载:“凡福之绸丝……富漳之桔,福兴之荔枝,泉水之糖,顺昌之纸,无日不走分水岭及浦城之小无,下吴越如流水。其
- 三只灯泡L1、L 2和L 3的额定电压分别为1.5 V、1.5 V和2.5 V,它们的额定电流都为0.3 A.若将它们连
- 某同学过滤含有泥沙的水,滤液仍然浑浊,其原因可能是A.用玻璃棒引流 B.倒液体时液