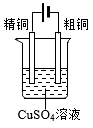
铜的电解精炼 知识点题库
下列说法中正确的是( )
A . 高温下,5.6 g Fe与足量水蒸气完全反应失去电子数为3×6.02×1022
B . FeCl3溶液蒸干、灼烧至恒重,最终剩余固体是FeCl3
C . 电解精炼铜时,阳极泥中常含有金属金、银、锌等
D . 向0.1 mol•L﹣1 氨水中加少量水,pH减小,c(OH﹣)/c(NH3•H2O)增大
利用电解法可将含有Fe、Zn、Ag、Au等杂质的粗铜提纯,下列叙述正确的是( )
A . 电解时以纯铜作阳极
B . 电解时阴极发生氧化反应
C . 粗铜连接电源负极,电极反应是Cu﹣2e﹣=Cu2+
D . 电解结束,电解槽底部会形成含少量Ag、Au等阳极泥
下列电化学有关说法中正确的是( )
A . 将钢闸门与直流电源的正极相连,可降低钢闸门腐蚀速率
B . 镀锌铁制品镀层受损后,铁制品仍不易生锈
C . 粗铜精炼时,电镀液中的c(Cu2+)保持不变
D . 纯银在空气中久置变黑发生的是电化学腐蚀
图Ⅰ的目的是精炼铜,图Ⅱ的目的是保护钢闸门.下列说法不正确的是( )
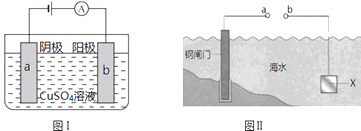
A . 图Ⅰ中a为纯铜
B . 图Ⅰ中SO42﹣向b极移动
C . 图Ⅱ中如果a、b间连接电源,则a连接负极
D . 图Ⅱ中如果a、b间用导线连接,则X可以是铜
电化学是研究化学能与电能相互转化的装置,过程和效率的科学.下列说法不正确的是( )
A . 铅蓄电池放电时,正极的质量会变小
B . 对于某耗氧燃料电池.无论负极通入何种燃料,若转移电子总数相等,则正极消耗等质量的氧气
C . 可以通过适当的电解装置实现反应2Ag+2H+=2Ag++H2↑
D . 电解精炼铜,阳极为粗铜,电镀铜,阳极为纯铜
金属铜是人们最早使用的金属之一,下列关于铜电极的叙述不正确的是( )
A . 铜锌原电池中铜是正极
B . 用电解法精炼粗铜时粗铜做阳极
C . 在镀件上镀铜时可用金属铜做阳极
D . 电解水制H2、O2时铜做阳极
下列说法正确的是( )
A . 向氨水中不断通入CO2 , 随着CO2的增加,  不断减小
B . 在铜的精炼过程中,若转移1mol电子,则阳极一定溶解32gCu
C . 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)的△H>0,△S<0
D . 将下图中的活塞快速推至A处固定,气体颜色先变深、再变浅,但比起始时深
不断减小
B . 在铜的精炼过程中,若转移1mol电子,则阳极一定溶解32gCu
C . 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)的△H>0,△S<0
D . 将下图中的活塞快速推至A处固定,气体颜色先变深、再变浅,但比起始时深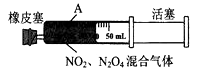
 不断减小
B . 在铜的精炼过程中,若转移1mol电子,则阳极一定溶解32gCu
C . 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)的△H>0,△S<0
D . 将下图中的活塞快速推至A处固定,气体颜色先变深、再变浅,但比起始时深
不断减小
B . 在铜的精炼过程中,若转移1mol电子,则阳极一定溶解32gCu
C . 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)的△H>0,△S<0
D . 将下图中的活塞快速推至A处固定,气体颜色先变深、再变浅,但比起始时深
下列化学用语对事实的表述错误的是( )
A . 硬脂酸与乙醇的酯化反应:C17H35COOH+C2H518OH 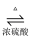 C17H35COOC2H5+H218O
B . 常温时,0.1mol·L-1氨水的pH=11.1:NH3·H2O⇆NH4++OH-
C . 由Na和Cl形成离子键的过程:
C17H35COOC2H5+H218O
B . 常温时,0.1mol·L-1氨水的pH=11.1:NH3·H2O⇆NH4++OH-
C . 由Na和Cl形成离子键的过程: 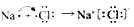 D . 电解精炼铜的阴极反应:Cu2+ +2e=Cu
D . 电解精炼铜的阴极反应:Cu2+ +2e=Cu
 C17H35COOC2H5+H218O
B . 常温时,0.1mol·L-1氨水的pH=11.1:NH3·H2O⇆NH4++OH-
C . 由Na和Cl形成离子键的过程:
C17H35COOC2H5+H218O
B . 常温时,0.1mol·L-1氨水的pH=11.1:NH3·H2O⇆NH4++OH-
C . 由Na和Cl形成离子键的过程:
以硫酸铜溶液作电解质溶液,对含有杂质Fe、Zn、Ag的粗铜进行电解精炼。下列叙述正确的是( )
A . 粗铜与直流电源负极相连
B . 粗铜电解精炼过程中,硫酸铜溶液的浓度不变
C . 电路中每通过3.0l×1023个电子,得到的精铜质量为16 g
D . 杂质Ag以Ag2SO4的形式沉入电解槽形成“阳极泥”
用指定材料做电极来电解一定浓度的溶液甲,然后加入物质乙能使溶液恢复为甲溶液原来的浓度,则合适的组是:( )
阳极 | 阴极 | 溶液甲 | 物质乙 | |
A | Pt | Pt | NaOH | NaOH固体 |
B | Pt | Pt | H2SO4 | H2O |
C | C | Fe | NaCl | 盐酸 |
D | 粗铜 | 精铜 | CuSO4 | Cu(OH)2 |
A . A
B . B
C . C
D . D
下列说法正确的是( )
A . 粗铜电解精炼时,粗铜作阳极,纯铜作阴极
B . 保护钢铁闸门时,可在钢铁闸门水下部分镶嵌铜锭
C . 甲醇燃料电池供电,化学能100%转化为电能
D . 电凝聚法处理废水时,铁作阴极,石墨作阳极
下列关于电解精炼铜的说法中错误的是( )
A . 电解质溶液中要含有Cu2+
B . 粗铜作阳极,精铜作阴极
C . 电解时,阳极发生氧化反应,阴极发生还原反应
D . 粗铜中所含Zn、Fe、Ni等杂质电解后以单质形式沉积于阳极泥中
工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)制取铜的操作流程如下:
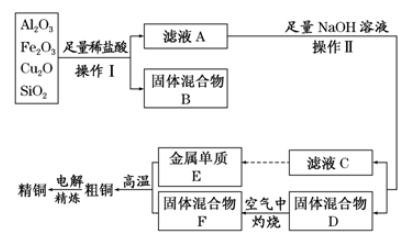
已知:Cu2O+2H+=Cu+Cu2++H2O
-
(1) 实验操作Ⅰ的名称为;在空气中灼烧固体混合物D时,用到多种硅酸盐质的仪器,除玻璃棒、酒精灯、泥三角外,还有(填仪器名称)。
-
(2) 滤液A中铁元素的存在形式为(填离子符号),生成该离子的离子方程式为,检验滤液A中存在该离子的试剂为(填试剂名称)。
-
(3) 金属E与固体F发生的某一反应可用于焊接钢轨,该反应的化学方程式为
-
(4) 常温下,等pH的NaAlO2和NaOH两份溶液中,由水电离出的c(OH-)前者为后者的108倍,则两种溶液的pH=。
-
(5) 利用电解法进行粗铜精炼时,下列叙述正确是(填代号)。
a 电能全部转化为化学能
b 粗铜接电源正极,发生氧化反应
c 精铜作阴极,电解后电解液中Cu2+浓度减小
d 粗铜精炼时通过的电量与阴极析出铜的量无确定关系
下列说法正确的是( )
A . 电解精炼铜时,若转移2NA个电子,则阳极减少的质量为64g
B . 合成氨生产中将NH3液化分离,可加快正反应速率,提高H2的转化率
C . 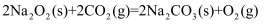 在常温下能自发进行,则该反应的△H>0
D . 常温下,
在常温下能自发进行,则该反应的△H>0
D . 常温下,  。欲使溶液中
。欲使溶液中 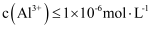 ,需调节溶液的
,需调节溶液的 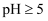
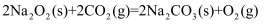 在常温下能自发进行,则该反应的△H>0
D . 常温下,
在常温下能自发进行,则该反应的△H>0
D . 常温下,  。欲使溶液中
。欲使溶液中 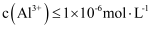 ,需调节溶液的
,需调节溶液的 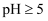
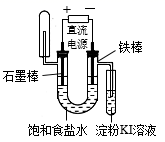
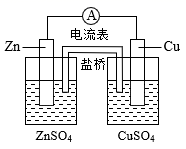
下列有关电化学的装置示意图正确的是 ( )
A . 铜锌原电池 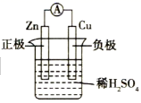 B . 铜锌原电池
B . 铜锌原电池 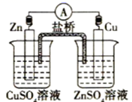 C . 精炼铜
C . 精炼铜 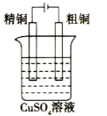 D . 电解饱和食盐水
D . 电解饱和食盐水 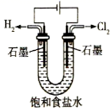
 B . 铜锌原电池
B . 铜锌原电池  C . 精炼铜
C . 精炼铜  D . 电解饱和食盐水
D . 电解饱和食盐水 
下列有关化工生产的说法中错误的是( )
① 可以电解饱和食盐水来制取金属钠
② 可以将钠加入MgCl2饱和溶液中制取镁
③ 用电解法冶炼铝时,原料是氯化铝
④ 冶炼金属时,必须加入一种物质作为还原剂
⑤ 在金属铁表面镀上一层铜,让铁作电解池的阴极,溶液中铜离子浓度可保持不变
⑥ 电解精炼铜时,若硫酸铜溶液为电解液,则粗铜作阳极,溶液中铜离子浓度始终保持不变
A . ② ③
B . ① ④ ⑤
C . ① ② ③ ④ ⑥
D . ① ② ③ ④ ⑤ ⑥
碲被誉为“现代工业、国防与尖端技术的维生素”,工业上常用铜阳极泥 ( 主要成分是 Cu2Te, 含 Ag 、 Au 等杂质 ) 为原料提取碲并回收金属其工艺流程如下:
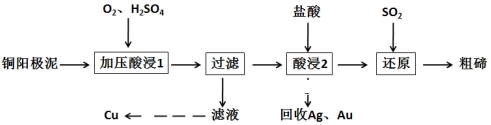
已知: TeO2是两性氧化物,微溶于水,易溶于较浓的强酸和强碱。回答下列问题:
-
(1) 写出“加压酸浸 1”过程中 Cu2Te 发生反应的化学方程式。
-
(2) “酸浸 2”时温度过高会使碲的浸出率降低,原因为 。要从 Ag 和 Au 中分离出 Au ,可以向回收的 Ag 和 Au 中加入的试剂是 。
-
(3) 写出“还原”反应中发生的离子方程式 。
-
(4) 工业上另一种提取碲的方法是将铜阳极泥在空气中焙烧 , 使碲转化成 TeO2 , 再加NaOH 碱浸,以石墨为电极电解溶液获得 Te。 电解过程中阴极的电极反应式为 。
-
(5) 25 ℃时 , 向 1mol/L 的 Na2TeO3溶液中滴加盐酸 ,当溶液 pH 值约为 6 时 ,此时溶液中 c(
 ):c(
):c( 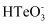 ) = ( 已知: H2TeO3:Ka1=1.0×10−3 , Ka2=2.0×10−8)
) = ( 已知: H2TeO3:Ka1=1.0×10−3 , Ka2=2.0×10−8)
粗铜中含有锌、铁、金、银等杂质,通过电解法将其精炼,下列说法错误的是( )
A . 粗铜与电源的正极相连发生氧化反应:Cu-2e-= Cu2+
B . 精铜作为阴极材料,不参与电极反应,电解过程中逐渐变粗
C . 用CuSO4作电解质溶液,电解过程中CuSO4溶液浓度略减小
D . 锌、铁、金、银等杂质沉积在阳极周围,成为阳极泥
铜是人类最早发现和使用的金属之一,铜及其合金的用途广泛。粗铜中含有少量铁、锌、银、金等杂质,工业上可用电解法精炼粗铜制得纯铜,下列说法正确的是( )
A . 精铜做阳极,粗铜做阴极
B . 可用AgNO3溶液做电解质溶液
C . 电解时,阴极反应为Cu – 2e- = Cu2+
D . 电解后,可用阳极泥来提炼金、银
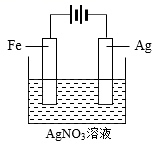
下列实验装置能达到实验目的的是( )
| A | B | C | D |
| | | | |
| 电解饱和食盐水并检验气体 | 构成铜锌原电池 | 电解精炼铜 | 铁片镀银 |
A . A
B . B
C . C
D . D
最近更新
- 用数学归纳法证明(1×22-2×32)+(3×42-4×52)+…+[(2n-1)(2n)2-2n(2n+1)2]=-n
- (2011浙江衢州,21,8分)某花圃用花盆培育某种花苗,经过实验发现每盆的盈利与每盆的株数构成一定的关系.每盆植入3株
- 若2m+4n<,则点(m,n)必在 ( )A.直线x+y=l的左上方
- 某溶液中存在Mg2+、Ag+、Ba2+三种金属离子,现用NaOH、Na2CO3、NaCl三种溶液使它们分别沉淀并分离出来
- 如下图所示,从“镰刀斧锤星旗”到“白蓝红三色旗”的变更宣告“苏维埃社会主义共和国联盟停止存在”。这一事件对于某班同学的一
- 11.朱熹说:“本朝鉴五代藩镇之弊,遂尽夺藩镇之权。兵也收了,财也收了,赏罚刑政,一切收了。”这段话说明宋朝 A.中央集
- You can come here to ask me _____ if you have any questions
- 下列围绕北冰洋的大洲,正确的一组是: A.亚洲、欧洲、北美洲 B.北美洲、亚洲、非洲 C.大洋洲
- 甲图中游标卡尺的读数是 mm。乙图中螺旋测微器的读数是 mm。
- 为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是 物质试剂分离方法①硝酸钾(氯化钠)蒸馏水降温结晶②
- 制成物品所使用的材料,属于无机非金属材料的是( )。
- 在△ABC中,三边长为AB=7,BC=5,AC=6,则·= .
- 《十二铜表法》在一定程度上维护了平民的利益,因为它 A、使案件的审理有法可依 B、是罗马历史上第一部成文法 C、明确规定
- 细胞内生物膜为细胞生命活动提供了广阔场所,不同细胞器增大膜面积的方式可能不同。下列有关细胞器增大膜面积方式的叙述中,错误
- 如图(甲)从阴极发射出来的电子束,在阴级和阳极间的高电压作用下,轰击到长条形的荧光屏上激发出荧光,可以显示出电子束运动的
- When the group discussion isnearing its end, make sure toit
- 下列句子中填入的关联词语最恰当的一项是( ) 踏着如雪的字,一路寻去, 风寒扑面, 想着
- 下列关于生物学实验的叙述中,正确的是A.用32P标记T2噬菌体侵染未标记的大肠杆菌,离心后上清液放射性很高 B.利用DN
- 电磁波包含了g射线、红外线、紫外线、无线电波等,按波长由长到短的排列顺序是( )A.无线电波、红外线、紫外线、g射线
- 下列属于吸热反应是 A.金属钠与水的反应 B.盐酸与氢氧化钠的反应 C.铝与氧化铁的铝热反应 D