第3节 氮的循环 知识点题库
已知:甲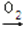 乙
乙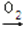 丙
丙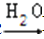 丁,其中丁为强酸,则甲不可能为 ( )
丁,其中丁为强酸,则甲不可能为 ( )
A . N2
B . C
C . S
D . NH3
关于NH3用途的叙述,正确的是( )
A . 制造氮肥
B . 制造玻璃
C . 做漂白剂
D . 做干燥剂
施用碳酸氢铵、氯化铵等铵态氮肥能够促进农作物生长,但是铵态氮肥不能与碱性肥料如草木灰混合使用,其原因是铵态氮肥( )
A . 易溶于水
B . 能与碱反应
C . 受热易分解
D . 在水中易发生电离
关于磷的下列叙述中,正确的是( )
A . 红磷没有毒性而白磷剧毒
B . 白磷在空气中加热到260℃可转变为红磷
C . 白磷可用于制造安全火柴
D . 少量白磷应保存在水中
含氮的物质丰富多彩
-
(1) 从分子结构上看,氮与碳有很多对应的物质(如甲烷跟氨气对应),请找出下列含碳化合物对应的含氮物质:
-
(2) 化学式为N4的分子结构等同于白磷,N4中每个原子满足最外层8e﹣结构.则1个N4中含有 对共用电子对.
-
(3) 某化合物的焰色反应为黄色,根据质谱分析它的相对分子质量为39且与水反应能生成氨气.则该化合物中存在的化学键类型为 ,其与过量盐酸反应的化学方程式为
-
(4) 某化合物A是一种易溶于水的不含结晶水的盐,溶于水后可完全电离出三种中学化学常见离子,其中有两种是10电子的阳离子.用A进行如下实验:取2.370gA溶于蒸馏水配成溶液;向该溶液中逐滴加入一定量的氢氧化钠溶液,过程中先观察到产生白色沉淀B,后产生能使湿润红色石蕊试纸变蓝的气体C,气体不再产生时沉淀开始溶解,当沉淀恰好完全溶解时共用去氢氧化钠的物质的量为0.050mol.回答下列问题:
①化合物A的化学式为 ;请设计实验方案验证A中阴离子
②请写出足量气体C与氯气发生氧化还原反应的化学方程式
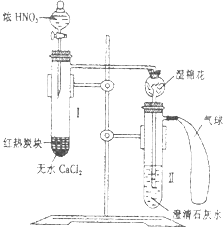
某校为了改进碳与HNO3反应的实验,设计了如图所示的装置:先预热盛有无水CaCl2的试管I,然后投入几小块红热的炭块,再缓缓地向炭块上滴加浓HNO3 , 反应即可连续进行.
-
(1) 由于浓HNO3易挥发,应怎样操作才能使分液漏斗中HNO3顺利滴下?.
-
(2) 写出试管I中的化学方程式:.
-
(3) 试管Ⅱ上方的长颈漏斗中放置一团湿棉花.其作用是.
-
(4) 试管Ⅱ中的现象:.
下列情况会有氢气生成的是( )
A . 铝放入冷的浓硫酸中
B . 铜放入热的浓硫酸中
C . 铝放入冷的稀酸中
D . 锌放入冷的稀硝酸中
硫和氮氧化物是形成酸雨、雾霾等环境污染的罪魁祸首,采用合适的措施消除其污染是保护环境的重要举措.
-
(1) 研究发现利用NH3可消除硝酸尾气中的NO污染.NH3与NO的物质的量之比分别为1﹕3、3﹕1、4﹕1时,NO脱除率随温度变化的曲线如图所示:
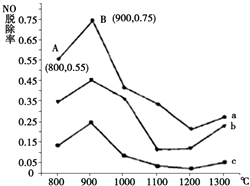
①用化学反应方程式表示NH3消除NO的反应原理(不用注明反应条件).
②曲线b 对应NH3与NO的物质的量之比是.
③曲线a中,NO的起始浓度为6×10﹣4mg/m3 , 从A点到B点经过0.8s,该时间段内NO的脱除速率为 mg/(m3•s).
-
(2) NO、NO2混合气体能被NaOH溶液吸收生成NaNO2和NaNO3 , 若吸收的溶液中NO2﹣的浓度为ag•L﹣1 , 要使1m3该溶液中的NO2﹣完全转化为NH4NO3 , 至少需通入标准状况下的O2L.(用含a的代数式表示,计算结果保留整数)
-
(3) SO2被少许NaOH溶液吸收生成能使pH试纸变红的NaHSO3溶液,工业上可电解NaHSO3得到重要化工产品Na2S2O4 .
①NaHSO3溶液中离子浓度大小为.
②写出生成S2O42﹣的电极反应式.
中学化学中很多“规律”都有其适用范围,下列根据有关“规律”推出的结论合理的是( )
A . Na2O、Na2O2组成元素相同,推出与水反应产物也完全相同
B . SO2和湿润的Cl2都有漂白性,推出二者混合后漂白性更强
C . H2CO3的酸性比HClO强,推出CO2通入NaClO溶液中能生成HClO
D . 根据常温下铜与浓硝酸可以制取NO2 , 推出常温下铁与浓硝酸也可以制取NO2
引起环境污染的原因错误的是( )
A . 重金属、农药和难分解有机物、含N、P的污水等会造成水体污染
B . 装饰材料中的甲醛、芳香烃及氡等会造成居室污染
C . SO2、NO2和CO2都会导致酸雨的形成
D . CO2的大量排放会造成温室效应的加剧
能使湿润的蓝色石蕊试纸最终褪色的气体是( )
A . SO2
B . Cl2
C . NH3
D . HCl
把铜粉和过量的铁粉加入到热的浓硝酸中,充分反应后溶液中大量存在的金属阳离子是( )
A . 只有Fe2+
B . 只有Fe3+
C . 有Fe2+和Cu2+
D . 有Fe3+和Cu2+
向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
| 操作 | 现象 | 结论 | |
| A | 滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B | 滴加氯水和CCl4 , 振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+、无K+ |
| D | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
A . A
B . B
C . C
D . D
铜和镁的合金4.6g完全溶于浓硝酸,若反应后硝酸被还原只产生标准状况下4480mLNO2气体和336mL的N2O4气体,在反应后的溶液中,加入1mol/L的NaOH溶液,当金属离子全部沉淀时,生成沉淀的质量为8.51g。下列说法错误的是( )
A . 该合金中铜与镁的物质的量之比是2:3
B . 得到8.51g沉淀时,加入NaOH溶液的体积为230mL
C . NO2和N2O4的混合气体中NO2的体积分数是93%
D . 该反应消耗HNO3的物质的量为0.23mol
某课外实验小组设计的下列实验合理的是( )
A . 完成喷泉实验 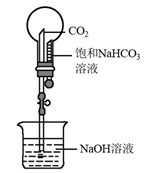 B . 比较
B . 比较  和
和  的热稳定性
的热稳定性 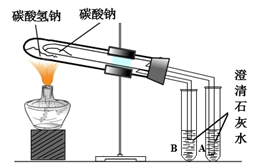 C . 除去
C . 除去  中的HCl气体
中的HCl气体 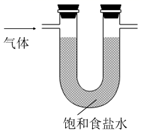 D . 验证氨气易溶于水
D . 验证氨气易溶于水 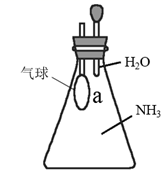
 B . 比较
B . 比较  和
和  的热稳定性
的热稳定性  C . 除去
C . 除去  中的HCl气体
中的HCl气体  D . 验证氨气易溶于水
D . 验证氨气易溶于水 
下图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去)。已知:E为红棕色固体,K为浅绿色溶液;反应①②是化工生产中的重要反应;B、C、D、H是单质;B、C、D、F、G、H常温下是气态;F和H的水溶液均具有漂白作用,且F是形成酸雨的主要物质之一;N是一种常见的氮肥;化合物G为极易溶于水且易液化。
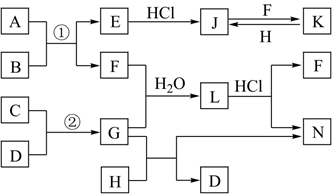
-
(1) 化合物A中含有的短周期元素是(写元素符号),E的化学式。
-
(2) 如何检验化合物N中的阳离子。
-
(3) 写出J与F反应的离子方程式:,G与H反应的化学方程式:。
-
(4) 等物质的量F和H的混合气体通入品红溶液中的现象为,原因是(用化学反应方程式表示)。
-
(5) 实验室制取G的化学方程式
某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。(制取氨气的反应原理:2NH4Cl+Ca(OH)2  CaCl2+2NH3↑+2H2O)
CaCl2+2NH3↑+2H2O)
 CaCl2+2NH3↑+2H2O)
CaCl2+2NH3↑+2H2O) 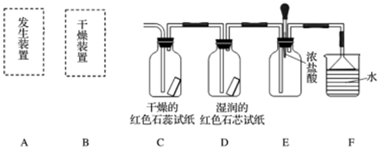
-
(1) A发生装置N元素的化合价是,该反应是否是氧化还原反应填(“是”或“否”)。甲、乙、丙三位同学分别用如图所示三套实验装置及化学药品来制取氨气
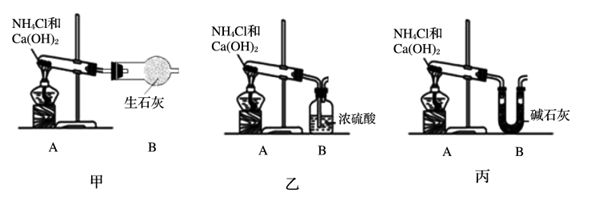
其中有一位同学没有完成制取并探究氨气性质实验(如果他们的实验操作都正确),你认为没有收集到氨气的同学是填(“甲”、“乙”或“丙”),收集不到氨气的主要原因是(用化学方程式表示)。若用如图装置代替上述A装置来完成实验,装置中加入试剂合理的是。
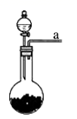
a.浓氨水
b.浓氨水与CaO
c.NH4Cl与Ca(OH)2
-
(2) 用5.35 g NH4Cl固体与足量Ca(OH)2反应,最多可制得标准状况下氨气的体积为L。(NH4Cl的摩尔质量为53.5 g/mol)
-
(3) 气体通过C、D装置时,试纸颜色会发生变化的是D,原因是。
-
(4) 当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是。
-
(5) 若收集一集气瓶氨气,检验氨气是否收集满的方法是。
-
(6) 某同学用如图所示装置进行氨气的性质实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有性质填序号。
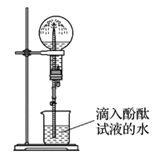
a.还原性
b.极易溶于水
c.与水反应生成碱性物质
-
(7) 氨气的用途很广。如可用氨气处理二氧化氮:8NH3+6NO2=7N2+12H2O,该反应中氨气体现(填“氧化性”或“还原性”)。
下列叙述中,错误的是( )
A . SO2有毒,不能用作食品添加剂
B . 工业合成氨属于人工固氮
C . 酸雨是pH小于5.6的雨水
D . 氧化铝陶瓷是一种无机非金属材料
下列关于物质保存的解释,反应方程式不正确的是( )
A .  溶液中放入铁粉:
溶液中放入铁粉: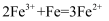 B . 浓硝酸保存于棕色试剂瓶:
B . 浓硝酸保存于棕色试剂瓶: C . 氮肥
C . 氮肥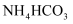 保存于阴凉处:
保存于阴凉处: D . 金属钠保存于煤油中:
D . 金属钠保存于煤油中:
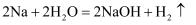
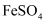 溶液中放入铁粉:
溶液中放入铁粉: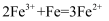 B . 浓硝酸保存于棕色试剂瓶:
B . 浓硝酸保存于棕色试剂瓶: C . 氮肥
C . 氮肥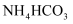 保存于阴凉处:
保存于阴凉处: D . 金属钠保存于煤油中:
D . 金属钠保存于煤油中:
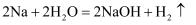
化学与生产、生活密切相关。下列与化学相关的说法合理的是( )
A . 分子筛、青花瓷、黏土、玛瑙、硅石的主要成分都是硅酸盐
B . 碳氢化合物与氮氧化物经紫外线照射发生反应形成的有毒烟雾,称为光化学烟雾
C . 硅酸钠俗称水玻璃,可用作木材防火剂
D . 二氧化硫有毒,严禁将其添加到任何食品和饮料中
最近更新
- 列宁说:“我们原来打算直接用无产阶级国家的法令,在一个小农国家里按共产主义原则来调整国家的生产和产品分配。现实生活说明我
- 反比例函数 (k是常数,k≠0)的图象经过点(1,4),那么这个函数图象所在的每个象限内,y的值随x值的增大而
- 依次填入下列各句横线上的词语,最恰当的一组是() ① 新式标点符号指的是,萌芽于清末,诞生于“五四”,_____到现在的
- 计算=
- 已知,则的值是______________.
- 简答题(共2题,每小题3分,共6分)(1)根据生活经验,对代数式作出解释.(2) 两个有理数的和是负数,那么这两个数一定
- 用50g 98%的浓H2SO4 配制成20%的稀H2SO4 ,需加水的质量为( ) A. 145g B
- 165年前,有一本在当时并不起眼的小册子出版了,它第一次较为完整系统地阐述了马克思主义的基本原理,这本小册子是 A
- —Why ! Where's my passport? Maybe I left it on the plane.
- z∈C,若|z|-=2-4i,则的值是
- 学校里种植了品种繁多的月季花,某兴趣小组想让一株月季开出不同色彩的花,应该采用的技术是 A.人工授粉 B.扦插
- 第四部分 写作技能 (共两节,满分 20 分) 四、双向翻译 (共 5 小题;每小题 2 分,满分 10 分) 请根据上
- 如图为某二倍体生物的三个处于不同分裂时期的细胞示意图。下列有关叙述中,正确的是()A.甲、乙、丙三个细胞中的着丝点均已分
- 已知一组数据的平均数是4,中位数是,,从这组数据中任取一数,取到数字4的概率为,那么这组数据的方差为( ) A.
- 下列实验现象描述不正确的是( )A.在空气中加热铝,失去金属光泽,表面变暗B.木炭在氧气中燃烧,发出白光,生成黑色固
- 对于函数与常数,若恒成立,则称为函数的一个“P数对”;若恒成立,则称为函数的一个“类P数对”.设函数的定义域为,且. (
- 下图为A、B两个国家的人口年龄构成,其中X、Y、Z分别表示某国0~14岁、15~64岁、65岁及以上三个年龄段人数所占总
- In terms of______ one-third of the world’s bears, winter sl
- 某小组同学分别测出了甲、乙电动小车作直线运动的路程和时间,并依据数据作出了相应的路程—时间图像,如图16(a)、(b)所
- 抛物线上一点M到焦点的距离为1,则点M的纵坐标是( )A. B.



