第3节 氮的循环 知识点题库
 4NO+6H2O
4NO+6H2O
-
(1) 我国化工专家侯德榜做出的突出贡献是
A.海水淡化 B.联合制碱 C.合成材料 D.金属冶炼
-
(2) 关于合成氨工业的说法不正确的是
A.常用铁触媒提高反应速率 B.原料气中的氮气来源于空气
C.通过冷凝把氨从混合气中分离出来 D.降低压强有利于氨的合成
-
(3) 下列有关工业生产的叙述中,不正确的是
A.高炉炼铁时用焦炭作氧化剂 B.添加必要的元素可提高钢材的性能
C.催化裂化可提高汽油的产量 D.电解氧化铝时用冰晶石降低其熔点
-
(4) 工业上用电解法冶炼铝时,析出铝的电极是
A.正极 B.负极 C.阴极 D.阳极.
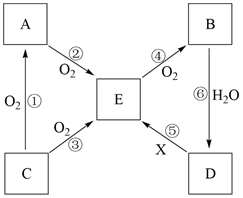
物质编号 | 物质转化关系 | a | b | c | d |
① |
| NO | NO2 | N2 | HNO3 |
② | Na2O | Na2O2 | Na | NaOH | |
③ | FeCl2 | FeCl3 | Fe | CuCl2 | |
④ | Al2O3 | NaAlO2 | Al | Al(OH)3 |
-
(1) Ⅰ.模拟制备碱式氯化铜。向
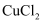 溶液中通入
溶液中通入  和
和  ,调节pH至5.0~5.5,控制反应温度于70~80℃,实验装置如图所示(部分夹持装置已省略)。
,调节pH至5.0~5.5,控制反应温度于70~80℃,实验装置如图所示(部分夹持装置已省略)。 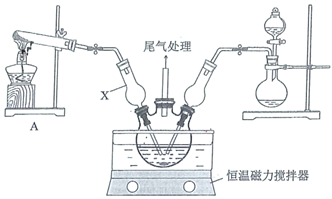
仪器X的名称是,其主要作用有导气、。
-
(2) 实验室利用装置A制
 ,发生反应的化学方程式为。
,发生反应的化学方程式为。
-
(3) 反应过程中,在三颈烧瓶内除观察到溶液蓝绿色褪去,还可能观察到的现象是、、。
-
(4) 若体系
 过高会导致碱式氯化铜的产量(填“偏高”、“偏低”或“无影响”)。
过高会导致碱式氯化铜的产量(填“偏高”、“偏低”或“无影响”)。
-
(5) 反应结束后,将三颈瓶中的混合物过滤,从滤液中还可以获得的副产品是(填化学式),经提纯得产品无水碱式氯化铜。
-
(6) Ⅱ.无水碱式氯化铜组成的测定。称取产品
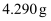 ,加硝酸溶解,并加水定容至200mL,得到待测液。
,加硝酸溶解,并加水定容至200mL,得到待测液。 铜的测定:取20.00mL测液,经测定,
 浓为
浓为 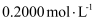 。则称取的样品中
。则称取的样品中  mol。
mol。 -
(7) 采用沉淀滴定法测定氯:用
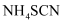 标准溶液滴定过量的
标准溶液滴定过量的 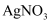 ,实验如图:
,实验如图: 
①滴定时,应选用下列哪种物质作为指示剂(填标号)。
A.
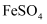 B.
B. 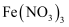 C.
C. 
②重复实验操作三次,消耗
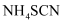 溶液的体积平均为10.00mL。则称取的样品中
溶液的体积平均为10.00mL。则称取的样品中 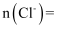 mol。
mol。 -
(8) 根据上述实验结果可推知无水碱式氯化铜的化学式为。
| 选项 | 操作 | 现象 | 结论 |
| A | 向NaAlO2溶液中滴加NaHCO3溶液 | 产生白色沉淀 | AlO |
| B | 蘸有浓氨水的玻璃棒靠近X | 有白烟产生 | X一定是浓盐酸 |
| C | 向某溶液中滴加几滴FeCl3溶液 | 溶液变红 | 溶液中一定含有KSCN |
| D | 用玻璃棒蘸取未知溶液进行焰色反应 | 火焰为黄色 | 说明一定含有钠元素 |
|
选项 |
实验内容 |
实验目的 |
|
A |
常温下用洁净的玻璃棒蘸取次氯酸钠溶液,滴在pH 试纸上,测定次氯酸钠溶液pH 值 |
验证次氯酸是弱酸 |
|
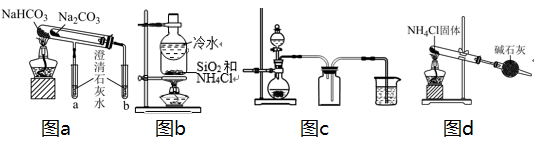
B |
加热 NaHCO3和 NH4Cl固体的混合物 |
除去混合物中的 NH4Cl |
|
C |
将Fe(NO3)2溶于适量硝酸中,然后加水稀释 |
配制一定浓度的Fe(NO3)2溶液 |
|
D |
向二氧化硫的水溶液中滴入几滴石蕊试液 |
检验二氧化硫水溶液具有酸性 |
|
选项 |
陈述Ⅰ |
陈述Ⅱ |
|
A |
|
|
|
B |
|
充满 |
|
C |
Al2O3的熔点很高 |
加入冰晶石可降低其熔点 |
|
D |
常温下,铁与浓硝酸发生钝化 |
常温下,铁与浓硝酸不反应 |
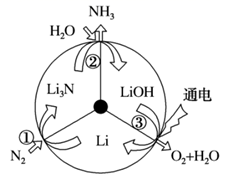
 发生了氧化反应
B . 反应①和②均属于“氮的固定”
C . 反应③为
发生了氧化反应
B . 反应①和②均属于“氮的固定”
C . 反应③为 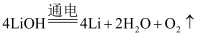 D . 三步循环的总结果为
D . 三步循环的总结果为 
- It will you about thirteen hours to fly to England f
- 某同学在做“测定匀变速直线运动的加速度”实验时打出的纸带如图所示,每两点之间还有四点没有画出来,图中上面的数字为相邻两点
- 在化学反应前后肯定没有变化的是 ( ) ①
- How hard we have all prayed(祈祷) to grow up quickly, and look
- Soon Cathy ______up with me, then we were neck and neck.
- 把各种藻类归为一大类,其原因是: A 它们是真正的单元发生的一个分类上的类群 B 它们是多元发生的,但表现明显的化学
- 图反映了国民政府统治时期某一经济状况,对图中信息解读正确的是( )A、抗战胜利后政府获得大量经济赔偿 B、国民经济建设
- 根据化学方程式书写原则判断,下列错误的是() A.Cu+2HCl═CuCl2+H2 B.Na2CO3+CaCl2═CaC
- I thought you _____ like something to read, so I have brough
- 法布尔在野外的自然状态下,实地观察研究昆虫行为的方法是: ( ) A、实验法 B、观察法
- Smith gave the books to all the students except _____ who ha
- Mr. Smith is well known in Washington because of his many so
- 右图是某生态系统的食物网示意图,甲一庚代表不同的生物.箭头表示能量流动的方向和食物联系。下列叙述正确的是 (
- (2009·广东基础训练题〈二〉)“没有无权利的义务,也没有无义务的权利。”这句话主要说明 ( )
- 如图,抛物线交轴于A、B两点(A点在B点左侧),交轴于点C,已知B(8,0),,△ABC的面积为8.1.求抛物线的解析式
- (1)将3根离体神经纤维(枪乌贼的巨轴突)分别放置于盛有海水(A)、等渗KCI溶液(B)、等渗葡萄糖溶液(C)3个培养
- 总书记在纪念改革开放30周年大会上指出,只要我们不动摇、不懈怠、不折腾,就一定能实现我们的宏伟蓝图和奋斗目标。“不动摇、
- 人类生存需要清洁的空气.下列情况不会造成环境污染的是() A.燃放烟花 B.汽车尾气 C.煤炭燃烧 D.光合作用
- 根据下面一段文字,概括出“3G手机”的主要特点。 (不超过15个字)(4分)3G是英文3rdGaneration的缩写
- .— Have you got your result of the final? — Not yet.I was to
 结合H+的能力比CO
结合H+的能力比CO  强
强 有漂白性
有漂白性


