第3节 氮的循环 知识点题库
(2)写出实验室制取氨气的化学方程式: ,实验室可以用 .
(3)NO2与水反应的化学方程式为 ,该反应中氧化剂与还原剂的物质的量之比为 .
(4)氢氟酸应存放在 中,因为 (请用化学方程式表示原因)
-
(1) 氮分子的电子式为 ,通常情况下氮气化学性质比较稳定的原因是
-
(2) 氮气在一定条件下与镁反应生成氮化镁(Mg3N2),氮化镁与水反应生成两种碱,其反应的化学方程为
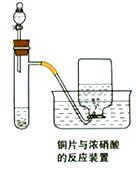
-
(1) 写出试管内发生反应的化学方程式;
-
(2) 描述在实验过程中观察到的颜色变化:
试管内液体呈色;试管内液体上方气体呈色;集气瓶内收集到的气体呈色.
-
(3) 在反应一段时间后,从分液漏斗处向试管内加入蒸馏水,请描述加水后试管内和集气瓶内颜色的变化情况:试管内液体呈色;试管内液体上方气体呈色.
-
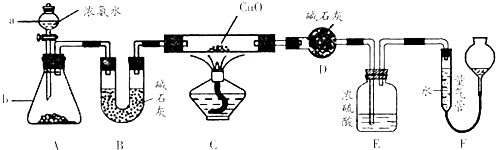
(1) 仪器a的名称为;仪器b中可选择的试剂为.
-
(2) 实验室中,利用装置A,还可制取的无色气体是 (填字母).A . Cl2 B . O2 C . CO2 D . NO2
-
(3) 实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有性,写出相应的化学方程式
-
(4) E装置中浓硫酸的作用.
-
(5) 读取气体体积前,应对装置F进行的操作:
-
(6) 实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为(用含m、n字母的代数式表示)
-
(1) 甲同学欲探究铜与稀硝酸反应产生的气体主要是NO,设计装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是含有一半空气的注射器。
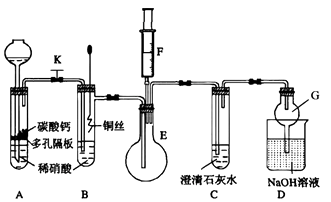
请回答有关问题:
①装置A中进行反应时打开止水夹K,当装置C中时,关闭止水夹K,试分析这样操作的目的是,A中反应的离子方程式为。
②在完成①中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是,B中反应的离子方程式为。
③为进一步证明产物是NO,将注射器F中的空气推入E中,看到的现象是。
④装置G的作用是。
-
(2) 同学们发现铜与稀、浓硝酸反应所得溶液的颜色不同,并记录如下:
将1 g细铜丝放入盛有10 mL的1 mol·L-1 HNO3溶液的试管中加热
铜丝表面有无色气体逸出,溶液变为天蓝色
将1 g细铜丝放入盛有10 mL的14 mol·L-1HNO3溶液的试管中
产生大量红棕色气体,溶液变为绿色,绿色由深到浅,未见到蓝色
有同学认为是铜与浓硝酸反应的溶液中溶解了生成的气体,也有同学认为是溶液中剩余硝酸浓度较大所致,同学们分别设计了以下4个实验来判断该看法是否正确,以下方案中可行的是(选填序号字母)。
a. 向上述绿色溶液中通入氮气,观察颜色变化
b. 加水稀释上述绿色溶液,观察颜色变化
c. 向饱和的硝酸铜溶液中不断滴加14 mol·L-1HNO3溶液
d. 向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
A ![]() B
B ![]() C
C ![]() D
D
-
(1) 若A为H2S,D的水溶液能使湿润的蓝色石蕊试纸变红,B为刺激性气味气体,写出B→C转化的化学反应方程式:.
-
(2) 若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝色石蕊试纸变红:A的化学式为,实验室制备气体A的化学反应方程式A→B转化的化学方程式为.
-
(3) 若A为活泼金属元素的单质,D为强碱,焰色反应显黄色,则B是(填化学式),C可作为呼吸面具的填充剂,C与水发生反应的离子方程式为.
-
(1) 氮在元素周期表的位置为,其非金属性比磷(填“强”或“弱”)。氮气的化学性质很稳定,原因是。
-
(2) 1909年,德国科学家哈伯利用氮气和氢气在500~600℃、18.5~20.0
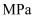 和锇为催化剂的条件下合成氨气。下列关于工业上合成氨的说法合理的是____。
A . 合成氨属于人工固氮 B . 合成原料氢气主要通过电解水获得 C . 将生成的氨气分离,可加快反应速率 D . 通过改良催化剂,可使反应更易发生
和锇为催化剂的条件下合成氨气。下列关于工业上合成氨的说法合理的是____。
A . 合成氨属于人工固氮 B . 合成原料氢气主要通过电解水获得 C . 将生成的氨气分离,可加快反应速率 D . 通过改良催化剂,可使反应更易发生 -
(3) 某兴趣小组在实验室中探究氮的氧化物的性质。
①利用铜和稀硝酸制取NO,化学方程式为,该反应中还原剂与氧化剂物质的量之比为。
②探究氮的氧化物性质的实验步骤及预期现象如下表:
步骤
预期现象
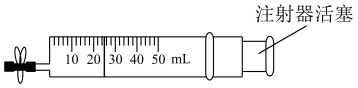
i.在一支注射器中吸入22.4mLNO(标准状况下),然后吸入5mL水,用乳胶管和弹簧夹封住管口,振荡注射器
无明显现象
ii.打开弹簧夹,快速吸入10mL空气后夹上弹簧夹,固定住注射署活塞
iii.松开注射器活塞,再振荡注射器
重复操作ii和iii,充分反应后,注射器中的溶液浓度为mol/L(假设反应前后液的体积几乎不变)。
-
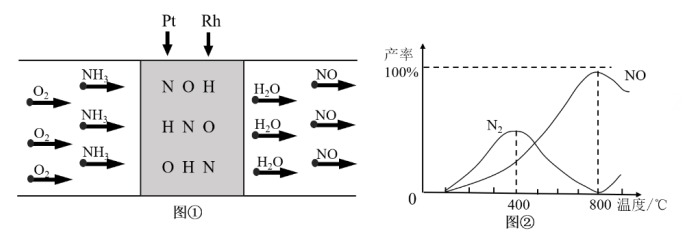
(4) 利用
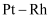 合金催化氧化
合金催化氧化 制取
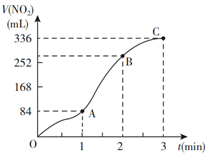
制取 , 图①是反应的微观模型,含氮生成物产率反应温度的变化曲线如图②所示。下列说法正确的是____。
, 图①是反应的微观模型,含氮生成物产率反应温度的变化曲线如图②所示。下列说法正确的是____。
 A . 可用湿润的蓝色石蕊试纸检验
A . 可用湿润的蓝色石蕊试纸检验 是否反应完全
B . 400℃时,生成的产物只有
是否反应完全
B . 400℃时,生成的产物只有 、
、 C . 800℃以上,可能发生反应:
C . 800℃以上,可能发生反应: D .
D . 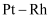 合金催化氧化
合金催化氧化 制取
制取 , 适宜的温度为800℃
, 适宜的温度为800℃
-
(1) 反应3Fe(s)+4H2O(g)
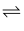 Fe3O4(s)+4H2(g),在一可变容积的密闭容器中进行,试回答:
Fe3O4(s)+4H2(g),在一可变容积的密闭容器中进行,试回答:
①保持体积不变,充入N2使体系压强增大,其正反应速率,逆反应速率。
②保持压强不变,充入N2使容器的体积增大,其正反应速率,逆反应速率。
-
(2) 海水提镁的重要步骤之一是用沉淀剂将海水中的Mg2+沉淀。该沉淀剂是(填“生石灰”或“盐酸”)。
-
(3) 盛有浓硫酸的烧杯敞口放置一段时间,质量增加,则浓硫酸表现出(填“吸水性”或“脱水性”)。
-
(4) 浓硫酸与碳共热时发生反应2H2SO4(浓)+C
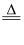 CO2↑+2SO2↑+2H2O,在该反应中,浓硫酸表现出,氧化产物是。
CO2↑+2SO2↑+2H2O,在该反应中,浓硫酸表现出,氧化产物是。
-
(5) 足量的Fe和稀硝酸反应的离子方程式为。
 )废水造成水体富营养化,必须脱除才能排放,常用的方法有化学沉淀法、氧化法等。
)废水造成水体富营养化,必须脱除才能排放,常用的方法有化学沉淀法、氧化法等。
-
(1) I.化学沉淀法:
向含有氨氮的废水中添加
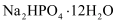 和
和 , 发生反应,生成
, 发生反应,生成 沉淀,写出该反应的离子方程式。
沉淀,写出该反应的离子方程式。 -
(2) 为探究溶液酸碱性对氨氮脱除效果的影响,室温下配制氨氮废水[
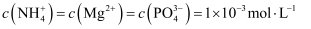 ],对该废水进行
],对该废水进行 值与氨氮脱除效果影响的实验研究,研究结果如图:
值与氨氮脱除效果影响的实验研究,研究结果如图: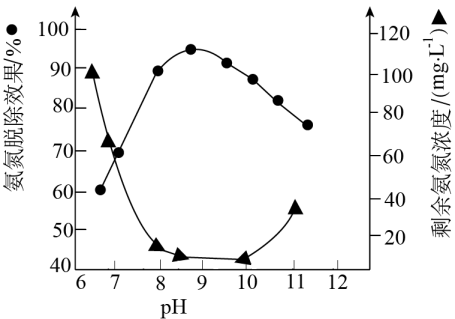
①氨氮脱除效果最佳的pH范围是。
a.6~7b.8~10c.10~12
②
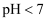 氨氮脱除率较低的原因为,
氨氮脱除率较低的原因为,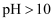 造成氨氮脱除率随
造成氨氮脱除率随 增大而减小的可能原因是。
增大而减小的可能原因是。 -
(3) II.氧化法:
 和
和 在有氧条件及催化剂作用下发生反应:
在有氧条件及催化剂作用下发生反应: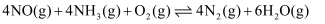
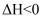 , 当温度升高到550~700℃时,NO转化率明显下降,
, 当温度升高到550~700℃时,NO转化率明显下降, 产率明显上升,可能原因是。
产率明显上升,可能原因是。
- A、B均是不与水反应的物质,在T3℃时,将A、B两物质分别溶于100g水中,刚好制成饱和溶液,然后降温(A、B物质的溶解
- 下列关于有机物的说法正确的是 A. 棉、麻、羊毛完全燃烧都只生成CO2和H2O B. 与是同分异构体,性质相似 C. 乙
- 三﹒完形填空 People do not analyse every problem they meet with. S
- “黄梅时节家家雨,青草池塘处处蛙”形象的描绘了我国哪一个地区的景象( ) A.长江中下游地区B.长江中上游地区 C
- ---Which of those English-Chinese dictionaries do you like m
- 把一长方体重物夹在两块竖直木板之间,在木板两侧施加水平压力,使重物保持静止,如图1所示.现分别用竖直向上和竖直向下的力把
- 已知钠不能与煤油、苯、四氯化碳等有机溶剂反应,且煤油、苯、四氯化碳均不溶于水,又知钠的密度为0.97g・cm-3,水的密
- 填写下列名句名篇的空缺部分 (1)学而不思则罔, !
- 当x=2时,代数式ax3+bx+1的值为3,那么当x=-2时,代数式ax3+bx+1的值是( )A.1B.-1C.3D
- 若数列是等差数列,则有数列类比上述性质,相应地:若数列是等比数列,且,则有数列
- 已知关于x的方程2x﹣3a=﹣1的解为x=﹣1,则a的值等于.
- 已知2A2(g)+B2(g) 2C3(g);△H=-Q1kJ/mol(Q1>0), 在一个有催化剂的固定容积的容器
- 激素作为~种化学信使,能把某种调节的信息由内分泌细胞携带至靶细胞。下图表示影响胰岛A细胞分泌的因素及其发挥作用的过程,相
- ---CouldI do it? ---Yes, you ____.A.may B.mi
- 某矿泉水标签的部分内容如图所示,阅读后完成下列相关问题: (1)亚铁离子的化学符号. (2)偏硅酸中硅元素的化合价; (
- 阅读下面的文言文,完成10~13题。梅圣俞诗集序〔宋〕欧阳修予闻世谓诗人少达而多穷,夫岂然哉?盖世所传诗者,多出于古穷人
- 图3为福建省1982年和2005年交通与城市发展示意图。读图,回答8、9题。8.1982——2005年期间,福建省 A.
- .(6分)如图,将腰长为的等腰Rt△ABC(∠C是直角)放在平面直角坐标系中的第二象限,其中点A在y轴上,点B在抛物线y
- 下列各组词语中加点字注音完全正确的一项是( ) A.屏除(bǐng) 椎心泣血(zhuī) 抛头露面(lù)
- 商品是用于交换的劳动产品。下列属于商品的是 ( )①原始森林 ②自产自用的



