第1节 铁的多样性 知识点题库
烧杯、试管、玻璃棒、酒精灯、漏斗、过滤架、滤纸、量筒、容量瓶、滴管、药匙;1mol/L硫酸、2mol/L硝酸、2mol/LNaOH溶液、10%KSCN溶液、稀氨水.
提示:ZnO、Zn(OH)2都是两性物质;且Zn(OH)2能溶于烧碱溶液生成Na2ZnO2 , 能溶于浓氨水生成[Zn(NH3)4](OH)2 .
(1)请写出ZnO与烧碱溶液反应的化学方程式:ZnO+2NaOH=
(2)请完成以下实验探究过程
①提出假设:假设1 该混合物中除Al2O3外还含有 ;
假设2 该混合物中除Al2O3外还含有 ;
假设3 该混合物中除Al2O3外还含有Fe2O3、ZnO.
②设计实验方案:基于假设3,设计出实验方案.请在下表对应栏目叙述实验操作、预期现象和结论(实验步骤可以不填满、也可以增加):
实验步聚 | 实验操作 | 预期现象和结论 |
第一步 |
|
|
第二步 |
| |
第三步 |
|
|
第四步 |
|
|
单质 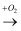 氧化物
氧化物 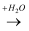 酸或碱
酸或碱 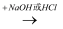 盐.
盐.
-
(1) 其中一个反应为3FeS2+8O2=6SO2+Fe3O4 , 则氧化产物为,若有3mol FeS2参加反应,则转移mol 电子.
-
(2) 氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式为.
-
(3) 与明矾相似,硫酸铁也可用作净水剂,其原理是(用离子方程式表示).
-
(4) 铁红是一种红色颜料,其成分是Fe2O3 , 将一定量的铁红溶于160ml 5molL 盐酸中,再加入一定量铁粉,两者恰好完全溶解,并收集到2.24L(标准状况)H2 , 经检测,溶液中无Fe3+ , 则参加反应的铁粉的质量为g
-
(5) FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为.
-
(1) 加入盐酸可抑制Fe3+及生成的Cu2+的水解, Fe3+水解的离子方程式为。
-
(2) FeCl3溶液蚀刻铜的化学方程式为。
-
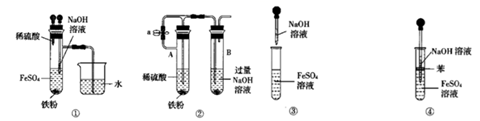
(3) 测定某废蚀刻液中Cu2+含量的实验步骤如下:量取25.00mL废蚀刻液,加入足量的NH4HF2(掩蔽Fe3+ , 消除干扰),加入稍过量KI溶液(2Cu2++4I-=2CuI↓+ I2),在暗处静置5min,然后用0.02000mol·L-1Na2S2O3标准溶液滴定(I2+2S2O
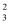 =2I-+S4O
=2I-+S4O  ),接近终点时,加入淀粉和10mL10%NH4SCN溶液(CuI可吸附少量I2 , CuSCN不吸附I2),继续滴定至终点,消耗Na2S2O3溶液20.00mL。
),接近终点时,加入淀粉和10mL10%NH4SCN溶液(CuI可吸附少量I2 , CuSCN不吸附I2),继续滴定至终点,消耗Na2S2O3溶液20.00mL。 ①不加NH4HF2会导致测得的铜的含量(填:“偏高”“偏低”或“不变”)。
②通过计算确定该废蚀刻液中铜的含量(单位g·L-1 , 写出计算过程)。
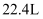 的
的  通入足量稀硝酸,电子转移
通入足量稀硝酸,电子转移 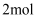 B . 标况下,
B . 标况下, 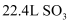 溶于水形成
溶于水形成 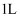 的溶液,所得溶液的物质的量浓度为
的溶液,所得溶液的物质的量浓度为 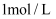 C . 常温下,将
C . 常温下,将 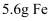 投入足量的浓硫酸中转移电子的物质的量为
投入足量的浓硫酸中转移电子的物质的量为 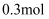 D . 用
D . 用  溶液吸收工业废气中的
溶液吸收工业废气中的  :
:  ,氧化剂与还原剂物质的量比为1∶1
,氧化剂与还原剂物质的量比为1∶1
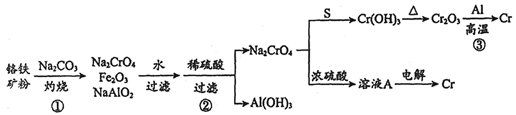
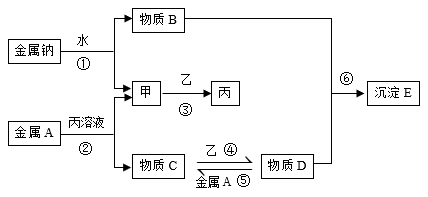
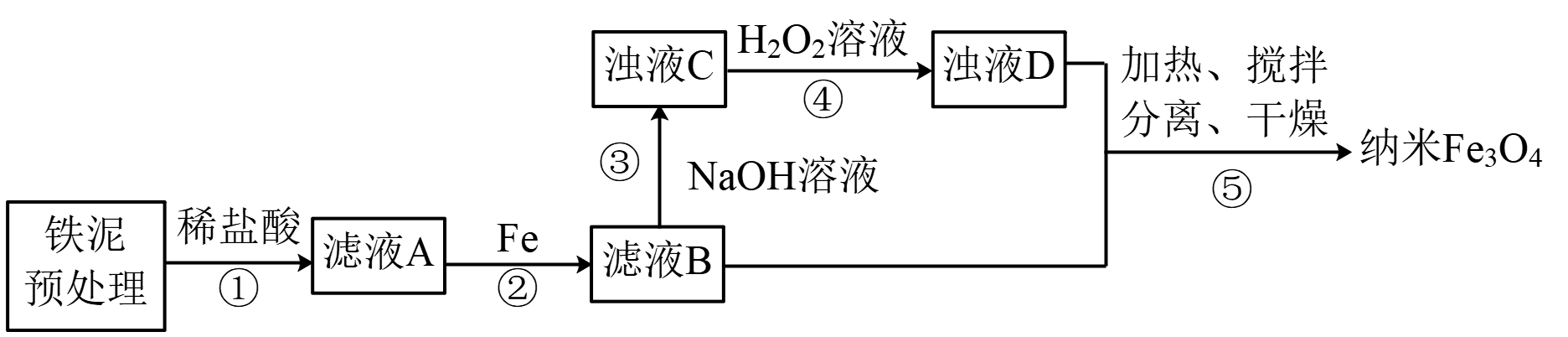
请根据以上信息回答下列问题:
-
(1) 写出反应①和④的化学方程式、。
-
(2) 写出反应⑤的离子方程式。
-
(3) 写出气体乙与水反应的离子方程式。
-
(4) 写出一个化合反应生成E。
-
(5) “维生素C”也可将物质D转化为物质C,试分析“维生素C”在这一反应过程中的作用是。
| 选项 | 实验操作和现象 | 结论 |
| A | 向某溶液中,滴加氯水后,再滴加KSCN溶液,结果溶液变为红色 | 该溶液中一定含有Fe2+ |
| B | 向硫酸催化下的淀粉溶液中,加入新制Cu(OH)2悬浊液,并加热,结果未生成砖红色沉淀 | 该淀粉溶液一定未水解 |
| C | 向AgNO3溶液中加入NaCl溶液,生成白色沉淀,再滴加Na2S溶液,又生成黑色沉淀 | Ksp(AgCl)>Ksp(Ag2S) |
| D | 用醋酸浸泡有水垢的水壶,能除去水垢 | 酸性:CH3COOH>H2CO3 |
序号 | 取样时间/min | 现象 |
ⅰ | 3 | 产生大量白色沉淀;溶液呈红色 |
ⅱ | 30 | 产生白色沉淀,较3min时量少;溶液红色较3min时加深 |
ⅲ | 120 | 产生白色沉淀,较30min时量少;溶液红色较30min时变浅 |
(资料:Ag+与SCN-生成白色沉淀AgSCN)
依据上述实验现象,不能得出的结论是( )
 具有氧化性
D . 30min时“白色沉淀量减少,溶液红色加深”的原因可能是:Fe2++Ag+=Fe3++Ag
具有氧化性
D . 30min时“白色沉淀量减少,溶液红色加深”的原因可能是:Fe2++Ag+=Fe3++Ag
下列叙述不正确的是( )
- The smartphonehas become the centerpiece of many students' d
- 某质点作直线运动,速度随时间的变化的关系式为v =(4+2t)m/s ,则对这个质点运动的描述,正确的是A.初速度为4
- 设与是定义在同一区间[a,b]上的两个函数,若对任意∈[a,b],都有成立,则称和在[a,b]上是“紧密函数”,区间[a
- (10分)阅读材料,回答问题。 材料一 《天仙配》是中国的一个美丽神话故事,它寄托着下层劳动人民对自由纯真爱情的向往。
- 在做“测滑轮组的机械效率”实验时,对同一滑轮组进行了两次实验,得到如下的数据(g=10N/kg): (1)计算两次
- 下面左图为某草原生态系统的结构简图,“→”表示碳的流动方向,右图表示某植食性昆虫迁入该生态系统后的种群数量增长率变化曲线
- We have every reason to believe that ______ 2010 World Expos
- 在口中咀嚼米饭和馒头时会感到有甜味,这是因为 ,它能将食物中部分淀粉催化水解为
- 下列几个关于力学问题的说法中正确的是 A.米、千克、牛顿等都是国际单位制中的基本单位 B.放在斜面上的物体,其重力沿垂直
- 下列4个种群不同年龄的个体数曲线图中,依次表示的是()A.甲、乙表示衰退型,丙表示稳定型,丁表示增长型 B.甲表示增长型
- 右图是元素周期表中的一部分,下列有关说法中正确的是 ( ) A.锂原子的原子序数为3 B.氢元素的相对原子质量
- 在石油化工及煤化工中,下列加工工艺只发生物理变化的是 A.分馏 B.干馏
- 太阳直射南回归线时,应是北半球的 ( )
- 单项选择 What’s that English? ——It’s UFO. A
- 马克思说:“巴黎公社不过是特殊条件下的一个城市的起义,而且公社的大多数人根本不是社会主义者,也不可能是社会主义者。”对马
- The experiment they had prepared for nearlya whole week ___
- 地球的自转和公转的方向( ) A.自东向西转 B.逆时针转 C.顺时针转 D.自西向东转
- 与中英《南京条约》比较,中日《马关条约》新增的内容是 A.割地 B.开通商口岸 C.赔款
- 已知等差数列{an}的首项a1=1,公差d>0,且第2项、第5项、第14项分别是等比数列{bn}的第2项、第3项、第4项
- (1)已知,求函数的最大值;(2)已知,且,求的最小值.



