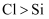第二单元 硫及其化合物的相互转化 知识点题库
-
(1) 组成羰基硫的元素中,原子半径最小的元素在周期表中的位置是
-
(2) 乙硫醇有特殊气味,是天然气的臭味指示剂.乙硫醇可以看作是乙醇分子中羟基(﹣OH)被﹣SH取代,则乙硫醇的结构式为
-
(3) 下列事实可用于比较C与S两种元素非金属性(原子得电子能力)相对强弱的是 (填序号).
a.沸点:H2S>CH4 b.元素在周期表中的位置 c.酸性:H2SO3>H2CO3 d.同温同浓度水溶液的pH:Na2CO3>Na2SO4
-
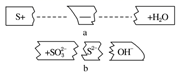
(4)
羰基硫水解及利用的过程如下(部分产物已略去):COS
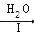 H2S
H2S Na2S溶液
Na2S溶液 X溶液+H2
X溶液+H2①常温下,在反应Ⅱ中,每吸收lgH2S气体放出热量a kJ,其热化学方程式为
②已知X溶液中硫元素的主要存在形式为S2O32﹣ , 则反应Ⅲ中生成该离子的离子方程式为
③如图是反应Ⅲ中,在不同反应温度下,反应时间与H2产量的关系图(Na2S初始含量为3mmo1).请结合图象数据解释X溶液中除S2O32﹣外,还有SO32﹣、SO42﹣的原因.答:
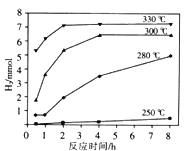
类比对象 | 结论 | |
A. | Cl2+H2O═HCl+HClO | I2+H2O═HI+HIO |
B. | Cl2+2Fe2+═2Fe3++2Cl﹣ | I2+2Fe2+═2Fe3++2I﹣ |
C. | S+Fe═FeS | S+Cu═CuS |
D. | Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO | Ca(ClO)2+SO2+H2O ═CaSO3↓+2HClO |
-
(1) 干法制备高铁酸钠的主要反应为:2FeSO4 + aNa2O2 =2Na2FeO4 + bX + 2Na2SO4 + c O2↑
①该反应中物质 X 应是,a 与 c 的关系是。
②简要说明 K2FeO4 作为水处理剂时,在水处理过程中所起的作用。
-
(2) 湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式: 。
②若反应过程中转移了0.3mo1电子,则还原产物的物质的量为 mol。
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题。
-
(1) 双氧水能使酸性KMnO4溶液褪色,反应式中H2O2的化学计量数为。
-
(2) KMnO4可与浓盐酸反应制氯气,反应式中HCl的化学计量数为。
-
(3) 单质氯气与强碱溶液共热可生成氯化物和氯酸盐,其离子方程式中OH-离子的化学计量数为。
-
(4) 离子方程式(未配平)SnCl2+Cl-+H3AsO3+H+→As+SnCl62-+M(未知物),其中未知物M的化学计量数和化学式分别为 、。
-
(1) Ca与最活跃的非金属元素A形成化合物D,D的电子式为,D的沸点比A与
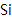 形成的化合物E的沸点.(填“高”或“低”)
形成的化合物E的沸点.(填“高”或“低”)
-
(2) 配平用钙线氧脱鳞的化学方程式:__P+ __FeO+__CaO
 __Ca3(PO4)2+__Fe
__Ca3(PO4)2+__Fe
-
(3) 将钙线试样溶于稀盐酸后,加入过量
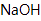 溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色
溶液,生成白色絮状沉淀并迅速变成灰绿色,最后变成红褐色 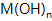 .则金属M为(填元素符号);检测溶液中含有
.则金属M为(填元素符号);检测溶液中含有 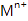 的方法是.
的方法是.
-
(4) 取1.6g钙线试样,与水充分反映,生成224mL
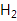 (标准状况),在此溶液中通入适量的
(标准状况),在此溶液中通入适量的 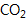 ,最多能得到
,最多能得到 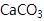 g.
g.
-
(1) Al2(SO4)3+3H2
 Al2O3 +3SO2 +3H2O 电子转移 氧化剂是
Al2O3 +3SO2 +3H2O 电子转移 氧化剂是
-
(2) 6KMnO4 +5KI +3H2O= 6KOH+6MnO+5KIO3 电子转移 氧化剂是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2已经变质 |
| B | 乙酸乙酯与NaOH溶液共热、搅拌 | 液体不再分层 | 乙酸乙酯在碱性条件下完全水解生成溶于水的物质 |
| C | 向黄色的Fe(NO3)3溶液中滴加氢碘酸 | 溶液变为黄褐色 | 氧化性:Fe3+>I2 |
| D | 微热滴加了酚酞的NaHCO3溶液 | 溶液红色加深 | NaHCO3分解产生Na2CO3 |
-
(1) 某汽车安全气囊的产气药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质。当汽车发生碰撞时,NaN3迅速分解产生N2和Na,同时放出大量的热。N2使气囊迅速膨胀,从而起到保护作用。
① KClO4的名称是,具有(填“还原性”或“氧化性”)。
② Fe2O3可处理产生的Na,反应为6Na+Fe2O3 =3Na2O+2Fe,反应中Na作(填“还原剂”或“氧化剂”)。
反应过程中氧化产物与还原产物的个数比为:。
-
(2) Na2O2可用于呼吸面具或潜水艇中氧气的来源。某实验小组利用下图装置探究Na2O2与CO2的反应。请回答下列问题:
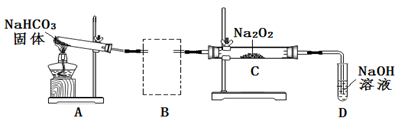
①根据实验目的,虚线框中的装置所用的试剂为。
②装置C中观察到的现象是,反应的化学方程式是。
③装置A的作用是制备CO2 , 写出A中发生反应的化学方程式是。
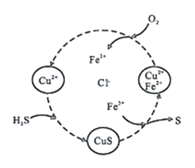
 2S↓+2H2O
C . 由图示的转化可得出:氧化性的强弱顺序为O2>Cu2+>S
D . 保持溶液中Fe3+的量不变,反应中消耗标况下22.4L的O2 , 可以生成64g硫
2S↓+2H2O
C . 由图示的转化可得出:氧化性的强弱顺序为O2>Cu2+>S
D . 保持溶液中Fe3+的量不变,反应中消耗标况下22.4L的O2 , 可以生成64g硫
| 选项 | 实验操作和实验现象 | 结论 |
| A | 向 | 氧化性: |
| B | 向盛某盐溶液的试管中滴入浓氢氧化钠溶液并加热,试管口处湿润的红色石蕊试纸变蓝 | 该盐中含有 |
| C | 将稀盐酸滴入 | 非金属性: |
| D | 将红热的炭放入浓硫酸中,产生的气体通入澄清石灰水,石灰水变浑浊 | 碳被氧化成 |
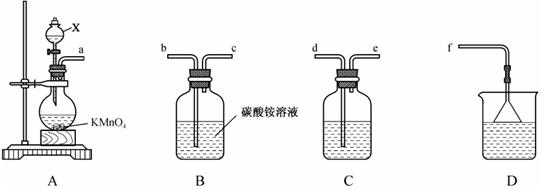
回答下列问题:
-
(1) 装置A中仪器X的名称是,盛放的试剂是,装置A中发生反应的离子方程式为。
-
(2) 整个装置的导管连接顺序为a→→→→→ 。
-
(3) 装置B中发生反应的化学方程式为。
-
(4) 装置C的作用为;装置D的作用为。
-
(5) 三氯化氮浓度的测定:准确量取20 mL装置B中反应后的溶液,置于100 mL容量瓶中,用水稀释至刻度,摇匀,吸取25.0 mL于烧杯中,加入足量V1 mL c1 mol·L-1亚硫酸钠溶液,充分反应后,向烧杯中加入足量V2 mLc2 mol·L-1 盐酸酸化的氯化钡溶液,得沉淀mg。
已知:i.Na2SO3+NCl3 +
 =Na2SO4+ HCl+NH4Cl;
=Na2SO4+ HCl+NH4Cl;ⅱ.BaCl2+Na2SO4=BaSO4↓十2HCl。
①请完成反应i的化学方程式(横线填数字,方框中填化学式):
ⅰ Na2SO3+NCl3+
 =Na2SO4+ HCl+NH4Cl
=Na2SO4+ HCl+NH4Cl②装置B反应后的溶液中三氯化氮的浓度为mol·L-1。
 (胶体)
(胶体) 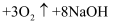 。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
。相比传统的用氯气进行水的消毒处理,高铁酸钠安全无异味,投加更方便。请回答下列问题:
-
(1) 高铁酸钠(Na2FeO4)属于(“酸”、“碱”、“盐”或“氧化物”),其中铁的化合价为价;与O2互为同素异形体的物质的化学式为。
-
(2) 将上述反应的化学方程式改写成离子方程式:,该反应中的O2为(填标号)。
a.氧化产物 b.还原产物 c.既不是氧化产物又不是还原产物
-
(3) 实验室制备
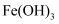 胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴(填化学式)饱和溶液,继续煮沸至液体呈色,停止加热。
胶体的操作:向烧杯中加入40mL蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴(填化学式)饱和溶液,继续煮沸至液体呈色,停止加热。
-
(4) 当生成48g O2时,至少有g水参与反应,生成的NaOH的质量为g。
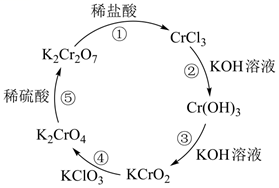
已知:反应①: 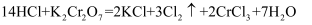 ;
;
反应④:  。
。
-
(1) 用单线桥法标出反应①和④的电子转移方向和数目:、。反应①中还原剂为(填化学式,下同),还原产物为。反应④中被氧化的元素为(填元素符号)
-
(2) 在上述有标号的反应中,不属于氧化还原反应的是(填标号)
-
(3) 写出反应⑤的离子方程式。
A | B | C | D | |
物质 | H2S、SO2 | FeS、CuS | CH4、C2H2 | Na2CO3、Na2SO4 |
鉴别方法 | 通入溴水 | 加入水 | 燃烧 | 加入AlCl3溶液 |
- 设向量与的夹角为,且,,则( ) A. B. C. D.
- 阅读下面短文,然后按照要求写一篇150词左右的英语短文。 Oseola McCarty spent morethan 7
- 已知中,内角A、B、C所对边长分别为a、b、c, (I)求B: (II)若a=2.求的面积
- 如图所示,把一个长方形纸片沿EF折叠后,点D,C分别落在D′,C′的位置.若∠EFB=65°,则∠AED′等于(
- 人的卷舌与非卷舌分别由R和r基因控制,某学生的父母均能卷舌,但本人不能卷舌,他的父母基因组成为( )A.RR和RR
- 小明的哥哥成家后,还是与父母住在一起,一家5口人其乐融融,十分幸福,这样的家庭属于 A.核心家庭B.主干家庭C.单亲家庭
- 关于物理学史,下列说法中不正确的是() A.电荷量e的数值最早是由美国物理学家密立根测得的 B.法拉第不仅提出了场的的概
- 人民币防伪技术之一是光学变色油墨。某变色油墨中含有汞的碘化物,汞元素符号是
- 重金属污染,是威胁人类身体健康的“隐形杀手”。1953年日本发生过震惊世界的水俣病事件,就是由工业污染造成了重金属物质汞
- 下列化学方程式中,不能正确表达反应颜色变化的是 A.向CuSO4溶液中加入足量Zn粉,溶液蓝色消失:Zn+CuSO4Cu
- 在如下数表中,已知每行、每列中的数都成等差数列,那么位于表中的第n行第n+1列的数是________.
- 如图为“用DIS(位移传感器、数据采集器、计算机)研究加速度和力的关系”的实验装置。(1)在该实验中必须采用控制变量法
- 下列物质由分子构成的是() A.汞 B.干冰 C.金刚石 D.氯化钠
- 如图所示,A为信号源,B为接收器,A、B间有一真空区域.当信号源A分别发射出次声波、无线电波、可见光和紫外线信号时,接收
- 阅读《背影》片段,回答问题。(12分) 1 那年冬天,祖母死了,父亲的差使也交卸了,正是祸不单行的日子。我从北京到徐州,
- 在图甲所示的电路中,已知电源为电压可调的直流学生电源,R0是定值电阻,灯泡L1的额定电压为8V,图乙是灯泡L2的U-I图
- 下列物质的俗名错误的是( ) A. 固体二氧化碳 干冰 B. 硫酸铜胆矾 C. 氢氧化钙
- 《巴黎圣母院》中流浪人为什么攻打圣母院?此事结局如何?请简述。
- 电容式位移传感器,其工作原理如图所示。当被测物体在左右方向发生位移时,电介质板随之在电容器两极板之间移动。如果测出了电容
- 如图是“用显微镜观察人体口腔上皮细胞”的部分操作步骤,请看图并回答下列问题:(1)
 和
和  的混合溶液中滴入酸化的
的混合溶液中滴入酸化的 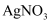 溶液,混合溶液变红
溶液,混合溶液变红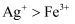

 溶液中,溶液中出现凝胶
溶液中,溶液中出现凝胶