第二单元 硫及其化合物的相互转化 知识点题库
酸性条件下,可用某些盐溶液吸收水煤气中的少量H2S,以回收硫元素、降低污染.欲达到该目的,下列试剂中最合适的是( )
A . KClO3
B . FeCl2
C . HNO3
D . FeCl3
某实验小组为探究ClO﹣、I2、SO 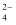 在酸性条件下的氧化性强弱,已知I2遇淀粉变蓝,设计实验如下:
在酸性条件下的氧化性强弱,已知I2遇淀粉变蓝,设计实验如下:
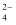 在酸性条件下的氧化性强弱,已知I2遇淀粉变蓝,设计实验如下:
在酸性条件下的氧化性强弱,已知I2遇淀粉变蓝,设计实验如下: 实验①:在淀粉KI溶液中加入少量NaClO溶液,并加入少量的稀H2SO4 , 溶液立即变蓝;
实验②:向实验①的溶液中加入4L 0.5mol/L的Na2SO3溶液,发生反应如下
SO 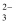 +I2+H2O→SO
+I2+H2O→SO 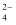 +I﹣+H+(未配平),恰好完全反应.
+I﹣+H+(未配平),恰好完全反应.
-
(1) 以上实验说明,在酸性条件下ClO﹣、I2、SO42﹣的氧化性由弱到强的顺序是.
-
(2) 实验②中化学反应转移电子的物质的量是.
-
(3) 写出实验①中发生反应的离子方程式.
下列装置或操作不能达到实验目的是( )
A .  比较Cl2、Fe3+、I2的氧化性
B .
比较Cl2、Fe3+、I2的氧化性
B . 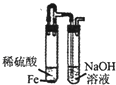 制取Fe(OH)2
C .
制取Fe(OH)2
C . 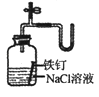 证明铁生锈时空气参加反应
D .
证明铁生锈时空气参加反应
D . 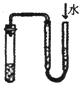 检查装置气密性
检查装置气密性
 比较Cl2、Fe3+、I2的氧化性
B .
比较Cl2、Fe3+、I2的氧化性
B .  制取Fe(OH)2
C .
制取Fe(OH)2
C .  证明铁生锈时空气参加反应
D .
证明铁生锈时空气参加反应
D .  检查装置气密性
检查装置气密性
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A . 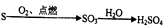 B .
B . 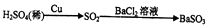 C .
C . 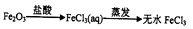 D .
D . 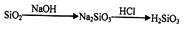
将Cu片放入0.1mol/L的 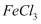 溶液中,一段时间后取出
溶液中,一段时间后取出 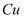 片,溶液中
片,溶液中 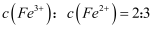 ,则
,则 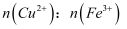 为( )
为( )
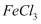 溶液中,一段时间后取出
溶液中,一段时间后取出 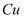 片,溶液中
片,溶液中 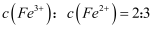 ,则
,则 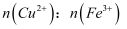 为( )
为( )
A . 3:4
B . 3:5
C . 4:3
D . 3:2
已知反应: ①Cl2+2KBr=2KCl+Br2 , ②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O,
③2KBrO3+Cl2=Br2+2KClO3 , 下列说法正确的是 ( )
A . 上述3个反应都是置换反应
B . ③中1 mol 氧化剂参加反应得到电子的物质的量为10 NA
C . 反应②中若得到13.44L Cl2 , 则电子转移个数为6.02×1023
D . 氧化性由强到弱的顺序为: KBrO3 > KClO3 > Cl2 > Br2
一定条件下,下列各组物质能一步实现 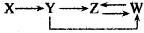 转化关系的是( )
转化关系的是( )
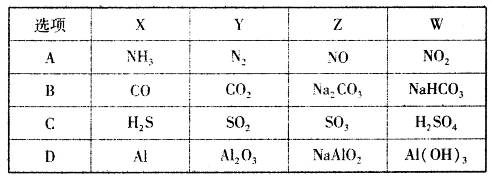
A . A
B . B
C . C
D . D
-
(1) Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中Na2O2 是(填氧化剂、还原剂),与CO2反应的化学反应方程式。
-
(2) 湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为mol。
-
(3) Ⅱ.已知:2Fe3++2I-=2Fe2++I2 , 2Fe2++Br2=2Fe3++2Br-。
含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2 , 此时被氧化的离子是。
-
(4) 若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2 , 当I-、Fe2+、Br-完全被氧化时,c=(用含a、b的代数式表示)。
为防止废弃的硒单质(Se)造成环境污染,通常用浓硫酸将其转化成二氧化硒(SeO2),再用KI溶液处理后回收Se。发生的反应为:①Se+2H2SO4(浓)=2SO2+SeO2+2H2O、②SeO2+4KI+4HNO3=4KNO3+Se+2I2+2H2O,下列说法错误的是( )
A . ①中SO2是还原产物,SeO2是氧化产物
B . ②中KI是还原剂,HNO3是氧化剂
C . 每生成0.4molI2共转移1.2mol电子
D . 氧化性由强到弱的顺序是:H2SO4(浓)>SeO2>HNO3
在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是( )
A . 在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32-
B . 含等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+
C . 含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH)2、K2CO3、BaCO3
D . 在含Fe3+、H+、NH4+的溶液中逐渐加入烧碱溶液:H+、NH4+、Fe3+
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。下列分析正确的是( )
A . 滴加KI溶液时,转移2mol电子时生成1mol白色沉淀
B . 通入SO2后溶液逐渐变成无色,体现了SO2的漂白性
C . 通入SO2时,SO2与I2反应,I2作还原剂
D . 上述实验条件下,物质的氧化性:Cu2+>I2>SO2
已知某物质X能发生如下转化:
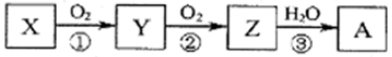
下列有关上述转化关系中物质及其反应的叙述错误的是( )
A . 若X为N2 , 则A为硝酸
B . 若X为S,则A为硫酸
C . 反应①和②一定为氧化还原反应,反应③一定为非氧化还原反应
D . 若X为非金属单质或非金属氢化物,则A不一定能与金属铜反应生成Y
3Na2S+4H2SO4(浓)=3Na2SO4+4S↓+4H2O,氧化剂与还原剂的物质的量之比为( )
A . 3:4
B . 4:3
C . 1:3
D . 3:1
工业尾气中含有的SO2对环境有害,采取合理的方法可以将其转化为硫化钙、硫酸钾等有用的物质。其一种转化路线如图所示:
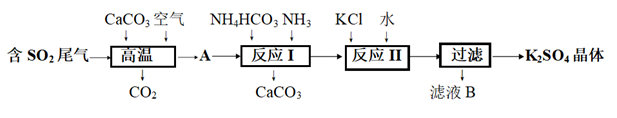
-
(1) 提高尾气中SO2的去除率,在高温反应时可采用的常用措施是,得到的固体产物A是(写化学式)。
-
(2) 反应Ⅰ的化学方程式为,该反应需在60℃~70℃下进行,温度不能高于70℃的原因除了减少氨气挥发外还有。
-
(3) 固体A与过量焦炭一起焙烧生成CaS,该反应的化学方程式。
-
(4) 滤液B中除K+、SO
 离子外,大量存在的的离子还有。
离子外,大量存在的的离子还有。
硫酰氯(SO2Cl2)可用于有机合成和药物制造等。实验室利用SO2和Cl2在活性炭作用下制取SO2Cl2[SO2(g)+Cl2(g)  SO2Cl2(l) ΔH= -97.3kJ/mol],装置如图所示(部分装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈反应并产生白雾。下列说法错误的是( )
SO2Cl2(l) ΔH= -97.3kJ/mol],装置如图所示(部分装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈反应并产生白雾。下列说法错误的是( )
 SO2Cl2(l) ΔH= -97.3kJ/mol],装置如图所示(部分装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈反应并产生白雾。下列说法错误的是( )
SO2Cl2(l) ΔH= -97.3kJ/mol],装置如图所示(部分装置省略)。已知SO2Cl2的熔点为-54.1℃,沸点为69.1℃,遇水能发生剧烈反应并产生白雾。下列说法错误的是( ) 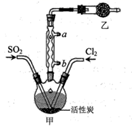
A . 乙装置中盛放的试剂是P2O5 , 防止水蒸气进入装置中
B . 装置甲应置于冰水浴中,目的是提高SO2Cl2产率
C . 反应结束后,分离甲中混合物的实验操作是蒸馏
D . SO2、Cl2均可使品红试液褪色,原理不相同
在给定条件下,下列物质间转化能实现的是( )
A . S  SO2
SO2  H2SO3
B . NH3
H2SO3
B . NH3 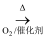 NO2
NO2  HNO3
C . Fe2O3
HNO3
C . Fe2O3 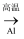 Fe
Fe  FeCl3
D . Al
FeCl3
D . Al  NaAlO2
NaAlO2 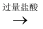 Al(OH)3
Al(OH)3
 SO2
SO2  H2SO3
B . NH3
H2SO3
B . NH3 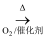 NO2
NO2  HNO3
C . Fe2O3
HNO3
C . Fe2O3 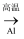 Fe
Fe  FeCl3
D . Al
FeCl3
D . Al  NaAlO2
NaAlO2 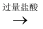 Al(OH)3
Al(OH)3
已知甲、乙、丙三种物质均含有同种元素,其转化关系如下(反应条件已略去)。
![]()
下列推断错误的是( )
A . 若丙为红棕色气体,则甲可能为  B . 若丙为
B . 若丙为  ,则X与稀盐酸反应可以得到丙
C . 若乙为
,则X与稀盐酸反应可以得到丙
C . 若乙为  ,则甲可能是
,则甲可能是  D . 若乙能使品红溶液褪色,则甲一定是S单质
D . 若乙能使品红溶液褪色,则甲一定是S单质
 B . 若丙为
B . 若丙为  ,则X与稀盐酸反应可以得到丙
C . 若乙为
,则X与稀盐酸反应可以得到丙
C . 若乙为  ,则甲可能是
,则甲可能是  D . 若乙能使品红溶液褪色,则甲一定是S单质
D . 若乙能使品红溶液褪色,则甲一定是S单质
五氟化锑( 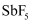 )是非常强的路易斯酸其酸性是纯硫酸的1500万倍。以某矿(主要成分为
)是非常强的路易斯酸其酸性是纯硫酸的1500万倍。以某矿(主要成分为  ,含有少量CuO、PbO、
,含有少量CuO、PbO、  等杂质)为原料制备
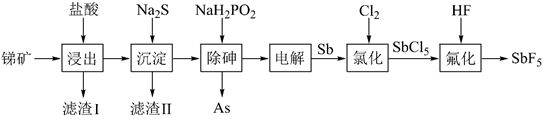
等杂质)为原料制备 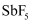 的工艺流程如图。
的工艺流程如图。
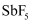 )是非常强的路易斯酸其酸性是纯硫酸的1500万倍。以某矿(主要成分为
)是非常强的路易斯酸其酸性是纯硫酸的1500万倍。以某矿(主要成分为  ,含有少量CuO、PbO、
,含有少量CuO、PbO、  等杂质)为原料制备
等杂质)为原料制备 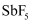 的工艺流程如图。
的工艺流程如图。
已知:I.CuS、PbS的Ksp分别为 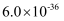 、
、 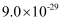
Ⅱ.  微溶于水、
微溶于水、  难溶于水,它们均为两性氧化物;SbOCl难溶于水。
难溶于水,它们均为两性氧化物;SbOCl难溶于水。
回答下列问题:
-
(1) 浸出时少量
 转化为SbOCl,为“滤渣Ⅰ”的成分,加入氨水对其“除氯”转化为
转化为SbOCl,为“滤渣Ⅰ”的成分,加入氨水对其“除氯”转化为  ,该反应的离子方程式为
,该反应的离子方程式为
-
(2) “除砷”时,
 转化为
转化为  ,该反应的离子方程式为
,该反应的离子方程式为
-
(3)
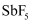 与
与 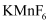 反应,首次实现了用化学方法制取F2 , 同时生成
反应,首次实现了用化学方法制取F2 , 同时生成 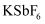 和
和 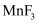 ,化学反应方程式为
,化学反应方程式为
-
(4) 已知

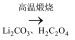 LiFePO4 , 写出该反应的化学方程式
LiFePO4 , 写出该反应的化学方程式
二氧化硫 是大气主要污染物脱硫是环境治理的热点问题。回答下列问题。
是大气主要污染物脱硫是环境治理的热点问题。回答下列问题。
 是大气主要污染物脱硫是环境治理的热点问题。回答下列问题。
是大气主要污染物脱硫是环境治理的热点问题。回答下列问题。
-
(1) 利用
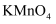 吸收
吸收 的离子方程式为:
的离子方程式为:
 +□ (在“□”里填入系数在“ ”上填入微粒符号),加入
+□ (在“□”里填入系数在“ ”上填入微粒符号),加入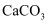 可以提高
可以提高 去除率,原因是。
去除率,原因是。 -
(2) 工业上还常用氨水吸收法处理
 , 可生成
, 可生成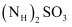 或
或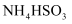 。
。
①
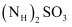 显碱性,结合化学用语,用化学平衡原理解释其原因:。
显碱性,结合化学用语,用化学平衡原理解释其原因:。②
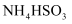 显酸性。用氨水吸收
显酸性。用氨水吸收 , 当吸收液显中性时溶液中离子浓度关系正确的是(填字母)。
, 当吸收液显中性时溶液中离子浓度关系正确的是(填字母)。a.

b.
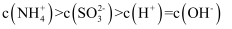
c.

-
(3) 某工厂烟气中主要含
 、
、 , 在较高温度经下图所示方法脱除
, 在较高温度经下图所示方法脱除 并制得
并制得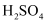 。
。
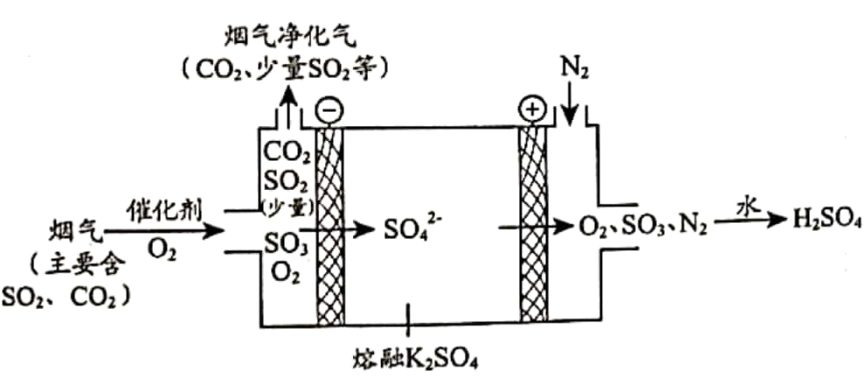
①在阴极放电的物质是。
②在阳极生成
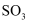 的电极反应式是。
的电极反应式是。
下列说法涉及物质的氧化性或还原性的是( )
A . 用葡萄糖制镜
B . 用硫酸铝净水
C . 用小苏打作食品膨松剂
D . 用氟化物添加在牙膏中预防龋齿
最近更新
- 下图表示2A(g)+B(g)2C(g)(正反应放热)。这个可逆反应的正确图像为 ( )
- 设、是非空数集,定义∪∩,已知集合,,则( ) A.∪ B.∪ C.
- 在西方人文精神的起源和发展过程中,欧洲思想家提出了各自的主张。下列思想家与其思想主张之间的对应关系正确的是( ) ①
- 下列各句中,标点符号使用正确的一句是() A.美国、欧共体、加拿大和日本等国的金融机构想进一步打开中国的金融市场,(包括
- 下图是制作“洋葱表皮细胞临时装片”实验的部分步骤,正确的操作顺序是() A.②③④①⑤ B.④③②①⑤ C.③④
- 目的基因导入受体细胞后,是否可以稳定维持和表达其遗传特性,只有通过鉴定和检测才能知道。下列属于目的基因检测和鉴定的是(
- 3000多年前,黎族人民横渡琼州海峡来到海南。他们在这方热土繁衍生息,创造了璀璨的文化:华美绝伦的黎族织锦,造型独特的船
- 目前妨碍台湾和祖国大陆统一的因素有( ) ①台湾岛内的分裂势
- 如图,D是△ABC边上的一点,AD=BD,∠ADC=70°,∠BAC=80°,则∠B=
- 近年来,我国气候持续异常。像北方一些城市,冬季气温持续偏高,降水稀少,造成各种呼吸道疾病,特别是流行性感冒频繁爆发,据调
- 图是亚热带欧亚大陆东部某地等高线分布图。对图示区域地理事象的叙述,正确的是A.①地位于三角洲
- 自从我上初中以后,我发现我个子长得特别的快、感觉特别敏锐发达、兴趣特别广泛、思维特别活跃等等。但,原来帅气的脸上莫名其妙
- 如图4-6-8所示,多匝线圈L的电阻和电池内阻不计,两个电阻的阻值都是R,电键S原来是断开的,电流I0=,今合上电键S将
- 碳及碳的化合物间的转化关系可表示为 CCOCO2,由此可写出各步反应的化学方程式。 硫及硫的化合物间的转化关系可表示为
- 梁启超说:“我国蚩蚩四亿之众,数千年受制于民贼政体之下,如盲鱼生长黑壑,不知天地间有□□二字。”省略的两字最可能是(
- 纳米技术给医学、环保、国防等领域带来突破的同时,科学家们也对纳米技术可能给环境和人类健康带来的风险抱有严重担忧。这说明(
- 19世纪中期以前,西方的科学家认为宇宙中有一种物质是弥漫在世界上,无所不在的。受其影响,19世纪90年代,谭嗣同撰写了《
- 有机物X的结构简式是,能用该结构简式表示的X的同分异构体共有(不考虑立体异构)00000 A.12种 B.
- 在平面直角坐标系xOy中,已知椭圆C:=1(a>b>0)的离心率e=,且椭圆C上的点到点Q(0,2)的距离的最大值为3.
- (重庆卷文15)已知圆C: (a为实数)上任意一点关于直线l:x-y+2=0的对称点都在圆C上,则a=



