第三单元 海洋化学资源的综合应用 知识点题库
海水开发利用的部分过程如图所示。下列说法错误的是( )
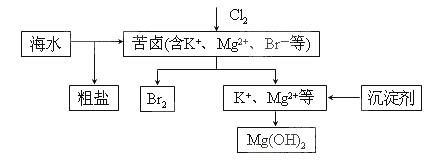
食盐是人类生活中不可缺少的物质,海水中含有大量食盐.某地出产的粗盐中,所含杂质是CaCl2 , 通过下面的实验可制得纯净的NaCl.
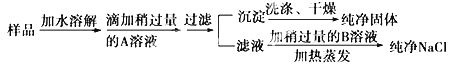
-
(1) 加入的A是 ,检验A已过量的方法是
-
(2) 加入的B是 ,加入稍过量B的目的是
-
(3) 为检验沉淀是否洗净,最好在最后几滴洗出液中加入 溶液
-
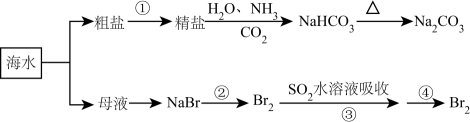
(1) Ⅰ、海水中制得的氯化钠除食用外,还用作工业原料,例如通常以NaCl、CO2和NH3为原料制取纯碱,请写出第一步制取NaHCO3的化学方程式:.
-
(2) Ⅱ、工业上以浓缩海水为原料提取溴的部分流程如图1:
已知:Br2常温下呈液态,易挥发,有毒:2Br2+3CO32﹣=5Br﹣+BrO3﹣+3CO2 .
①通过步骤①氯气氧化已获得含Br2的溶液,为何还需经过吹出、吸收、酸化来重新获得含Br2的溶液,原因是.
②反应釜2中发生反应的离子方程式为.
③向蒸馏塔中通入水蒸气加热,控制温度在90℃左右进行蒸馏的原因是.
-
(3)
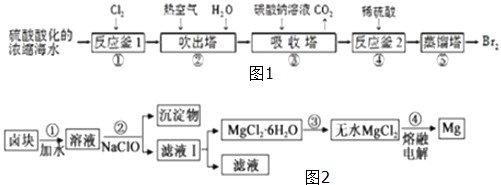
Ⅲ、盐卤蒸发冷却后析出卤块的主要成分是MgCl2 , 此外还含有Fe2+、Fe3+、Mn2+等离子.以卤块为原料制得镁的工艺流程如图2(部分操作和条件已略去):
生成氢氧化物沉淀的pH
物质
开始沉淀
沉淀完全
Fe(OH)3
2.7
3.7
Fe(OH)2
7.6
9.6
Mn(OH)2
8.3
9.8
Mg(OH)2
9.6
11.1
①用NaClO氧化Fe2+得到Fe(OH)3沉淀的离子反应方程式是.
②步骤③需在HCl保护气中加热进行,请用化学平衡移动原理解释原因.
③NaClO还能除去盐卤中的CO(NH2)2 , 生成盐和能参与大气循环的物质,除去0.1molCO(NH2)2时消耗NaClOg.
选项 | 陈述I | 陈述Ⅱ |
A | 铝比铁活泼 | 铝比铁更容易被腐蚀 |
B | HClO具有强氧化性 | HClO有杀菌消毒作用 |
C | 与水反应时,钠浮在水面上 | 钠与水反应是放热反应 |
D | 浓硝酸具有强氧化性 | 浓硝酸能和浓氨水反应产生白烟 |
甲  乙
乙  丙.
丙.
-
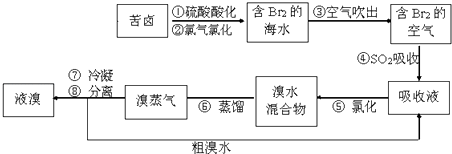
(1) 步骤③的离子方程式: 。
-
(2) 步骤⑤中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是。
-
(3) 溴水混合物Ⅱ中溶有一定量的氯气,因此在步骤⑤中可将蒸馏产生的气体通过(填试剂名称)溶液,以除去氯气。
-
(4) 步骤⑤的蒸馏过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,请解释原因。
-
(1) 已知碘元素最终变为无色HIO3。上述整个过程中的还原剂是。写出CCl4层变成紫色的离子反应方程式。
-
(2) 若把KI换成KBr,则CCl4层变为色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是。
-
(3) 智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘。试配平该反应的化学方程式,并用短线标出电子转移方向及总数NaIO3+NaHSO3→NaHSO4+Na2SO4+I2+( )H2O,已知含氧酸盐的氧化作用随溶液酸性的加强而增强,在制备实验时,定时取样,并用酸化的氯化钡来检测SO42-离子生成的量,发现开始阶段反应速度呈递增的趋势,试简述这变化趋势发生的原因:。
-
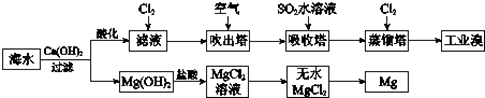
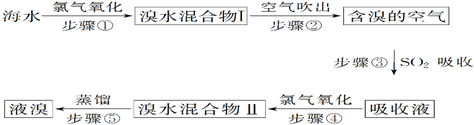
(1) 向苦卤中通入Cl2是为了提取溴,发生反应的离子方程式为。
-
(2) 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2的水溶液将其还原吸收,发生反应的化学方程式为。也可用纯碱吸收溴,主要反应是Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),吸收1 mol Br2时,转移的电子为 mol。
-
(3) 下列有关海水综合利用的说法错误的是____。A . 粗盐可采用除杂和重结晶等过程提纯 B . 电解饱和食盐水可制得金属钠 C . 工业生产常选用Ca(OH)2作为沉淀剂 D . 海水提镁涉及到复分解反应
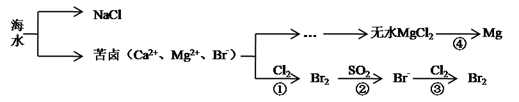
-
(1) 淡化海水的方法有(写一种合理方法即可)。由海水提取的粗盐中含有Ca2+、Mg2+、SO42-等离子,为了除去这些离子,需要依次加入稍过量的NaOH、BaCl2、(填化学式),之后(填操作名称),再加入适量(填试剂名称)。将所得溶液加热浓缩、冷却结晶,得到精盐。
-
(2) 反应④由无水MgCl2制取金属镁的常用工业方法是。
-
(3) 向苦卤中通入Cl2置换出Br2 , 再用空气吹出溴并用SO2吸收,转化为Br- , 反复多次,
以达到富集溴的目的。由海水提溴过程中的反应可得出Cl-、SO2、Br-还原性由强到弱的顺序是。
-
(4) 工业上也可以用Na2CO3溶液吸收吹出的Br2 , 生成溴化钠和溴酸钠,同时放出CO2。写出反应的离子方程式,最后再用H2SO4处理所得溶液重新得到Br2。
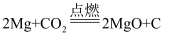 ,下列叙述正确的是( )
,下列叙述正确的是( )
-
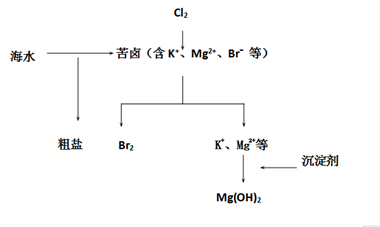
(1) 无需经过化学变化就能从海水中获得的物质是____(填序号)A . Cl2 B . 淡水 C . 烧碱 D . 食盐
-
(2) 从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是。
-
(3) 下图是从海水中提取镁的简单流程。
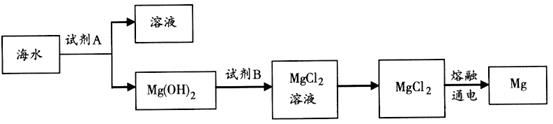
①工业上常用于沉淀Mg2+的试剂A是,转Mg(OH)2化为MgCl2的离子方程式是。
②由无水MgCl2制取Mg的化学方程式是。
-
(4) 海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:
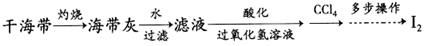
①灼烧海带至灰烬时所用的主要仪器名称是。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式。反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈色。
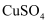 C .
C . 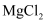 D .
D . 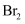
 再通
再通 C . 制取
C . 制取 的反应是利用其溶解度小于NaCl
D . ③④的目的是进行溴的富集
的反应是利用其溶解度小于NaCl
D . ③④的目的是进行溴的富集
- 12.阅读下面文字,完成(1)-(4)题(25分) 马尔克斯,世界上最不孤独的人 陈众议 马尔克斯走了。然而,只要我
- 9.在恒温恒容条件下,能使A(g)+B(g)C(g)+D(g)正反应速率增大的措施是( )A.减小C或D的浓度
- 现有以下物质:①NaCl晶体,②干冰,③液态的醋酸,④铜,⑤BaSO4晶体,⑥蔗糖,⑦酒精,⑧熔融的KNO3。 请回答下
- 如图17所示,是小英的折叠自行车前梁的折叠装置,请说出其中所用到的物理知识(一条即可)
- 为调节水资源的地区分布不均,我同采取的主要措施是 A.修建水库
- 2. Zhou Yang of China won____women's 1500 meters short trac
- 下面各组词语中,加点字读音完全相同的一项是 A.踟躇/踯躅 禁令/情不自禁
- 已知R2+有b个中子,核外有a个电子,表示R原子符号正确的是()
- 如图,⊙O的直径AB与弦CD(不是直径)相交于点E,且CE=DE,过点B作CD得平行线AD延长线于点F.(1)求证:BF
- 如图所示,一小闹钟静止在水平桌面上,则 A.闹钟受到的重力和闹钟对桌面的压力是一对平衡力 B.闹钟受到的重力和桌面对闹钟
- My sister oftenargues me colors. A.with, about
- 阅读下面文章,完成1—4题。 假想金箍棒 麦笛 ①《西游记》中孙悟空从东海龙王那里借了一根“定海神针”,又称“如意金箍棒
- 如图,在△ABC中,AB=AC=26,边BC上的中线AD=24.求BC的长度.
- .香港“上天”(建设高层建筑),“下海”(填海造地)的原因是( )A.建筑水平高
- 如图,已知一次函数的图象与反比例函数的图象交于,两点,且点的横坐标和点的纵坐标都是.求:(1)一次函数解析式;(2)求的
- 已知有机物A分子中含有苯环且只有一个侧链,C中除苯环外还有一个四元环。有机物A的相对分子质量M不超过200,其中氧元素的
- 史学家钱穆指出:“在此制度下,人民优秀分子均有参政之机会,新陈代谢,决无政治上之特权阶级。”钱穆所说的“制度”是( )
- 工业上,煅烧石灰石【CaCO3】可以制得生石灰【CaO】和二氧化碳。如果要制取5.6t氧化钙,需要含碳酸钙80%的石灰石
- 下列关于哺乳动物胚胎发育和胚胎工程的叙述,正确的是 A.卵裂期胚胎中细胞数目和有机物总量在不断增加 B.胚胎分割时需将原
- 动物的1个精原细胞在减数分裂中形成4个四分体,则在减数第二次分裂的中期可能有的染色体数、染色单体数分别是() A.2条、



