第二单元 溶液组成的定量研究 知识点题库
已知0.5 L盐酸和硫酸的混合溶液中含有0.1 mol Cl-和0.2 mol SO42- , 则此溶液中H+的物质的量浓度是:( )
A . 1 mol/L
B . 0.5 mol/L
C . 0.6 mol/L
D . 0.1 mol/L
在标准状况下,将224LHCl气体溶于635mL水(ρ=1.0g•cm﹣3)中,所得盐酸的密度为1.18g•cm﹣3 . 试计算:
①所得盐酸的物质的量浓度为 .
②取出这种盐酸100mL,稀释至1.18L,所得稀盐酸的物质的量浓度为 .
③现用0.1mol•L﹣1的NaOH溶液中和②中盐酸100mL,需要NaOH溶液体积为
实验室用63%的浓HNO3 (其密度为1.4g/mL)配制240mL 0.50mol/L稀HNO3 , 若实验仪器有:A.10mL量筒 B.50mL量筒 C.托盘天平 D.玻璃棒
E.100mL容量瓶 F.250mL容量瓶 G.500mL容量瓶 H.胶头滴管 I.200mL烧杯.
-
(1) 此浓硝酸的物质的量浓度为 mol/L
-
(2) 应量取63%的浓硝酸 mL,应选用.(填仪器的字母编号)
-
(3) 实验时还需选用的仪器有(填序号) D、I、
-
(4) 配制过程中,下列操作会使配制的稀硝酸溶液浓度偏高的是(填序号).
①量取浓硝酸的量筒用蒸馏水洗涤2﹣3次,并把洗涤液转入容量瓶
②容量瓶使用时未干燥
③溶解后未经冷却就移液
④定容时不小心有少量蒸馏水滴到瓶外
⑤定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
-
(5) 容量瓶是一种颈部细长的梨形瓶,由于其颈部细长,所以在向容量瓶中移入液体时,需要一定的耐心和技巧.有人建议将容量瓶的瓶颈改粗,对该建议的正确评价是A . 可以按此建议改进,便于使用容量瓶 B . 不能按此建议改进,因为会降低容量瓶的精确度 C . 不必加粗瓶颈,因为向容量瓶中转移液体时,有少量液体倒出瓶外,不会对溶液的浓度产生太大影响.
实验室配制250mL 0.5mol/L的Na2CO3溶液,有如下操作步骤:①将称量好的Na2CO3固体放入烧杯中,加入适量的蒸馏水溶解;②把①所得溶液小心转入250mL容量瓶中;③继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,小心滴加蒸馏水至溶液凹液面与刻度线相切;④用少量蒸馏水洗涤烧杯2~3次,每次洗涤的液体都小心转入容量瓶中并轻轻摇匀;⑤计算所需Na2CO3固体的质量并用托盘天平称取;⑥塞紧容量瓶的塞子,充分摇匀.回答下列问题:
-
(1) 本实验操作步骤的正确顺序是(填序号).
-
(2) 本实验中除用到容量瓶和烧杯外,还需要用到的玻璃仪器有.
-
(3) 实验中用托盘天平实际称取Na2CO3固体的质量是.
-
(4) 在实验中,若出现如下情况,对所配溶液的浓度有何影响?
未进行操作④,所配溶液的浓度会(填“偏高”、“偏低”或“无影响”,下同);定容时俯视液面,所配溶液的浓度会.
-
(5) 若实验过程中出现如下情况应如何处理?
加蒸馏水时不慎超过了刻度,向容量瓶中转移溶液时,不慎有少量溶液洒在容量瓶外面.
用容量瓶配制一定物质的量浓度的溶液,下列操作会使配制的NaOH溶液浓度偏低的是( )
A . 称量12.5g固体NaOH时,将砝码放在左盘上,NaOH放在右盘上
B . 选用的容量瓶中有少量蒸馏水
C . 定容时俯视刻度线
D . 定容摇匀后,液面下降,又加水至刻度线
用2.4mol/L的H2SO4溶液配制100mL浓度为0.2mol/L的稀H2SO4 , 回答下列问题:
-
(1) 需量取2.4mol/L的H2SO4溶液的体积是 mL.
-
(2) 配制过程有下列几步操作:
A.用10mL量筒量取所需体积的H2SO4溶液,注入烧杯中,用玻璃棒搅拌,使其混合均匀;
B.将蒸馏水加入容量瓶至液面接近刻度线1cm~2cm处;
C.向烧杯中加入约20mL蒸馏水;
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液也转移到容量瓶中;
E.用 胶头滴管加水至刻度线;
F.将烧杯中溶液冷却后,沿玻璃棒转移到容量瓶;
G.盖好瓶塞,反复颠倒摇匀.
以上各步骤操作的先后顺序是(填字母).
-
(3) 取上述所配溶液10mL与足量BaCl2溶液反应,生成白色沉淀0.48g.则该溶液浓度 0.2mol/L(填“大于”“等于”或“小于”)造成此误差的操作可能是.
A.定容时俯视容量瓶;
B.用量筒取2.4mol/LH2SO4溶液时俯视读数;
C.使用容量瓶前未干燥;
D.使用的烧杯和玻璃棒未洗涤彻底;
E.定容时将蒸馏水洒在容量瓶外面.
将50g质量分数为ω1 , 物质的量浓度为C1的浓硫酸沿玻璃棒加入到VmL水中,稀释后得到质量分数为ω2 , 物质的量浓度为C2的稀溶液.下列说法中正确的是( )
A . 若C1=2C2 , 则ω1<2ω2 , V<50Ml
B . 若C1=2C2 , 则ω1<2ω2 , V>50mL
C . 若ω1=2ω2 , 则C1<2C2 , V=50mL
D . 若ω1=2ω2 , 则C1>2C2 , V<50Ml
把2mol/L CuSO4和1mol/L硫酸铁溶液等体积混合(假设混合后溶液的体积等于混合前溶液的体积之和),求混合溶液中C(SO42﹣)═mol/L.
下列关于物质的量浓度表述中正确的是( )
A . 0.3 mol•L﹣1 Na2SO4溶液中含有Na+和  总物质的量为0.9 mol
B . 用1 L水吸收22.4 L氨气所得氨水的浓度是1 mol•L﹣1
C . 50mL 1 mol•L﹣1的KCl溶液和100mL 0.25 mol•L﹣1MgCl2溶液中,Cl﹣的物质的量浓度相等
D . 10℃时0.35 mol•L﹣1的KCl饱和溶液100 mL,蒸发掉5 g水,再冷却到10℃时,它的物质的量浓度仍为0.35 mol•L﹣1
总物质的量为0.9 mol
B . 用1 L水吸收22.4 L氨气所得氨水的浓度是1 mol•L﹣1
C . 50mL 1 mol•L﹣1的KCl溶液和100mL 0.25 mol•L﹣1MgCl2溶液中,Cl﹣的物质的量浓度相等
D . 10℃时0.35 mol•L﹣1的KCl饱和溶液100 mL,蒸发掉5 g水,再冷却到10℃时,它的物质的量浓度仍为0.35 mol•L﹣1
 总物质的量为0.9 mol
B . 用1 L水吸收22.4 L氨气所得氨水的浓度是1 mol•L﹣1
C . 50mL 1 mol•L﹣1的KCl溶液和100mL 0.25 mol•L﹣1MgCl2溶液中,Cl﹣的物质的量浓度相等
D . 10℃时0.35 mol•L﹣1的KCl饱和溶液100 mL,蒸发掉5 g水,再冷却到10℃时,它的物质的量浓度仍为0.35 mol•L﹣1
总物质的量为0.9 mol
B . 用1 L水吸收22.4 L氨气所得氨水的浓度是1 mol•L﹣1
C . 50mL 1 mol•L﹣1的KCl溶液和100mL 0.25 mol•L﹣1MgCl2溶液中,Cl﹣的物质的量浓度相等
D . 10℃时0.35 mol•L﹣1的KCl饱和溶液100 mL,蒸发掉5 g水,再冷却到10℃时,它的物质的量浓度仍为0.35 mol•L﹣1
标准状况下VL氨气溶解在1L水中,所得溶液的密度为ρ g·mL-1 , 质量分数为ω,物质浓度为c mol·L−1 , 则下列关系中正确的是( )
A . c= 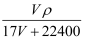 B . ω=
B . ω= 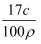 C . ω=
C . ω= 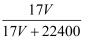 D . ρ=
D . ρ= 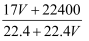
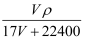 B . ω=
B . ω= 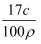 C . ω=
C . ω= 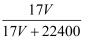 D . ρ=
D . ρ= 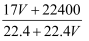
若NA代表阿伏加德罗常数,则下列叙述正确的是( )
A . 1 mol/L的氨水与等质量的水混合后(忽略体积变化),所得溶液浓度大于0.5 mol/L
B . 1 mol Na2O2与足量的水完全反应,转移的电子数为2NA
C . 在标准状况下,22.4 L氢气与22.4 L氦气所含有的原子数均为2NA
D . 28 g乙烯和环丙烷(C3H6)的混合气体含有的原子总数为3NA
使用胆矾(CuSO4·5H2O)配制1L 0.2 mol·L-1的硫酸铜溶液,正确的操作是( )
A . 将胆矾加热除去结晶水后,称取32 g溶解在1 L水里
B . 称取胆矾50 g,溶解在1 L水里
C . 将32 g胆矾溶于水,然后将此溶液稀释至1 L
D . 将50 g胆矾溶于水,然后将此溶液稀释至1 L
用NA代表阿伏加德罗常数的值,下列说法正确的是( )
A . 常温常压下,11. 2 L 二氧化硫气体中含有0. 5NA个SO2分子
B . 标准状况下,22. 4 L CCl4中含有NA个分子
C . 1 mol Na与一定量的O2反应生成Na2O和Na2O2 , 转移的电子数为NA个
D . 将NA个HCl气体分子溶于1 L水中得到1 mol·L-1的盐酸
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A . 2.3gNa与O2完全反应,转移电子总数为0.1NA
B . 常温下,0.2mol/LNH4Cl溶液中,NH4+数目小于0.2NA
C . 标准状况下,11.2LCHCl3中氯原子数目为1.5NA
D . 7.8g苯中碳碳双键的数目为0.3NA
实验室用28g铁粉与足量的稀硫酸反应制取氢气,同时得到125g密度为1.25g/mL的溶液,请计算(写出计算过程):
-
(1) 生成氢气在标准状况下的体积为L?
-
(2) 所得溶液中硫酸亚铁的物质的量浓度为mol/L。
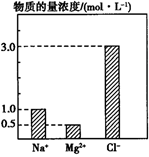
在0.2 L由NaCl溶液、MgCl2溶液、CuCl2溶液组成的混合溶液中,部分离子的浓度如图所示。
-
(1) 混合液中,NaCl的物质的量为mol
-
(2) 混合液中,MgCl2的质量为g。
-
(3) 该混合溶液中CuCl2的物质的量浓度为mol•L﹣1 ,
mgHCl气体溶于水形成 VmL 溶液,密度为 dg•cm-3 , 质量分数为 w %,物质的量浓度为 c mol•L-1。下列表达式正确的是( )
A . n(HCl)= 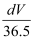 mol
B . c=
mol
B . c= 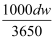 C . w=
C . w= 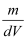 D . V=
D . V= 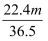
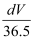 mol
B . c=
mol
B . c= 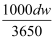 C . w=
C . w= 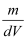 D . V=
D . V= 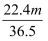
在相同体积、相同物质的量浓度的酸中,必然相等的是( )
A . H+ 的物质的量
B . 溶质的质量分数
C . 溶质的质量
D . 溶质的物质的量
某同学欲用NaOH固体配制480 mL质量分数为25%,密度为1.2 g/mL的溶液。下列叙述错误的是( )
A . 需用托盘天平称量NaOH固体的质量为144 g
B . 容量瓶用蒸馏水洗净后,不必烘干就能用于配制溶液
C . 定容时俯视容量瓶的刻度线,会造成所配溶液的物质的量浓度偏高
D . 未冷却到室温就将溶液转移到容量瓶并定容,会使测定结果偏高
实验室用质量分数为20.0%的盐酸配制250mL0.400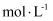 稀盐酸。请填写完整以下实验步骤并回答有关问题:
稀盐酸。请填写完整以下实验步骤并回答有关问题:
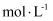 稀盐酸。请填写完整以下实验步骤并回答有关问题:
稀盐酸。请填写完整以下实验步骤并回答有关问题:
-
(1) 步骤1:计算。查得室温下20.0%的盐酸密度为1.095
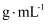 , 则该盐酸的物质的量浓度为
, 则该盐酸的物质的量浓度为 。进而计算得出配制所需20.0%盐酸的体积。
。进而计算得出配制所需20.0%盐酸的体积。
-
(2) 步骤2:称量。本次实验量取盐酸所需量筒规格为mL。
步骤3:稀释。将量取的盐酸倒入烧杯,再倒入适量蒸馏水,静置,待溶液温度恢复至室温。
-
(3) 步骤4:转移、洗涤。将烧杯中的溶液转移到容量瓶需使用引流。用适量蒸馏水洗涤烧杯等仪器,洗涤液转入容量瓶,重复2~3次。容量瓶内液面未达瓶颈前将瓶内溶液混匀。
-
(4) 步骤5:定容、摇匀:加蒸馏水至距离刻度线1~2cm处,平视环形刻度线,改用逐滴加水至凹液面最低处与刻度线相切。摇匀,倒入试剂瓶并贴上标签。
-
(5) 使用容量瓶前必须进行的一步操作是。
-
(6) 在配制过程中,其他操作都符合题意,下列操作会引起浓度偏低的是____(填字母)。A . 容量瓶洗净后未干燥,有蒸馏水残留 B . 量取盐酸后用蒸馏水将量筒内残留盐酸洗出并转入容量瓶 C . 稀释盐酸的烧杯未用蒸馏水洗涤 D . 转移稀释后的盐酸时少量溶液顺着容量瓶口流至瓶外 E . 定容时俯视刻度线 F . 摇匀后发现液面低于刻度线,重新定容至刻度线
最近更新
- 读下图,同答下列问题:(每空1分,共10分)(1)A处地形名称是____ ____,这里目前面临的最突出的环境问
- 某阻值为10欧的定值电阻连在一节新干电池两端,则它两端的电压为 (7) 伏,,通过它的电流是 (8) 安;若把它
- —_____________ has Hong Kong been back to our motherland? —F
- 以下实验操作简便、科学且易成功的是A.将乙醇和乙酸的混合液注入浓硫酸中制备乙酸乙酯B.将铜丝在酒精灯外焰上加热变黑后,再
- 除去括号内的杂质,所选用的试剂或方法不正确的是( ) A.Na2CO3粉末(NaHCO3):加热直至固体质量不再减
- 如图1,在Rt△ABC中,∠C=90°,AC=8m,BC=6m,点P由C点出发以2m/s的速度向终点A匀速移动,同时点Q
- 给出施化肥量对水稻产量影响的试验数据:施化肥量x15202530354045水稻产量y33034536540544545
- 泡菜的制作过程中,许多乳酸菌产生大量乳酸,共同抑制其它菌的生长,乳酸积累过多,又会抑制乳酸菌自身的生长,以上体现出的生物
- 在图中,线框ABCD绕OO′轴以角速度ω匀速转动,穿过线框的磁通量为Φ,产生的感生电动势为E,则下列说法正确的是( )
- 中国人民银行于国家重大节庆日都会发行一些纪念钞,这些纪念钞与同面额人民币等值流通。这说明纪念钞在本质上是 A.商品
- --What did you do _________ Saturday night? --I _________ TV
- 多硫化钠Na2Sx(x>2)在结构上与Na2O2、FeS2、CaC2等有相似之处。Na2Sx在碱性溶液中可被NaClO氧
- Few pleasures can equal ________ of a cool drink on a hot d
- 下列各句中,没有语病的一句是 A.跟随神六太空旅行的12支种苗中,柴油树种苗独占4支,可见搭载太空种苗的北京飞鹰绿色食品
- 小明的爸爸在出版社工作,正在准备出版《齐民要术》这本书。封面上应该写的作者的名字是 A.贾思勰
- 某中学兴趣小组在进行研究性学习中,将两株植物放在封闭的玻璃罩内置于室外,并用经过灭菌的全素营养液进行培养(如甲图所示),
- 中学常见的某反应的化学方程式为(未配平,反应条件略去)。下列叙述不正确的是 ( ) A.若a是铁,b是
- (2013成都高新区摸底)物体沿一直线运动,在t时间内通过的路程为s,它在中间位置s处的速度为v1,在中间时刻t时的速度
- 17、在下面的空格处填入恰当的词语,正确的一项是( ) 要是哈姆莱特在 他自己的心神的时候,做了对不起雷欧提
- 关于声现象,下列说法错误的是:A.一切正在发声的物体都在振动; B.声音在真空中传播的速度最大;



