第二单元 溶液组成的定量研究 知识点题库
a.烧杯 b.1000mL容量瓶 c.500mL容量瓶 d.玻璃棒 e.托盘天平 f.100mL量筒
-
(1) 配制时,必须使用的仪器有(填字母序号),还缺少的仪器是.
-
(2) 该实验两次用到玻璃棒,其作用分别是、.
-
(3) 配制时,一般可分为以下几个步骤:①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却.其正确的操作顺序是.
-
(4) 若使用密度为1.8g/mL、质量分数为98%的浓硫酸,配制1000mL0.18mol/L的稀硫酸,则需浓硫酸的体积是 mL.
-
(1) 实验中必须用到的玻璃仪器有:.
-
(2) 根据计算得知,所需NaOH的质量为 g.
-
(3) 配制时,其正确的操作顺序是(字母表示,每个字母只能用一次);
A.用50mL水洗涤烧杯2﹣3次,洗涤液均注入容量瓶,振荡
B.用托盘天平准确称量取所需的NaOH的质量,倒入烧杯中加入适量水,用玻璃棒慢慢搅动.
C.将已冷却的NaOH溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.加水至离刻度线1~2cm处改用胶头滴管加水,使溶液凹面恰好与刻度相切
-
(4) 下列操作对所配浓度有何影响(填写字母)
偏大的有;
偏小的有;
无影响的有.
A.称量用了生锈的砝码;
B.将NaOH放在纸张上称量;
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中;
D.往容量瓶转移时,有少量液体溅出
E.未洗涤溶解NaOH的烧杯
F.定容时仰视刻度线
G.容量瓶未干燥即用来配制溶液
H.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.
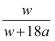 ×100%
B .
×100%
B . 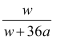 ×100%
C .
×100%
C . 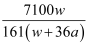 %
D .
%
D . 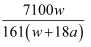 %
%
-
(1) 配制上述溶液需要的玻璃仪器除烧杯和玻璃棒外有。
-
(2) 根据计算,本实验需要用量筒量取浓盐酸的体积为mL。
-
(3) 配制过程有下列几步操作:
A. 将蒸馏水加入容量瓶至液面接近刻度线1~2cm处;
B.量取所需体积的盐酸溶液,注入烧杯中,用玻璃棒搅拌,使其混合均匀;
C.用胶头滴管加水至刻度线;
D.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液也转移到容量瓶中;
E.向烧杯中加入约20mL蒸馏水;
F.待烧杯中溶液冷却后,沿玻璃棒转移到容量瓶中;
G.盖好瓶塞,反复颠倒摇匀,静置,装瓶。
以上各步骤的先后顺序是(填字母),使用容量瓶之前需要进行的一步操作是。
-
(4) 假设配制时其他操作均正确,只出现以下某一情况,试判断所配制的溶液浓度相比于要求的值偏高的是________________A . 容量瓶中有少量蒸馏水 B . 稀释浓HCl时,没有冷却就立即转移到容量瓶中 C . 配制的溶液装入洁净的但有少量蒸馏水的试剂瓶中 D . 定容时俯视
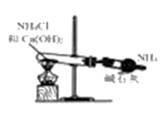 B . 向容量瓶中转移溶液
B . 向容量瓶中转移溶液 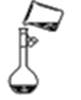 C . 吸收HCl
C . 吸收HCl 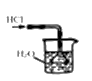 D . 稀释浓硫酸
D . 稀释浓硫酸 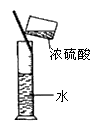
-
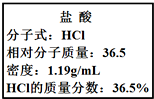
(1) 该浓盐酸的物质的量浓度为mol•L-1。
-
(2) 取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是______。A . 溶液中HCl的物质的量 B . 溶液的浓度 C . 溶液中Cl-的数目 D . 溶液的密度
-
(3) 某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol•L-1的稀盐酸。
①该学生需要量取mL上述浓盐酸进行配制。
②所需的实验仪器有:胶头滴管、烧杯、量筒、玻璃棒,配制稀盐酸时,还缺少的仪器有。
-
(1) 0.5 mol CH4 的质量为g,在标准状况下的体积为L;含个碳原子。
-
(2) 将标准状况下 22.4 L 的 HCl 溶于水配成 200 mL 的溶液,所得溶液的物质的量浓度为mol/L;配制 300 mL 0.5 mol/L 氯化钠溶液,需要 1.5 mol/L 的氯化钠溶液的体积为mL。
-
(3) 1.204×1024 个水分子的物质的量为mol。
①取m g试样A,全部溶于0.5L 2mol·L-1稀硫酸溶液中,放出11.2 L气体(已换算成标准状况),同时生成溶液B;
②另取m g试样A,加入2mol·L-1的NaOH溶液,当加到100mL时,气体不再生成;
③往溶液B中加入2mol/L NaOH,至沉淀不再发生变化。
根据以上过程回答下列问题:
-
(1) 溶液B中是否含有H+(填“是”或“否”);
-
(2) 写出②中发生反应的离子方程式;
-
(3) 下列能表示过程③产生的沉淀质量W与加入NaOH溶液体积V的关系是;
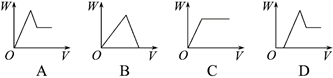
-
(4) m g试样A中含Mg的质量为g;
-
(5) 林同学通过查阅资料,发现浓硫酸与铝发生钝化,但与Mg能剧烈反应生成SO2 , 如果忽略钝化的反应过程,可以通过测定浓硫酸与固体试样反应产生的气体体积,来确定混合物A中镁的质量分数。
郭同学认为林同学的方案可行,但考虑到如果反应结束后硫酸未保持“浓”的状态,测定结果会(填“偏大”、“偏小”或“不变”),其依据是。
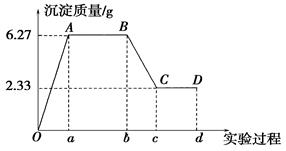
注明:Ob段表示滴加硝酸钡溶液;bd段表示滴加稀硝酸
-
(1) 水样中一定含有的阴离子是,其物质的量浓度之比为。
-
(2) 写出BC段所表示反应的离子方程式:。
-
(3) 由B点到C点变化过程中消耗硝酸的体积为。
-
(4) 试根据实验结果推断K+是否存在?(填“是”或“否”);若存在,K+的物质的量浓度c(K+)的范围是。(若K+不存在,则不必回答该问)
-
(5) 设计简单实验验证原水样中可能存在的离子:。(写出实验步骤、现象和结论)
 为阿伏加德罗常数的值,下列说法正确的是( )
为阿伏加德罗常数的值,下列说法正确的是( )
 溶液中含
溶液中含  数为
数为  D . 密闭容器中
D . 密闭容器中 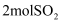 与
与 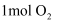 反应,生成
反应,生成 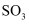 的分子数为
的分子数为 
-
(1) 49g的H2SO4能与mol NaOH恰好完全反应。
-
(2) 在一定的温度和压强下,1体积气体X2跟2体积气体Y2化合生成2体积化合物,则该化合物的化学式是。
-
(3) 1mol H2O所含电子个数为:;
-
(4) 现有mg某X2气体,它的摩尔质量为M g/mol,则:
①该气体的物质的量为mol。
②一个X原子的质量g。
③该气体在标准状况下的体积为L。
④相同温度与压强下,若X2与氮气以体积比1:4混合,该混合气体相对氢气密度为14.4,X2的相对分子质量为。
⑤若标况下X2的密度为1.25 g/L,X原子最外层有个电子。
①稀硫酸 ②小苏打 ③水玻璃 ④二氧化碳 ⑤Na ⑥NaOH溶液 ⑦Na2O2 ⑧Al
-
(1) 上述物质中有两种物质在水溶液中反应的离子方程式为:H++OH-=H2O,这两种物质的序号是(填序号)。
-
(2) 上述物质中有两种物质可用于呼吸面具或潜水艇中制备氧气,该反应的化学方程式是。
-
(3) 上述物质中既能与HCl又能跟NaOH反应的物质是(填序号)。
-
(4) 向③中通入CO2 , 会出现软而透明的凝胶胶体,其化学方程式是。
-
(5) ②可用于治疗胃酸过多,其原理是(用离子方程式表示)。
-
(6) ⑤需密封保存,其中一个目的是与水隔离,原因是(用化学方程式表示)。
-
(7) 用18.4 mol/L的浓硫酸配制500 mL 0.5mol/L的①,所需主要仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要,定容时由于仰视刻度线,则对所配溶液浓度产生的影响为(填“偏大”、“偏小”或“无影响”)。
- He looked around and caught a man ______ his hand into the p
- 哺乳动物如牛、羊等是人类生活中一种重要的肉制品、皮毛制品的原料来源,但哺乳动物妊娠时间长,每胎产子数少、繁殖速度比较慢。
- 在做“绿叶中色素的提取和分离”实验时,甲、乙、丙、丁四位同学对相关试剂的使用情况如下表所示(“+”表示使用,“-”表示未
- 2014年9月18日,中国非公有制经济发展论坛在宁夏银川开幕,本届论坛的主题是: 全面深化改革,激发非公经济活力,促进西
- 图示圆圈为台风系统,该系统分成四个区域,短箭头表示风,长箭头表示台风整体移动方向,回答1~2题。1.当你假期坐船旅行,不
- 下图为极地俯视图,据此回答(1)~(2)题。 (1)甲处风带的风向为 A.西北 B.东南 C.西南
- 通过宇宙飞船搭载生物材料进行生命科学研究,不仅有助于揭示生命的本质,而且可以培育一些新品种。请依据所学知识回答相关问题:
- 关于电子秤中应变式力传感器的说法 正确的是( ) A.应变片多用半导体材料制成. B.当应变片的表面拉伸时,其电
- 两个相似三角形的面积分别为64和36,则它们周长的比是______.
- 等物质的量的CO和CO2中所含O原子个数之比 ,C原子数之比 ,二者的质量之比
- (04年全国卷Ⅱ)一定量的气体吸收热量,体积膨胀并对外做功,则此过程的末态与初态相比, A.气体内能一定增加
- 名著阅读 与语言运用 (3分)选取《西游记》《水浒》《童年》《鲁滨逊漂流记》《钢铁是怎样炼成的》这五部名著中的人物和相关
- 下图是一个健康人原尿流经肾小管形成尿液的过程中某种物质A.水 B.无机盐
- 节能减排、低碳出行是我们倡导的生活方式.下列有关二氧化碳的说法正确的是() A.二氧化碳通入紫色石蕊溶液中,溶液变为红色
- 3.6g CaCO3高温煅烧一段时间后,冷却,测得剩余固体中含钙元素57.6%,求剩余固体中CaO的质量.
- 进化论作为一种科学理论,至迟在19世纪80年代已被初步介绍到中国,但其仅仅是众多科学理论之一种,并没有得到中国知识界的特
- 函数的单调增区间与值域相同,则实数的取值为 ( ) A. B.
- One of my close friends made great progress in her studies s
- He looked quite healthy though he was __________.A. in seven
- 若曲线上点处的切线平行于直线,则点的坐标是________.



