实验活动1 配制一定物质的量浓度的溶液 知识点题库
-
(1) 配制250mL0.1mol/L的盐酸溶液需要 ml容量瓶.还需要,,.(仪器)
-
(2) 配制时,其正确的操作顺序是计算称量溶解 转移定容摇匀装瓶.
-
(3) 若出现如下情况,对所配溶液浓度将有何影响?加蒸馏水时不慎超过了刻度;定容时俯视未冷却.
-
(1) 配制0.5 mol/L的硫酸溶液450 mL,需用量筒量取质量分数98%、密度1.84 g/cm3的浓硫酸的体积为mL,如果实验室有10 mL、25mL、50 mL 量筒,应最好选用mL量筒。
-
(2) 配制上述溶液,除用到量筒、烧杯、玻璃棒外,还需要的两种玻璃仪器是 ,。
-
(3) 请说出本实验中玻璃棒的作用: , 。
-
(4) 下面操作造成所配稀硫酸溶液浓度偏高的是________(填序号)。A . 浓硫酸稀释后溶液没有冷却到室温就转移 B . 容量瓶中原有少量蒸馏水 C . 向容量瓶加水定容时眼睛俯视液面 D . 定容时加水超过刻度线,立即用滴管吸出多余液体
-
(1) 该实验所需的玻璃仪器:、玻璃棒、烧杯、胶头滴管、量筒。
-
(2) 所需浓硫酸的体积是,量取浓硫酸所用的量筒的规格是(规格从下列中选用 A.10mL B.20mL C.50mL D.100mL)
-
(3) 第⑤步定容的具体实验操作是。
-
(4) 下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
A.容量瓶用蒸馏水洗涤后残留有少量的水。
B.转移溶液前未冷却至室温。
C.定容时仰视溶液的凹液面。
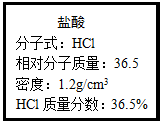
-
(1) 该浓盐酸的物质的量浓度为
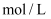 .
.
-
(2) 取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 ______ .A . 溶液中HCl的物质的量 B . 溶液的浓度 C . 溶液中Cl-的数目 D . 溶液的密度
-
(3) 某学生欲用上述浓盐酸和蒸馏水配制450mL物质的量浓度为
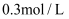 稀盐酸.
稀盐酸.  该学生需要量取 mL上述浓盐酸进行配制.
该学生需要量取 mL上述浓盐酸进行配制.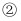 配制时,其正确的操作顺序是
配制时,其正确的操作顺序是  用字母表示,每个字母只能用一次
用字母表示,每个字母只能用一次  ;
;A.用30mL水洗涤烧杯
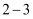 次,洗涤液均注入容量瓶,振荡
次,洗涤液均注入容量瓶,振荡B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水
 约
约 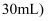 的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
的烧杯中,用玻璃棒慢慢搅动,使其混合均匀C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线
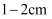 处
处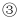 在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?  填“偏高”或“偏低”或“无影响”
填“偏高”或“偏低”或“无影响”  .
.I、用量筒量取浓盐酸时俯视观察凹液面
II、用量筒量取浓盐酸后,洗涤量筒
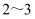 次,洗涤液也转移到容量瓶
次,洗涤液也转移到容量瓶 III、溶液注入容量瓶前没有恢复到室温就进行定容
-
(4) 若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为d
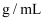 ,则此溶液的物质的量浓度为 ______
,则此溶液的物质的量浓度为 ______ 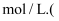 填字母
填字母  A .
A .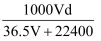 B .
B . 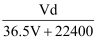 C .
C . 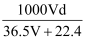 D .
D . 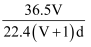
-
(1) 98 %的浓硫酸的物质的量浓度为。
-
(2) 现有下列几种规格的量筒,应选用(填序号)。
①5 mL量筒 ②10 mL量筒 ③50 mL量筒 ④100 mL量筒
-
(3) 实验需要以下步骤:
①定容②量取③摇匀④洗涤⑤转移⑥冷却⑦计算⑧装瓶⑨稀释进行顺序为。
-
(4) 下列操作使所配溶液的物质的量浓度偏高的是__________。A . 往容量瓶中转移溶液时有少量液体溅出 B . 未洗涤稀释浓H2SO4的小烧杯 C . 定容时俯视刻度线 D . 洗净容量瓶未干燥即用来配制溶液 E . 定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
|
84消毒液 [有效成分] NaClO [规格] 1000mL [质量分数] 25% [密度] 1.192g·cm-3 |
回答下列问题:
-
(1) 工业上常用氯气与烧碱溶液反应制取84消毒液,写出反应的离子方程式。
-
(2) 84消毒液使用时需要稀释。某化学实验小组用上述84消毒液配制480mL0.2mol·L-1的稀溶液。
①量取84消毒液mL。
②洗涤时需要将仪器(填名称)洗涤2~3次。
③定容时加蒸馏水不慎超过了刻度线,此时应采取的处理方法是;该小组同学用量筒量取84消毒液时,仰视观察液面,所配溶液的浓度会(填“偏高”、“偏低”或“无影响")。
-
(3) 向84消毒液中加入少量稀硫酸可以增强漂白消毒效果,请解释其原因(用化学方程式回答)。
-
(1) Ⅰ下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题。
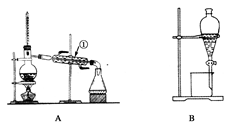
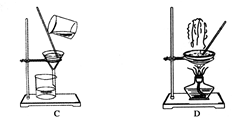
装置A中①的名称是,进水的方向是从(填“上”或“下”)口进水。
-
(2) 装置B在分液时为使液体顺利下滴,应进行的具体操作是。
-
(3) 从碘水中分离出I2 , 选择装置,该分离方法的名称为。
-
(4) 装置C和装置D中玻璃棒的作用分别是,。
-
(5) Ⅱ用提纯后的NaCl固体配制100mL1.0mol/LNaCl溶液,所用仪器除托盘天平、烧杯、玻璃棒、药匙、量筒外,还需要(填仪器名称)。其操作步骤如乙图所示,则甲图操作应在乙图中的(填选项字母)之间。
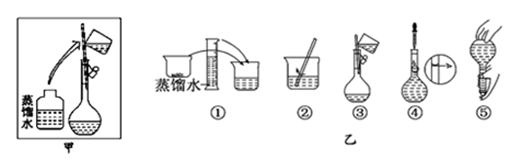
A.①与② B.②与③ C.③与④ D.④与⑤
配制NaCl(精盐)溶液时,若出现下列操作,造成结果偏低的是
A.称量时NaCl已潮解 B.天平的砝码已锈蚀
C.定容摇匀时,液面下降又加水 D.定容时俯视刻度线
-
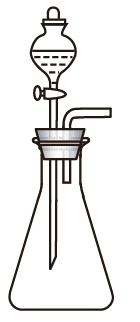
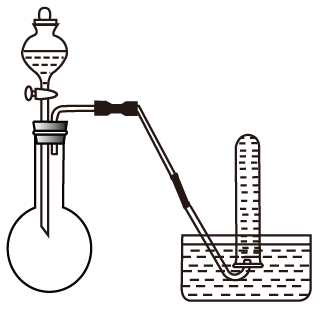
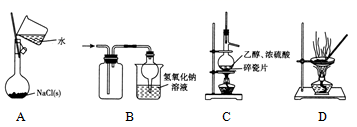
(1) I.[二氧化硫制备]
实验室一般采用亚硫酸钠固体与硫酸(浓硫酸与水1:1混合)反应制取二氧化硫:
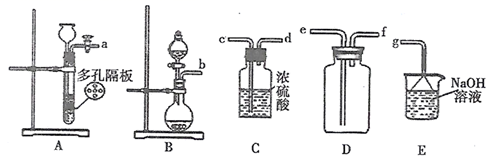
欲收集瓶干燥的二氧化硫,选择上图中的装置,其最佳连接顺序为: (按气流方向,用小写字母表示)。
-
(2) II. [实验探究]
实验:向盛有2 ml 0.1mol/L Ba(NO3)2溶液的试管中,缓慢通入SO2气体,试管内有白色沉淀产生。
配制0.1mo/L Ba(NO3)2溶液出现如下情况应如何处理?
①加蒸馏水到离刻度线1cm~2cm处时:。
②加蒸馏水时不慎超过了刻度线,应:。
-
(3) 配制0.1 mol/L Ba( NO3)2溶液时所用蒸馏水必须先除去溶液中溶解的氧气,具体方法是。
-
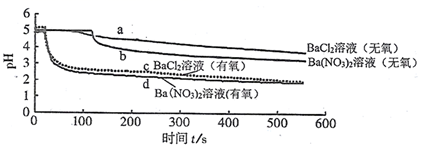
(4) 将SO2分别通入无氧、有氧且浓度均为0.1 mol·L-1的BaCl2溶液和Ba(NO3)2溶液中,探究NO
 和O2哪种微粒起到了主要氧化作用,实验记录如下:
和O2哪种微粒起到了主要氧化作用,实验记录如下:
实验记录
pH变化
溶液中是否产生沉淀
BaCl2溶液(无氧)中无白色沉淀、BaCl2溶液(有氧)中有白色沉淀Ba(NO3)2溶液(无氧)中有白色沉淀、Ba(NO3)2溶液(有氧)中有白色沉淀
曲线a所示溶液pH降低的原因(用化学用语作答),曲线c所示溶液中所发生的离子反应方程式为,曲线d(填“能”或“不能”)说明NO
 是氧化SO2 , 的主要微粒,其理由是。
是氧化SO2 , 的主要微粒,其理由是。
选项 | A | B | C | D |
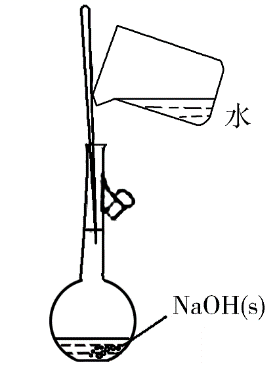
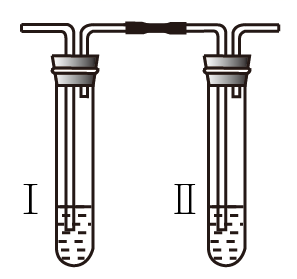
实验目的 | 制备Cl2 | 制备并收集NO | 配制0.10 | 检验CO2中混有的CH4 |
实验试剂 | 浓盐酸和二氧化锰 | Cu和稀硝酸 | 水和NaOH(s) | I中澄清石灰水,II中溴水 |
实验装置 |
|
|
|
|
 消毒液,下列操作导致所配溶液浓度偏高的是( )
消毒液,下列操作导致所配溶液浓度偏高的是( )
 固体受潮
B . 溶解搅拌时有液体溅出
C . 定容时俯视容量瓶刻度线
D . 摇匀后见液面下降,再加水至刻度线
固体受潮
B . 溶解搅拌时有液体溅出
C . 定容时俯视容量瓶刻度线
D . 摇匀后见液面下降,再加水至刻度线
 与浓盐酸反应制备
与浓盐酸反应制备 (发生装如下图所示).
(发生装如下图所示).
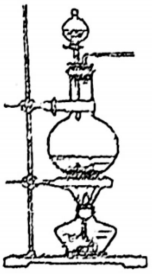
-
(1) 制备实验开始时,先检查装置气密性,接下来的操作依次是(填序号)
A.往烧瓶中加入 粉末 B.加热 C.往烧瓶中加入浓盐酸
粉末 B.加热 C.往烧瓶中加入浓盐酸
-
(2) 制备反应会因盐酸浓度下降而停止.
为测定反应残余清液中盐酸的浓度,探究小组同学提出下列实验方案:
甲方案:与足量
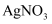 溶液反应,称量生成的AgCl质量.
溶液反应,称量生成的AgCl质量.乙方案:采用酸碱中和滴定法测定.
丙方案:与足量Zn反应,测量生成的
 体积.
体积.继而进行下列判断和实验:
①判定甲方案不可行,理由是.
②进行乙方案实验:
a.使用移液管准确量取残余清液10.00mL,稀释至100mL作为试样,稀释时需用到的玻璃仪器有烧杯、量筒、玻璃棒、、.
b.量取试样20.00mL,用
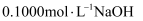 标准溶液滴定,HCl恰好完全反应时,消耗22.00mLNaOH标准溶液,可计算得残余清液中盐酸浓度为
标准溶液滴定,HCl恰好完全反应时,消耗22.00mLNaOH标准溶液,可计算得残余清液中盐酸浓度为 (结果保留四位有效数字)
(结果保留四位有效数字)c.平行滴定后获得实验结果.
③进行丙方案实验:装置如图所示(夹持器具己略去).
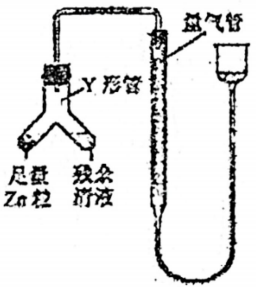
(i)使Y形管中的残余清液与锌粒反应的正确操作是将转移到中.
(ii)反应完毕,每间隔1分钟读取气体体积,气体体积逐次减小,直至不变.气体体积逐次减小的原因是(排除仪器和实验操作的影响因素).
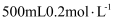 的稀
的稀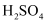 。请回答下列问题:
。请回答下列问题:
-
(1) 实验室欲用98%的浓
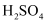 (密度为
(密度为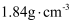 )来配制,经计算需要mL(保留一位小数)浓硫酸,在量取时宜选用下列量筒中的。
)来配制,经计算需要mL(保留一位小数)浓硫酸,在量取时宜选用下列量筒中的。A.5mL B.10mL C.25mL D.50mL
-
(2) 实验中所用的玻璃仪器除烧杯、玻璃棒、量筒、胶头滴管外还有。
-
(3) 在量取浓硫酸后,进行了下列操作:
①等稀释的硫酸的温度与室温一致后,沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水至液面离容量瓶刻度线1~2cm时,改用胶头滴管加蒸馏水,使溶液的液面与瓶颈的刻度标线相切。
③将量取的浓硫酸稀释。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)。第③步中稀释浓硫酸的操作是。
-
(4) 下列哪些操作会引起所配溶液浓度偏大____(填写字母)。A . 容量瓶底部有蒸馏水未干燥即用来配制溶液 B . 硫酸在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容 C . 往容量瓶转移时,有少量液体溅出 D . 在容量瓶中定容时俯视刻度线 E . 定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
- 下列各图中不正确的是
- 改革开放后,我国对世界的看法由战争与革命转变为和平与发展,其根本原因是 A.党和政府正确分析了当今世界向多极化发展的趋势
- It was the quality of life in the future I to
- 京广铁路和陇海铁路交汇的铁路枢纽是 A.株洲 B.郑州 C.武汉 D.徐州
- 升降利率是央行调节经济的重要手段。中国人民银行降低存款准备金率和存贷款基准利率,有利于 ( )
- 下列烃中,一氯代物的同分异构体数目相同的是 ①邻二甲苯 ②间二甲苯 ③对二甲苯
- ,自缘身在最高层。(《登飞来峰》)
- 中国是世界上最早研究和生产合金的国家之一。 ①在原子反应堆中得以广泛应用的钠钾合金在常温下呈液态,说明合金的熔点比其成分
- 某元素最高价氧化物对应水化物的化学式是H2XO4,这种元素的气态氢化物的化学式为A、HX B、H2
- 下列试剂保存时,不用棕色试剂瓶的是() A.氯水 B.溴化银 C.碘化
- 在动摩擦因数m=0.2的粗糙绝缘足够长的水平滑漕中,长为2L的绝缘轻质细杆两端各连接一个质量均为m的带电小球A和B,如图
- 如图①是一个长为2a,宽为2b的长方形,沿图中虚线剪开,将其分成4个小长方形,然后按图②的形状拼成一个正方形。1、图②中
- -2016的倒数是( ) A.-2016 B.- C. D.2016
- 地震主要是内力作用形成的地质灾害。
- Iraq has _______ too many wars since 1990s, making his peop
- 建国后,各种运动不断,这在当时人们取名中留下深刻的印记。例如:王建国、向小康、李文革、周跃进等。如果这四人按年龄从大到小
- 近年来,土地问题日益受到我国政府和社会各界的关注,也成为2010年两会上的热点问题。读我国某省土地资源构成和利用结构图,
- 下列各组物质中,都是共价化合物的是() A. H2S和Na2O2 B. H2O2和CaF2 C. NH3和N2 D. H
- He wanted __________ help raise money ________ Project Gree
- 问:怎么判断两个相对静止的物体之间有没有静摩擦力?