实验活动1 配制一定物质的量浓度的溶液 知识点题库
 c(Na+)=c(SO
c(Na+)=c(SO 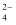 ),则其溶质可能是( )
),则其溶质可能是( )
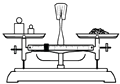 称量
B .
称量
B . 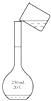 转移
D .
转移
D . -
(1) 选用的主要仪器有:①,②,③,④,⑤.
-
(2) 现有下列配制操作:
A.用量筒量取浓H2SO4
B.反复颠倒摇匀
C.用胶头滴管加水至刻度线
D.洗涤烧杯和玻璃棒2﹣3次,并洗涤液也转移到容量瓶中,振荡摇匀
E.稀释浓H2SO4
F.将溶液转入容量瓶
正确的操作顺序为:
-
(3) 简要回答下列问题:
①所需浓硫酸的体积为mL.
②如果实验室有15mL、20mL、50mL的量筒,应选用mL的量筒最好,量取时发现量筒不干净,用水洗净后直接量取,将使配制的浓度(偏高、偏低、无影响).
③取配制好溶液100ml,加水稀释到500ml,此时溶液中H+ 的物质的量浓度是.
-
(1) 配制该溶液的实验步骤包括:
a.计算需要氢氧化钠固体的质量;
b.称量氢氧化钠固体;
c.将烧杯中的溶液注入容量瓶中,洗涤烧杯和玻璃棒,将洗涤液全部转移入容量瓶中;
d.用适量的蒸馏水溶解称量好的氢氧化钠固体,冷却;
e.盖好瓶塞,反复上下颠倒,摇匀;
f.继续向容量瓶中加蒸馏水至刻度线下1~2cm时,改用滴加蒸馏水至凹液面与刻度线相切。
上述步骤的正确操作顺序是。
-
(2) 使用mL的容量瓶配制此溶液,需要称量NaOH固体的质量为g。
-
(3) 下列操作会使所配制溶液浓度偏大的有________。A . 容量瓶中原有少量蒸馏水 B . 转移溶液时,没有洗涤玻璃棒和溶解用的烧杯 C . 定容摇匀后,静置时发现液面低于刻度线,又加水至刻度线 D . 定容时,俯视观察液面
①容量瓶是配制一定物质的量浓度的溶液的专用仪器 ②容量瓶使用前要先检查容量瓶是否漏液 ③容量瓶可以用来加热 ④容量瓶不能用长期贮存配制好的溶液 ⑤一定要用500mL容量瓶配制250mL溶液
-
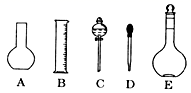
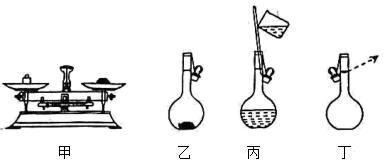
(1) 如图所示的仪器中配制溶液肯定不需要的是 (填字母),配制上述溶液还需用到的玻璃仪器是(填仪器名称)。
-
(2) 容量瓶上标有以下5项中的(填序号)
①压强 ②温度 ③容量 ④浓度 ⑤刻度线
-
(3) 在配制过程中,下列操作使所配溶液浓度偏大的是 .
①未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
②定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
③定容时,仰视刻度线
④使用容量瓶前用蒸馏水洗涤且没干燥
-
(4) 计算实验室配制上述溶液需用量筒量取质量分数为98%、密度为1.84g/mL的浓硫酸的体积为:mL。(保留小数点后一位)
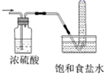
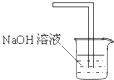
| A.配制一定物质的量浓度的溶液 | B.排去碱式滴定管内的气泡 | C.收集纯净的氯气 | D.吸收尾气中的SO2 |
| | | | |
 B .
B .  D .
D . 
-
(1) 兴趣小组成员根据已有认知模型提出以下猜测:
猜测1:钠分别与水、盐酸反应,由于,钠与盐酸反应更快。
猜测2:钠分别与乙醇、醋酸反应,由于醋酸,钠与醋酸反应更快。
-
(2) 设计实验进行“证实与证伪”
实验I配制一定浓度的HCl
①用12.00mol·L-1HCl配制0.50mol·L-1HCl和5.00mol·L-1HCl时,除用到烧杯、胶头滴管、玻璃棒外,还必须用到下列仪器中的(写对应字母)。
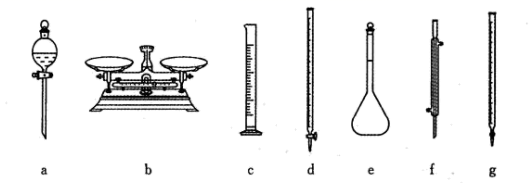
②配制0.50mol·L-1HCl250mL,需要取用12.00mol·L-1浓盐酸的体积为。
实验II相同温度下,比较钠与水、0.50mol·L-1HCl、5.00mol·L-1HCl反应的快慢
序号
钠块(形状几乎相同)
反应液体(50mL)
钠块消失时间
Ⅰ
0.15g
水
Ⅱ<Ⅰ<Ⅲ
Ⅱ
0.15g
0.50mol·L-1HCl
Ⅲ
0.15g
5.00mol·L-1HCl
该小组查阅资料知,相同温度下,影响钠与盐酸反应速率的主要因素是c(H+)和钠表面的c(Na+)。
③钠与5.00mol·L-1HCl反应,速率最慢的原因可能是。
实验II相同温度下,比较钠与乙醇、醋酸反应的快慢
序号
钠块(形状几乎相同)
反应液体(50mL)
反应现象
钠块消失时间
ⅳ
0.15g
乙醇
钠沉在烧杯底部,产生气泡较快
ⅳ<ⅴ
ⅴ
0.15g
冰醋酸
钠浮在液体表面,产生气泡较慢
④该小组某同学提出,依据化学实验的控制变量思想,该实验设计存在缺陷,该缺陷是。
⑤请你帮助该小组设计新的方案,对上述实验进行改进。
实验结论:
⑥通过实验探究,该小组同学认为钠与醋酸反应比钠与乙醇反应慢,原因可能是。
A.冰醋酸是无水乙酸,无水情况下难以电离出氢离子
B.乙醇钠在乙醇中的溶解度大于乙酸钠在乙酸中的溶解度
C.乙酸羧基中的氢原子比乙醇羟基中的氢原子更难电离出氢离子
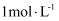
 溶液,下列叙述正确的是( )
溶液,下列叙述正确的是( )
 B . 待
B . 待  全部溶解后应立即将溶液转移至容量瓶中
C . 定容时若俯视刻度线观察液面,会使所配制的
全部溶解后应立即将溶液转移至容量瓶中
C . 定容时若俯视刻度线观察液面,会使所配制的  溶液的浓度偏高
D . 摇匀后发现液面略低于刻度线,应再加水到达刻度线
溶液的浓度偏高
D . 摇匀后发现液面略低于刻度线,应再加水到达刻度线
-
(1) K2Cr2O7是常用的氧化还原滴定试剂。滴定时应将K2Cr2O7溶液加入(填“酸式”或“碱式”)滴定管中;在规格为25mL的滴定管中,若K2Cr2O7溶液起始读数是5.00mL,此时滴定管中K2Cr2O7的实际体积为(填序号)。
A.1.5mL B.20mL C.大于20mL D.小于20mL
-
(2) 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验。请完成下列填空:
①由NaOH固体配制0.10mol/LNaOH标准溶液,需要的仪器有药匙、玻璃棒、(从图中选择,写出名称)。
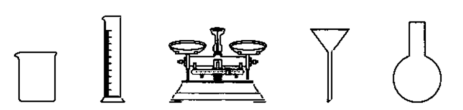
②取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如表:
实验编号
NaOH溶液的浓度(mol/L)
滴定完成时,NaOH溶液滴入的体积(mL)
待测盐酸溶液的体积
(mL)
1
0.10
22.62
20.00
2
0.10
22.72
20.00
3
0.10
22.80
20.00
滴定达到终点的标志是。根据上述数据,可计算出该盐酸的浓度约为(保留两位有效数字)。
③用NaOH标准溶液滴定未知浓度的盐酸时,下列各操作中无误差的是(填序号)。
A.用蒸馏水洗净碱式滴定管后,注入NaOH标准溶液进行滴定
B.用蒸馏水洗涤锥形瓶后,再用待测盐酸润洗,而后装入一定体积的盐酸溶液进行滴定
C.用酸式滴定管量取10.00mL稀盐酸放入用蒸馏水洗涤后的锥形瓶中,再加入适量蒸馏水和几滴酚酞后进行滴定
D.滴定完毕读数后发现滴定管尖嘴还残余1滴液体
- 用一种试剂就可以将NaOH、NH4SCN、AgNO3、Na2SO4四种无色溶液一一鉴别出来,这种试剂是 A、溴
- 在25 OC,1.01×105Pa条件下,反应2N2O5(g)===4NO2(g)+O2(g) △H=+56.7kJ/m
- “低碳”已成为人们的一种生活理念,下列做法中不符合这一理念的是( )A.植树造林,严禁乱砍滥伐森林B.在生产和生活
- (本题共12分)以海水中常见物质A为原料可以发展很多种工业,下图中包含了中学课本中介绍的几种基本工业生产,请根据物质之间
- 阅读下面文字,完成1—4题。 “伟大的中国小说”,这是一个建设性和挑战性兼而有之的话题。它的建设性是要树立
- 经过30多年的发展,我国形成了 的对外开放格局。( ) A.多方位、多领域、多层次
- 下面句子措辞得当的一句是( ) A.惊悉家父仙逝,足下不胜哀伤,特致沉痛哀悼。 B.
- She always likes to ____ her beauty in public. A. come in
- 某有机物的蒸气完全燃烧时需要3倍于其体积的氧气,产生2倍于其体积的CO2,该有机物可能是( ) A.CH3CH3
- 下列关于细胞结构和功能及细胞分裂有关的叙述,正确的是( )A.线粒体是细胞有氧呼吸的主要场所,其内氧气的浓度一般比细
- 设NA 表示阿伏加德罗常数的值。下列说法正确的是 A.标准状况下,0.1 mol Cl2 溶于足量水,转移的电子数目为0
- 20.补写出下列句子中的空缺部分。 (1)此恨绵绵无绝期。(白居易《长恨歌》) (2)李煜《虞美人》中“,”两句,暗含着
- 某城市计划建设一个化工厂,下面四种布局方案较合理的是( )
- 作为新中国成立60周年庆祝活动的一部分,中央组织33位在延安工作过的老同志“重返延安”,重返他们魂牵梦萦的精神家园。对此
- 2010年,海地、智利相继发生强烈地震。损失严重。地震发生后,联合国各机构立即全力开展工作。中国政府迅速做出反应,跨越遥
- 没食子酸丙酯(简称PG)是脂溶性食品抗氧化剂,其结构简式如图:下列有关说法不正确的是 A.没食子酸的分子式为C10H12
- The doctor was _______ immediately the little boy fell off a
- 假如你要探究法国资产阶级革命初期反对君主专制和封建等级制度的思想,最值得参考的历史文献是 A.《人权宣言》
- 蚌埠市是安徽省下辖的一个地级市,位于华北平原南端京沪铁路和淮南铁路的交会点。蚌埠市现代花卉科技产业园,集花卉研发、生产、
- 和谐文化是以和谐为思想内涵、以文化为表现形式的一种文化系统。我们建设和谐文化,是因为 A. 和谐文化就是关注人与人之间