2.3 从海水中提取溴和碘 知识点题库
下列变化过程中,需要加入氧化剂的是( )
A . HCl→H2
B . HCl→FeCl2
C . H2SO4→SO2
D . Fe→Fe2O3
将6.50g锌投入200mL某浓度的盐酸中制取H2 , 锌和盐酸均恰好完全反应.求:
-
(1) 6.50g锌的物质的量
-
(2) 所用盐酸中HCl中的物质的量浓度
-
(3) 反应中生成的H2在标准状况下所占的体积.
下列物质均有漂白性,其中漂白原理与另外三种不同的是( )
A . 二氧化硫
B . 氯水
C . 过氧化钠
D . 浓硝酸
用氯气制漂白粉的主要目的是( )
A . 提高氯的质量分数
B . 增强漂白能力
C . 转变为很易溶于水的物质
D . 转变为较稳定,便于贮存的物质
已知:
①KMnO4+HCl(浓)→KCl+MnCl2+Cl2↑+H2O(未配平)
②检验Mn2+的存在:5S2O82﹣+2Mn2++8H2O=10SO42﹣+2MnO4﹣+16H+
下列说法中错误的是( )
A . S2O82﹣离子中存在一个过氧键(﹣O﹣O﹣),则S2O82﹣离子中硫元素的化合价为+6
B . 反应②若有0.1mol还原剂被氧化,则转移电子0.5mol
C . K2S2O8与浓盐酸混合可得到黄绿色气体
D . 反应①配平后还原剂与还原产物之比为8:1
X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等,X、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构.下列说法正确的是( )
A . 原子半径:Z>Y>X
B . Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点
C . CaY2与水发生氧化还原反应时,CaY2只作氧化剂
D . CaX2、CaY2和CaZ2等3种化合物中,阳离子与阴离子个数比均为1:2
下列物质常用作还原剂的是( )
A . 氢气
B . 硝酸
C . 氯气
D . 高锰酸钾
在下列反应中,水只作氧化剂的是( )
A . 2F2+2H2O═4HF+O2
B . 2Na+2H2O═2NaOH+H2↑
C . CaO+H2O═Ca(OH)2
D . 2H2O  2H2↑+O2↑
2H2↑+O2↑
 2H2↑+O2↑
2H2↑+O2↑
氧化还原反应发生在同种元素之间的是( )
A . Zn+2HCl═ZnCl2+H2↑
B . 2H2S+SO2═3S+2H2O
C . H2+CuO═Cu+H2O
D . 2H2O  2H2↑+O2↑
2H2↑+O2↑
 2H2↑+O2↑
2H2↑+O2↑
现有下列十种物质:
①H2②铝③CaO④CO2⑤H2SO4⑥Ba(OH)2⑦红褐色的氢氧化铁液体⑧氨水⑨稀硝酸⑩Al2(SO4)3
-
(1) 上述各物质按物质的分类方法填写表格的空白处(填物质编号):
分类标准
金属单质
氧化物
溶液
胶体
电解质
属于该类的物质
-
(2) 上述十种物质中有两种物质之间可发生离子反应:H++OH﹣═H2O,该离子反应对应的化学方程式为.
-
(3) ⑩在水中的电离方程式为,
-
(4) 少量的④通入⑥的溶液中反应的离子方程式为.
-
(5) ②与⑨发生反应的化学方程式为:Al+4HNO3═Al(NO3)3+NO↑+2H2O,该反应的氧化剂是(填化学式),氧化剂与还原剂的物质的量之比是,当有5.4gAl发生反应时,转移电子的物质的量为.该反应的离子方程式为.
-
(6) 白色沉淀变成灰绿色再变成红褐色沉淀的化学方程式:.
下列物质长期露置于空气中会变质,但不是发生氧化还原反应的是( )
A . Na
B . 氯水
C . FeSO4
D . NaOH
下列物质中,不能使淀粉碘化钾试纸变蓝的是( )
A . 氯水
B . 溴水
C . 碘水
D . 食盐水
酸性重铬酸钾(K2Cr2O7)溶液可以将乙醇氧化为乙酸,20.0 mL 1.00 mol·L−1 酸性 K2Cr2O7 溶液与1.38 g 乙醇恰好完全反应,则K2Cr2O7 的还原产物是( )
A . CrO2-
B . Cr(OH)3
C . Cr3+
D . Cr2+
由含[Cu(NH3)4]Cl2的蚀刻废液制取[Cu(NH3)4]CO3溶液的流程如图:
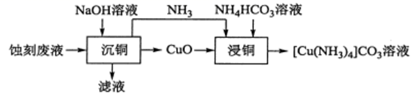
下列有关说法错误的是( )
A . 上述制取流程不涉及氧化还原反应
B . “沉铜”在加热条件下进行,发生反应的离子方程式为[Cu(NH3)4] 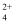 +2OH-
+2OH- 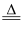 4NH3↑+CuO↓+H2O
C . “滤液”中大量存在的离子有Na+、
4NH3↑+CuO↓+H2O
C . “滤液”中大量存在的离子有Na+、  、Cl-和OH-
D . “浸铜”时温度过高可能导致铜的浸出率下降
、Cl-和OH-
D . “浸铜”时温度过高可能导致铜的浸出率下降
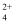 +2OH-
+2OH- 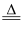 4NH3↑+CuO↓+H2O
C . “滤液”中大量存在的离子有Na+、
4NH3↑+CuO↓+H2O
C . “滤液”中大量存在的离子有Na+、  、Cl-和OH-
D . “浸铜”时温度过高可能导致铜的浸出率下降
、Cl-和OH-
D . “浸铜”时温度过高可能导致铜的浸出率下降
某溶液中可能含有Na+、  、Fe2+、K+、I-、
、Fe2+、K+、I-、  、
、  ,且所有离子物质的量浓度相等。向该无色溶液中滴加少量氯水,溶液仍呈无色。下列关于该溶液的判断正确的是( )
,且所有离子物质的量浓度相等。向该无色溶液中滴加少量氯水,溶液仍呈无色。下列关于该溶液的判断正确的是( )
 、Fe2+、K+、I-、
、Fe2+、K+、I-、  、
、  ,且所有离子物质的量浓度相等。向该无色溶液中滴加少量氯水,溶液仍呈无色。下列关于该溶液的判断正确的是( )
,且所有离子物质的量浓度相等。向该无色溶液中滴加少量氯水,溶液仍呈无色。下列关于该溶液的判断正确的是( )
A . 肯定不含I-
B . 肯定含有  、I-
C . 肯定不含
、I-
C . 肯定不含  D . 肯定含有
D . 肯定含有 
 、I-
C . 肯定不含
、I-
C . 肯定不含  D . 肯定含有
D . 肯定含有 
已知 Pb3O4 与稀 HNO3 发生反应 I:Pb3O4+4H+=PbO2+2Pb2++2H2O,PbO2 与酸化的MnSO4 溶液发生反应 II:5PbO2+2Mn2++4H++5SO  =2MnO
=2MnO  +5PbSO4+2H2O。下列说法正确的是( )
+5PbSO4+2H2O。下列说法正确的是( )
 =2MnO
=2MnO  +5PbSO4+2H2O。下列说法正确的是( )
+5PbSO4+2H2O。下列说法正确的是( )
A . 类比 Fe3O4 , Pb3O4 可写成 PbO·Pb2O3 的形式
B . 反应 I 中 Pb3O4 既是氧化剂也是还原剂
C . Pb3O4 可与浓盐酸反应生成 Cl2
D . 由反应 I、II 可知,氧化性:MnO  >HNO3>PbO2
>HNO3>PbO2
 >HNO3>PbO2
>HNO3>PbO2
按题目要求填空:
-
(1) 根据下列物质填空:①蔗糖 ②熔融
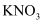 ③氯气 ④NaOH固体。上述物质中不能导电,但属于电解质的是(填序号);③的电子式是。
③氯气 ④NaOH固体。上述物质中不能导电,但属于电解质的是(填序号);③的电子式是。
-
(2)
 是一种酸式盐,请填写下列空白:
是一种酸式盐,请填写下列空白: ①
 溶液与
溶液与  溶液反应的离子方程式为。
溶液反应的离子方程式为。②与0.1mol/L
 溶液中
溶液中  浓度相同的
浓度相同的  溶液的物质的量浓度为。
溶液的物质的量浓度为。 -
(3) 已知:
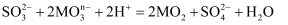 ,则
,则 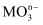 中M的化合价是。
中M的化合价是。
-
(4) 已知钙的金属活泼性介于钾和钠之间,其化学性质与钠相似。钙与氧气在一定条件下可以反应生成过氧化钙(
 ),其性质与过氧化钠相似。回答下列问题:
),其性质与过氧化钠相似。回答下列问题: ①标出钙与水反应的电子转移方向和数目:。
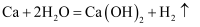
②请写出
 与水反应的化学方程式;若向反应后的溶液中立即滴入酚酞,预期的实验现象可能是。
与水反应的化学方程式;若向反应后的溶液中立即滴入酚酞,预期的实验现象可能是。
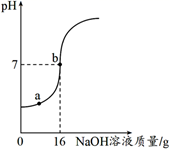
实验室欲测定一瓶标签破损的稀硫酸中溶质的质量分数。现取10 g稀硫酸样品,将5%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的不断加入,溶液的pH变化如右图所示。试回答:
-
(1) a点溶液中含有的溶质有。
-
(2) 当pH=7时,消耗NaOH溶液中溶质的质量为g。
-
(3) 计算稀硫酸溶液中溶质的质量分数。(要求写出必要的计算过程)
下列工业生产中不涉及氧化还原反应的是( )
A . 合成氨
B . 制漂白粉
C . 冶炼Fe
D . 煅烧石灰石
某化学研究小组设计利用硝酸工业尾气(含NO、NO2)制备亚硝酸钠(NaNO2)的工艺流程如下:
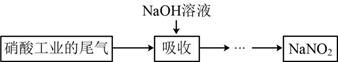
已知:NO和NO2的物质的量比为1:1时发生的化学方程式:NO+NO2+2NaOH=2NaNO2 + H2O。下列说法错误的是( )
A . NaNO2中N元素为+3价
B . NO+NO2 +2NaOH =2NaNO2 + H2O的反应中NO作还原剂
C . 用尾气制备的NaNO2中可能含有NaNO3
D . 尾气中NO2的含量越高,NaNO2的纯度越高
最近更新
- 下图漫画《你的心境》所体现的哲理是( )A.人们在意识指导下自发改造客观世界 B.意识是脱离客观存在的主观映象 C.
- 一打点计时器固定在倾角为θ的斜面上,一小车拖着穿过打点计时器的纸带从斜面上滑下,打出的纸带的一段如图所示,。纸带上0、1
- 某旅游城市为向游客介绍本地的气温情况,绘制了一年中各月平均最高气温和平均最低气温的雷达图.图中A点表示十月的平均最高气温
- 在氮源为14N和15N的培养基上生长的大肠杆菌,其DNA分子分别为14N-DNA(相对分子质量为a)和15N-DNA(相
- 图1为“正常年份南太平洋部分海区水温分布图”,图2为“厄尔尼诺年的南太平洋部分海区水温分布图”,读图并按要求完成下列问题
- — Everything for the project has been progressing smoothly s
- “山中之王”老虎的食性是( ) A.肉食性 B.植食性
- The lecture given by the professor from NanjingUniversity co
- 下列实验设计及其对应的离子方程式均正确的是A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+ =Cu2+ + 2Fe
- 下列各组函数中,的图象完全相同的是 A. B. C.
- 《中华人民共和国个人所得税法》规定,公民全月工资、薪金所得不超过3500元的部分不必纳税,超过3500元的部分为全月应
- 当进行某杂交实验时,获得下图所示结果: AaBb ╳ aaBB ↓ Aabb aaBb
- 白种人主要分布在: A、亚洲 B、非洲 C、欧洲 D、南美洲
- 20世纪30年代蒋廷黻的《中国近代史大纲》称:近百年的中华民族根本只有一个问题,即追求近代化。如果这一观点成立,是基于它
- .下列说法正确的是 A.氧的摩尔质量是32
- a>2,b>2,则有()A.ab=a+bB.ab≤a+bC.ab>a+bD.ab<a+b
- (09天河区五校期末联考)一种细胞器的部分生物膜是怎样转移到另一种细胞器的 A.随着细胞质
- 已知集合A={x|x2-5x+6=0},B={a,2,2a-1}. (1)求集合A; (2)若A⊆B,求实数a的值.
- 下列物质的分类合理的是 A.碱性氧化物:Na2O、CaO、Mn2O7、Na2O2 B.碱:NaOH、KOH、Ba(OH)
- 2.依次填入下面一段文字横线处的语句,衔接最恰当的一组是( ) 今天的日子很短,正在自己的脚下悄悄地流逝______



